100种化学反应
1. Arndt -Eistert 反应
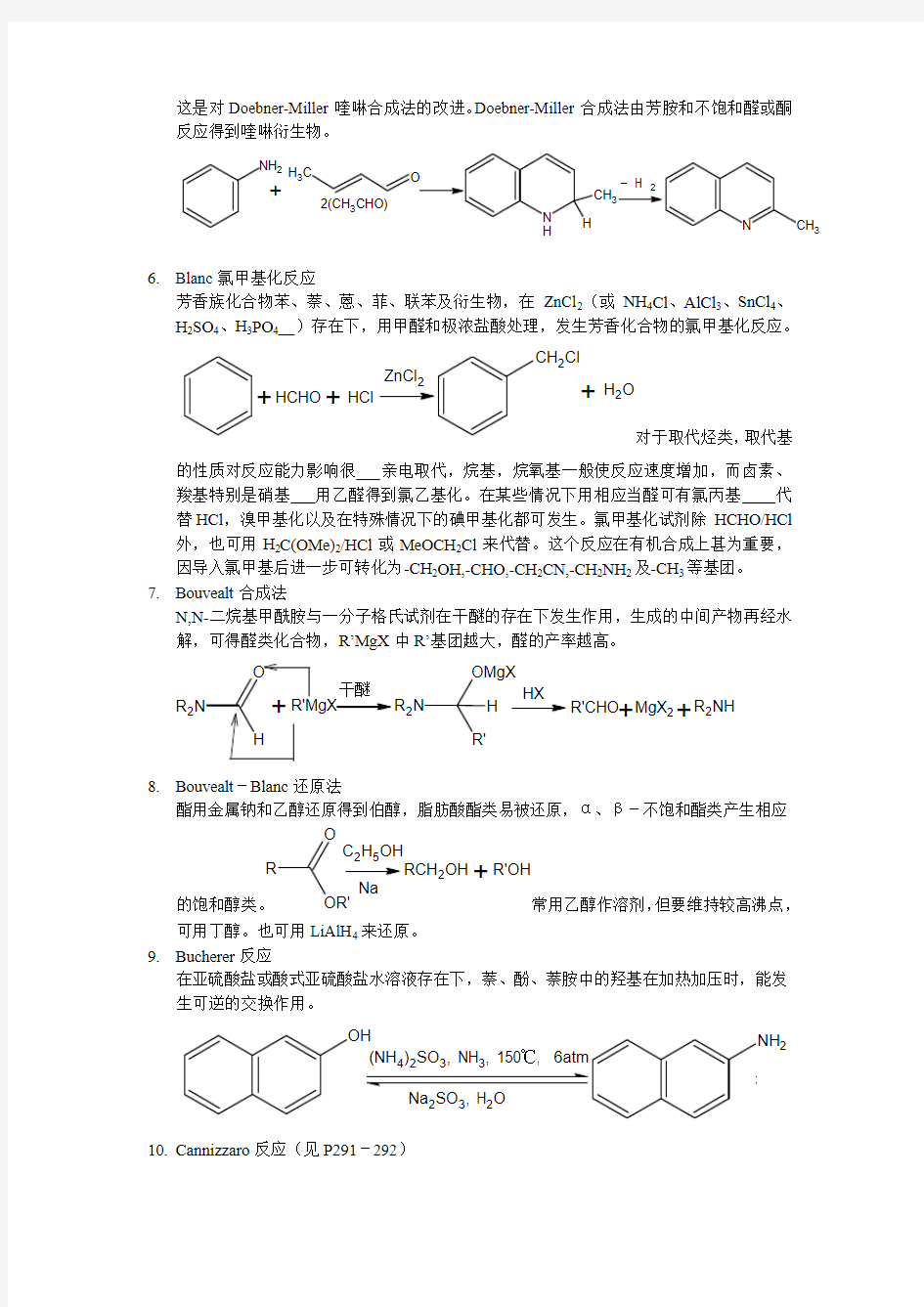
醛、酮与重氮甲烷反应,失去氮并重排成多一个CH 2基的相应羰基化合物,这个反应对于环酮的扩环反应很重要。
O +CH 2N 2
-2
N
+
N
-N
2
重排
O
2. Baeyer -Villiger 氧化
应用过氧酸使酮氧化成酯。反应中在酮的羰基和相邻的碳原子之间引人一个氧原子。如
由樟脑生成内酯:O
CH 3
C
H 3CH 3
O
O
C
H 3CH 3H SO 有时反应能生成二或多过
氧化物,但环状酮转变为内酯能得到单一的预期产物。合适的酸为过硫酸(Caro’s 酸)、过氧苯甲酸、三氟过氧乙酸。除环酮外,无环的脂肪、芳香酮也可发生此反应。二酮生成酸酐类、α、β-不饱和酮得到烯醇酯类。 3. Bechamp 还原(可用于工业制备)
在铁、亚铁盐和稀酸的作用下,芳香族硝基化合物能还原成相应的芳香胺。 C 6H 5-NO 2
+ 2Fe + 6HCl C 6H 5-NH 2 + 2FeCl 3 + 2H 2O 。
当某些盐(FeCl 2、FeCl 3、FeSO 4、CaCl 2等)存在时,所用酸无论是过量还是少量,甚至在中性溶液中都能够进行这种还原。此方法适用于绝大部分各种不同结构的芳香族化合物,有时也用来还原脂肪族硝基化合物。 4. Beckmann 重排
醛肟、酮肟用酸或路易斯酸处理后,最终产物得酰胺类。单酮肟重排仅得一种酰胺,混酮肟重排得两种混合酰胺。但一般质子化羟基的裂解和基团R 的转移是从相反的位置同
时进行的。OH
R'
R
R
O
N R'
R
R'
NHR O
无论酯酮肟和芳酮肟都会发生此反应。环酮肟重排得内酰胺,这在工业生产上很重要,利用此反应可帮助决定异构酮肟的结构。 5. Beyer 喹啉类合成法
芳香伯胺与一分子醛及一分子甲基酮在浓盐酸或ZnCl 2存在下,反应生成喹啉类化合物。
NH 2
H
+
+
R'CHO
RCOCH
这是对Doebner-Miller 喹啉合成法的改进。Doebner-Miller 合成法由芳胺和不饱和醛或酮反应得到喹啉衍生物。
NH 2
H
3
+
C
H 32(CH 3CHO)
6. Blanc 氯甲基化反应
芳香族化合物苯、萘、蒽、菲、联苯及衍生物,在ZnCl 2(或NH 4Cl 、AlCl 3、SnCl 4、H 2SO 4
、H 3PO 4 )存在下,用甲醛和极浓盐酸处理,发生芳香化合物的氯甲基化反应。
+++HCHO HCl
H 2O
2Cl
对于取代烃类,取代基
的性质对反应能力影响很 亲电取代,烷基,烷氧基一般使反应速度增加,而卤素、羧基特别是硝基 用乙醛得到氯乙基化。在某些情况下用相应当醛可有氯丙基 代替HCl ,溴甲基化以及在特殊情况下的碘甲基化都可发生。氯甲基化试剂除HCHO/HCl 外,也可用H 2C(OMe)2/HCl 或MeOCH 2Cl 来代替。这个反应在有机合成上甚为重要,因导入氯甲基后进一步可转化为-CH 2OH,-CHO,-CH 2CN,-CH 2NH 2及-CH 3等基团。 7. Bouvealt 合成法
N,N-二烷基甲酰胺与一分子格氏试剂在干醚的存在下发生作用,生成的中间产物再经水解,可得醛类化合物,R’MgX 中R’基团越大,醛的产率越高。
R 2N
H
O
R'MgX
干醚
R 2N
OMgX
H
R'CHO ++MgX 2
R 2NH
+
8. Bouvealt -Blanc 还原法
酯用金属钠和乙醇还原得到伯醇,脂肪酸酯类易被还原,α、β-不饱和酯类产生相应
的饱和醇类。R O
C 2H 5OH
Na RCH 2OH R'OH
+
常用乙醇作溶剂,但要维持较高沸点,
可用丁醇。也可用LiAlH 4来还原。
9. Bucherer 反应
在亚硫酸盐或酸式亚硫酸盐水溶液存在下,萘、酚、萘胺中的羟基在加热加压时,能发生可逆的交换作用。
2
10. Cannizzaro 反应(见P291-292)
11. Chichibabin 吡啶类合成法
醛、酮类与氨或胺类在Al 2O 3等催化剂存在下,加压加热,脱氢脱水,生成吡啶类化合
物。
N
CH 3
3CH 3CHO
+++NH 3
3H 2O H 2
此法不易得纯产物,
还有其他化合物生成。 12. Chichibabin 对称合成法
碳酸二乙酯与三分子格氏试剂反应,中间产物经水解得到对称叔醇类。
H 5C 2O
2H 5
O
+3RMgX
R
OH
R
如果格氏试剂用量不足,与一分
子RMgX 反应生成酸,与二分子RMgX 反应生成酮。
H 5C 2O
2H 5
O
+
RMgX R H 5C 2H 5C 2O
OMgX
R
2H 5
O
H 2O
RCOOH +
C 2H 5OH
R
O
RMgX R
H 5C 2R
OMgX
R
2H 5
O
-MgXOC
2H 5
13. Chichibabin 胺化反应
含氮杂环碱类,如吡啶,喹啉或其衍生物与金属胺基化物在一起加热,则起胺化反应,生成氨基衍生物。产率一般为50%~100%。
N
N
NHNa
N
NH 2NaNH 2 溶剂
105- 110, ℃66- 76%H 2O
水解
反应中副产物很多:4-氨基吡啶,2,6-二氨基吡啶,2,4,6-三氨基吡啶,2,2’-联吡啶等。产物随温度、溶剂性质、氨基钠用量而异。Bechamp 还原法不适用于制备氨基吡啶类,因为吡啶类在一般情况下很难硝化,所以此反应是吡啶环中直接引入氨基的有效方法。
14. Chugaev 反应
该反应制备烯烃类。黄原酸酯在120~200℃时热解,顺利产生烯烃,相应 醇和氧硫化碳。黄原酸酯在热解前制备不须离析 除黄原酸酯外,其他的酯氨基甲酸酯,碳酸酯和羧酸酯 热解。特别是使用大分子量的羧酸酯(棕榈酸酯)的烯烃提供了有利条件。因为这些酯本身沸点高,而热解温度较低(约300℃),在液相中简单加热即可。 15. Claisen 重排
烯醇或酚类的烯丙醚在加热时,易起重排反应。烯丙基由氧原子上转移到碳原子上,这与弗利斯重排有相似之处。
CH 2CH=CH 2
OH
2CH=CH 2
200℃
OCH 2CH=CH 2
OH
CH 2CH=CH 2
200℃
;
Cl
OCH 2CH=CH 2
OH
CH 2CH=CH 2
250℃
醚分子中,
如临位未被取代则不起重排反应,产生复杂的热分解作用。此反应是在苯环引入丙基的简易方法,因为烯丙基可还原成丙基。 16. Claisen 缩合反应(P352~354) 17. Claisen -Schmidt 反应(P287) 18. Clemmensen 还原(P291) 19. Cope 消除反应
这个反应是由氧化叔胺消除羟胺来产生烯烃。反应在低温进行且产量较高,当加热到120℃时,具有光学活性的纯氧化叔胺1-(N,N-二甲氨基)-3-苯基丁烷就得到具有旋光性的纯3-苯基丁烯-1
,而且总是定量进行。
CH -
65
3
C
H 3CH 2
H 56
+(CH 3)2NOH
*△
20. Criegee 氧化法
乙二醇类在稀醋酸或苯溶液中,室温时用四乙酸铅进行很温和的氧化,两个相连的各带有游离羟基的碳原子之间的碳链就断裂,得到定量的醛酮类。此法用于研究醇类结构及制备醛酮类且产率很高。
R 22
OH OH
++
+
Pb(AcO)4R
O
R'
R'O
RHC
OH OH +Pb(AcO)4
RCHO R'CHO
21. Curtius 降解
库尔修斯降解是羧酸的迭氮化合物经加热脱氮重排成异氰酸酯,再经水解得伯胺类。若反应在惰性溶剂中进行,可以得到异氰酸酯,并能将它分离出来。
R
-O
N
+
-N 2
△
重排
O=C=N-R
H 2O
RNHCOOH
RNH 2
- CO 2
N
O
22.Darzens-Claisen反应
在无水惰性溶剂中,在碱性缩合剂的作用下,酸性强的α-卤代脂肪酸酯作为亚甲基部分和醛、酮反应,首先生成氯代醇酸酯,随即裂解放出氯化氢得到2,3-环氧酸酯,其再经水解脱羧便得到醛:
O
+H2C COOR
-HCl
C CH C CH
CH
-CO2
除α-氯代酸酯外,其他的C-H酸性化合物如邻和对硝基甲苯,环戊二烯等也能作为亚甲基部分与醛、酮反应。无水惰性溶剂为醚、苯或二甲苯。醛、酮可以是脂肪族、芳香族,也可以是α、β-不饱和醛酮,此反应对于形成C-C键的制备上很重要。23.Delepine反应
六亚甲基四胺与卤代烷反应,生成季胺盐。在稀酸作用下,其水解为伯胺。
C6H12N4 + RCH22-NC6H12N3
2
2
-NH3I + 6HCHO + 3NH4Cl RCH2-NH2NH2
溶剂为氯仿。卤代烷的反应活性为:RI>RBr>RCl,水解用95%乙醇和稀盐酸,最后能得到纯伯胺。
24.Dieckmann缩合
含有δ或ε位活泼亚甲基的二羧酸二酯在碱性催化剂存在下,分子内起“Claisen缩合”
反应,环化成β-酮酸酯类,其再经水解、脱羧而生成环酮类,当n=2,3时收率最高,高级二羧酸酯的缩合产率很低。
(CH2)n
CH2COOR
CH2COOR
(CH2)n
H
C
C
H2
25
COOR
-CO2
(CH2)n
H
C
C
H2
COOH
(CH2)n
H2
C
C
H2
C
25.Diels-Alder反应P83-84
26.Etard反应
具有侧链的芳烃,特别是甲基芳烃,在CS2中用二分子铬酰氯氧化,中间产物经水解得芳醛。
CH3CHO
CrO2Cl2
如果分子中有多个甲基,只可氧化一个,这是本反应的特征。
27.Favorskii重排
α-卤代酮用碱处理,消除卤素重排得羧酸:
X-CH 2-COR + NaOH
R-CH 2-COOH + NaX
环状α-卤代酮也可得到羧酸,
同时缩环:
O
H
H
COOH
NaOH -NaCl 环氧醚类和羟基缩酮类为副产物。在此条件下,二卤代酮也可发生重排,产生α、β-不饱和酸 28. Feist -Benary 合成法
此法用来合成呋喃类化合物,在吡啶或氨存在下,α-氯化羰基化合物或α,β-氯醚类与1,3-二羰基化合物发生缩合反应,生成呋喃类化合物。
R
C CH 2O
H 2C COOR'
C 3
O
O
R
COOR'
3
H
OC 2H 5Cl CH 2HC O
CH 2O
COOC 2H 5
CH 3
-C 2H 5Cl
CH 3COCH 2COOC 2H 5
-H 2O, -HCl
2+
29. Fischer 吲哚类合成法
醛和酮的苯腙类与ZnCl 2一起加热,发生重排,分子内缩合,脱氨环化等作用,最后生成吲哚类化合物。
大量脂肪醛酮和醛酸、酮酸及其酯的芳腙都能发生这个反应。但用这个方法,由乙醛的苯腙不能制得吲哚。通常,β-酮酯的苯腙的能得到吡唑啉酮。ZnCl 2、CuCl 和溴代物或其他重金属卤代物,H 2SO 4、HCl-酒精溶液或冰醋酸都可用作催化剂。 30. Friedel -Crafts 酰基化反应P276, P131-132 31. Friedel -Crafts 烷基化反应P130-131
芳烃与烷基卤试剂在路易斯酸存在下,生成烷基芳烃。
RCl
+
AlCl 3
R
+HCl
烷基化试剂除卤代烷外,醇类、烯烃、甲
苯磺酸烷基酯亦可。各种路易斯酸的催化效应:AlCl 3>FeCl 3> SbCl 5>SnCl 4>BF 3>TiCl 4>ZnCl 2。醇类至少需1mol 路易斯酸作催化剂。因为反应中生成的水使等摩尔的催化剂失去活性,对于卤代烷和烯烃来说,催化量就已足够。酚类的反应较令人满意(P258~259),而低碱度的芳烃如硝基苯、吡啶都不能反应。 32. Fries 重排
在当量数AlCl 3存在下,加热脂肪或芳香羧酸苯基酯,酰基发生重排反应,脂肪酸苯基酯比芳香酸苯基酯更易进行。根据反应条件,重排可以到邻位,也可以到对位。在低温(100℃以下)时主要形成对位产物,在高温时一般得到邻位产物。
3C
OH
3
OH
H 3C
3
H 3C
CH O
催化剂除AlCl 3外,也可用BF 3、ZnCl 2、FeCl 3。催化剂不同,生成邻、对位异构体的比例也不同。用硝基苯作溶剂有利于重排,可在低温时进行。氯苯、CS 2、CCl 4可用作溶剂。但没有溶剂反应也可以进行。原料结构影响异构体的相对比例。此反应对于合成酰基酚类很重要。
33. Gabriel 氨基酸合成法P454
邻苯二甲酰亚胺钾与α-卤代脂肪酸作用,生成物经水解得到氨基酸。
NK
O
N
O
COOC 2H 5
+X
COOC 2H 5
-KX
3H 2O(H +
)△
+
+COOH
COOH
C 2H 5OH
R
2
COOH
34. Gabriel 伯胺合成法P372-373 35. Gattermann 醛类合成法
酚类或酚醚类与无水HCN 和HCl 混合物在无水AlCl 3或ZnCl 2存在下发生反应,生成的中间物经水解,醛基便导入羟基、烷氧基的邻位或对位。
O
H CHO
O
H OHC
O
H +
HCN
+
HCl
AlCl 3
3
H 3CO CHO
HCN
HCl
+
+
AlCl 3
40 - 50℃
Gattermann 合成法不仅适用于酚类和酚醚类,也适用于某些杂环化合物,如呋喃、吡咯和吲哚的衍生物(但未经取代的不能反应),也适用于噻吩。醛基总是优先进入活化基团的对位,具有明显的选择性,只有对位被占据才发生邻位取代。
C
H 3C
H 3CHO
N
H N
H HCN HCl +
AlCl 3100, ℃39%
HCN
HCl
+40℃
36. Gattermann -Adams 合成法
这是Gattermann 醛类合成法的改进。由盐酸作用于Zn(CN)2,从而释放出HCN ,避免使用无水氰化氢。
OH
C
H 3CH(CH 3)2
OH
CH(CH 3)2
C
H 3Zn(CN)2
+HCl +AlCl 3
99%
37. Gattermann -Koch 合成法P276 38. Grignard 反应P185-186 39. Hantzsch 吡咯类合成法
在氨或伯胺类作用下,α-卤代甲基酮和乙酰乙酸乙酯进行环化反应,再消除HCl 和H 2O ,产生吡咯羧酸酯。
COOC 2H 5CH 2
C
H 3C
O
Cl
CH 2
C
O
+
NH 3-H 2O
N H
R
H 3C
C 2H 5OOC
40. Hantzsch 吡啶类合成法
CH 2
ROOC
H 3C
R'
H
H
N H
COOR CH 2
CH 3
O COOR CH
3C
2R'H
COOR
O
CH 3
N H
N
R'
H
ROOC
3
H 3C
R'
ROOC
COOR
3
H 3C
2++
+
乙酰乙酸酯和氨或伯胺及醛类反应,可得到二氢吡啶,其再用亚硝酸脱氢,产生吡啶类衍生物。此反应对吡啶类衍生物的合成是非常有用的。 41. Hinsberg 反应P378 42. Hoesch 合成法
这是Gattermann 醛类合成法的改进。Hoesch 用腈代替氢氰酸,便得到酮。
O
H OH
OH
O
H NH.HCl
O
H OH
O
N
H N
H R
NH.HCl
N H R
O
HCl
RCN RCN
43. Hoffmann 胺降解
胺类经过彻底甲基化后,生成季胺盐。其再经AgOH 作用,生成相应的季胺氢氧化物。将此在100~200℃时加热分解,产生叔胺、烯烃。反应中通过亲核羟基离子的作用,使带有最少数烷基的β-碳原子上失去一个质子而生成水,裂解出叔胺得到烯烃。
H 3C
H 2C
H 2C
C H 2
3
3H 3C
2C
CH 2H 3C
N
CH 3
CH 2CH 2CH 3H 2O
OH
++在各种取代的季胺化合物中,甲基比具有两个或多个碳原子的烷基有较大的韧性。因此一般不能被消除。对于没有β-者也不发生消除,而是取代。
(CH 3)4NOH 3)3N + CH 3OH 130~135℃
44. Hoffmann 烷基化反应
卤代烷与氨或胺的反应。反应最后产物是一个复杂的混合物。如果混合物的沸点有一点的差距,可用分馏的方法将其一一分离,这适用于工业上大规模的制备。 H
3N + RX H 3NR + X RNH 3 + NH RNH 2 + NH 4RNH 22NH 2 + X R 2NH 2 + NH 2NH + NH 4R 2NH + RX
3NH + X R 3NH + NH 3
R 3N + NH 4
也可利用原料摩尔比不同,控制反应温度、时间和其他条件,使其中某一个胺为主要产物。脂肪卤代烷的反应速度:RI>RBr>RCl 。仲、叔卤代烷易与氨作用失去一分子卤化氢成为烯。芳香卤代物一般不易与氨或胺发生反应,只有在高温高压及催化剂存在时或卤素的邻、对位有一个或多个强吸电子基团存在时,才可发生此反应。
C 6H 5Cl
NH C 6H 5NH 2
Cl
NO 2
NHCH 3
NO 2
+
+
CH 3NH 2
CU O, 200℃C H OH 此法可制备一级、二级、三级胺,但不易得到纯化合物。 45. Hoffmann 酰胺降解P339 46. Hoffmann 消除反应
仲烷基、叔烷基进行消除反应时,被消除对质子系来自带有最少烷基的β-碳原子上,产生的烯烃在其双键上具有最少数目的烷基。
H 3C
H 2C
C 3
CH 3
H 3C
H 2C
C
CH 2
CH 3
- H 2O
这种消除叫Hofmann 消除或Hofmann 定向。这种烯烃叫Hofmann 烯烃。 47. Knoevenagel 反应P354 48. Kolbe 烃合成法
此法通过电解羧酸盐制备烷烃。一般使用高浓度羧酸钠盐,在中性或弱酸性溶液中进行电解。用铂电极于较高的分解电压和较低的温度下进行反应,阳极处产生烷烃和二氧化碳,阴极处产生NaOH 和H 2。羧酸原子数不宜太多或太少,最好在10个左右。
2CH 3COONa + 2H 222如果用两种羧酸钠的混
合溶液进行反应,生成三种不同的烷烃,其性质相近,难以分离,故无制备意义。用二元羧酸酯盐的水溶液进行电解,可得到二元羧酸酯,这在制备上是可行的。
H 2C
H 2C
H 2C H 2C
H 2C H 2C
2
+ 2CO 2
49. Kolbe 腈合成法
碱性氰化物与卤代烷的无水醇溶液在一起加热,便生成腈。通常利用此反应合成多一个
碳原子的羧酸。RX + NaCN
RCN + NaX 反应中异腈为副产物,可由其特殊
气味识别。形成异腈的量取决于所用金属氰化物的性质。如AgCN 得到100%异腈,
CuCN:56%,Ca(CN)2:11%,Zn(CN)2:2.6%,用KCN、NaCN仅有少量的异腈产生。
烷基化试剂反应速度:RI>RBr>RCl,伯烷基>仲烷基,叔烷基易发生异构反应,一般不用。
50.Kolbe-Schmitt反应
在绝对无水的情况下,干燥的CO2和苯酚钠在压热器中加热180~200℃,生成大约25%水杨酸钠盐,其再酸化即得水杨酸。
ONa
OH OH
COOH
+
CO
2++
Schmitt对此反应进行改良,在低温125℃、4~7atm时反应,几乎可得理论量的水杨酸。
51. Kucherov 反应
乙炔在Hg 2+盐和稀硫酸存在下直接水合生成乙醛,单取代乙炔可生成甲基酮。
C
H CH
++H 2O
CH 3CHO
RC CH
Hg ++
/ H 2SO 4
Hg ++
/ H SO H 2O
RCOCH 3
52. Lebedeff 合成法
在高温下(400~500℃)乙醇与特种催化剂硅酸盐、Al 2O 3、ZnO 混合物作用,脱氢脱
水得1,3-丁二烯。
++2CH 3CH 2C
2CH 2
H 2H 2O
丁二烯的产
率大约为20%,其他副产物如戊烷、己烷、己烯、己二烯、丁醇、醛、酮都有,所以此反应制备意义不大。 53. Leuckart 反应
在甲酸(甲酰胺、甲酸铵)作还原剂的情况下,加热胺和羰基化合物,就发生胺的烷基
化反应。
R
NH O
R"
N
R R'
R"++++CO 2H 2O
通过
这种反应可使伯胺、仲胺及氨发生烷基化反应,但以叔胺为最妥。因为伯胺、仲胺总是
有多烷基化副产物形成。特别是很活泼的甲醛,同时总是生成完全甲基化的胺。高沸点芳香醛和酮产物为40~90%,低分子量脂肪醛和酮不能得到满意大结果。反应中由少量MgSO 4或MgCl 2催化,起还原作用的甲酸经常是过量,每摩尔羰基化合物需2~4mol 甲酸。
54. Lieben 碘仿试验P289 55. Lossen 降解
氧肟酸或其酰基衍生物,在惰性溶剂或最好在亚硫酰氯、乙酸酐、P 2O 5存在下加热分解
而得到异氰酸酯。O
R
O
R
H OH +NH 2OH
(Ac)
56. Mannich 反应
这是具有α-活泼氢化合物的胺甲基化反应。一般是甲醛与胺及具有α-活泼氢化合物同时反应,胺甲基取代一个α-活泼氢:反应一般在水、醇或醋酸溶液中进行。
N
H 3
CH 3
H 3CCOCH 2CH 2N
CH 3
3
NH 2CH 2COCH 3C
3
3
CH 3COCH 3
++HCHO .HCl
NaOH
.HCl 甲醛可以是甲醛溶液、三聚或多聚甲醛,胺一般是仲胺盐酸盐,如二甲胺、六氢吡啶等等盐酸盐,反应中生成单一产物。伯胺或氨副产物多不常使用。此反应合成范围广,不但醛和酮的活泼氢可以进行反应,其他化合物如羧酸、酯、酚或其他杂环化合物(如噻吩、吡咯、吲哚等)的活泼氢也都可以,特别值得注意的是在合成体系及氨基酸方面的应用。
57. Meerwein -Ponndorf -Veriey 还原
醛、酮与醇镁或醇铝反应,醛酮被还原成醇,而醇盐则被氧化成相应的羰基化合物。
R
O
R'
H
Al
O
R
R
H
Al R'
+
_3
/3
3
+
反应中,醇盐与加入的醇处于平衡状态,当催化量的醇盐存在时,用醇作还原剂也可发
生反应,醇铝溶于有机溶剂,在蒸馏时不被分解。它的螯合倾向较大,所以醇铝特别适合Meerwein -Ponndorf -V eriey 还原。仲醇盐比伯醇盐更好,产生的副反应当可能性更小。上式为平衡反应,要得到好的收率必须不断从平衡中出去由醇铝所生成的羰基化合物。丙酮易挥发,可以蒸出,使平衡破坏,促使反应向右移动,所以用异丙醇作还原剂。如果用乙醇作还原剂,最好用氮气流把生成的乙醛从反应混合物中带走。此反应特点:(1)双键(即使是与羰基共轭的双键)能够保留而不被还原;(2)硝基与卤素不被还原;(3)β-二羰基化合物通常不能进行此反应,因为会生成酸性较强的铝化物沉淀。 58. Meyer 合成法
卤代烷与金属亚硝酸盐反应,合成硝基烷。亚硝酸酯为副产物。用碘代甲烷、乙烷、正丙烷、异丙烷反应很顺利。但用高分子量卤代物容易发生副反应。伯、仲、叔烷基不同,
得到不同的主要产物:+RCH 2X
NaNO 2
RCH 2NO 2
NaX (主要产物硝基烷)
,
++
R 2CHX
NaNO NaX
2CHONO (亚硝酸酯较多), ++NaNO 2
NaX
R 3CONO
R 3CX
(全为亚硝酸酯)。
59. Meyer -Schuster 重排
在酸性催化剂存在下,乙炔甲醇类重排成α、β-不饱和酮类。芳基取代的乙炔甲醇最
易重排:H 56C C C 6H 5H 5C 6C CH H 5C 6
H 56
C C 6H 5+ 60. Michael 加成
在碱性催化剂(哌啶、二乙胺、NaOR 等)存在下,活泼酸性CH 2基与活泼碳碳双键(α、β-不饱和羰基化合物、酯、腈)发生亲核加成。
H 5C 6
CH
CH
COOR
5C 6
HC
CH 2COOR
COOR COOR
+
H 2C
COOR
COOR
H 5C 6
2COOH
CH 2COOH
活泼CH 2基化合物可用通式
R
A
B 来表示。其中A ,B 可以是-COOR 、-COR 、-
CN 、-CONH 2、―NO 2、―SO 2R 、―CHO 等。亚甲基越容易放出质子,就越容易发生加成反应。活泼碳碳双键化合物可用通式-RC =CH -来表示。R 为-COOR 、-COR 、
-CN 、-CONH 2、―NO 2、―SO 2R 。乙炔类和醌类也可以发生这种反应。反应活性随双键极性增加而增大,在反应中常发生醇醛缩合和Claisen 缩合,使反应复杂。若使用相应的烯胺作为酸性亚甲基部分,反应中由碱性引起的副反应便可预先避免。 61. Nef 合成法
乙炔钠与羰基双键加成,水解即得乙炔醇类:
O
C H 3CH 3+
NaC ONa C
H 33
H O
CH OH C
H 33
苯乙酮和苯基乙炔钠在醚溶液中作用能发生相似的反应。
62. Oppenauer 氧化P274
在叔丁醇铝存在下,伯、仲醇用过量的酮或醌类使之氧化成相应的醛或酮。
R
OH
++
(H 3C)2C [(CH )C-O]Al
(CH 3)2CHOH R O 常用的酮为丙
酮、2-丁酮、环己酮。在特殊情况下可同时加入适量的苯、甲苯或1,4-二氧六环作为稀
释剂,以减少生成物发生缩合反应的机会。本法也适用于氧化不饱和甾族醇类及由不饱和醇制备不饱和酮。 63. Pechmann 反应
在浓硫酸、AlCl 3、P 2O 5等脱水剂存在下,酚类与β-酮酸酯类进行缩合反应,产生香
豆素类。
O
H OH
OH
O
H OH
O
O
H O
3
O
O
H OH
3
O
O
CH
RO C O
H CH 3
+
CH COCH COOC H 225改变酚为酮酯的结构可以合成具有各种取代基地香豆素类。取代基可以在苯环上、杂环上,也可同时在二者之上。酚间位有给电子基团能加速缩合,相反,吸电子基团则减缓反应进行。
64. Perkin 脂环化合物合成法
在乙醇钠存在下,含有活泼亚甲基化合物与二卤代物反应,生成环状羧酸酯,再经水解、加热、脱羧即得环烷烃及其衍生物。
H 2C H 2C
H
2C
COOR
COOR
+
除三元环外,也可制得四、五、六、七元环,产率高低取决于环的大小。 65. Perkin 反应
芳香醛和酸酐,在此酸的碱性盐存在下,发生醇醛缩合反应,生成α、β-不饱和羧酸。
C 6H 5-CHO
(CH 3CO)2CH 3COONa
C 6H 5-CH=CH-COOH
+除简单芳香醛外,某些取代
芳香杂环醛也可用作羰基组分。甚至二芳基、芳基烷基酮与强活性亚甲基化合物也能够反应。脂肪醛反应产率很低。酸酐的α-碳原子上有两个氢原子方可作为亚甲基组分。高分子量比低分子量酸酐好。 66. Prileschajew 反应
烯烃与有机过氧酸作用,发生双键的过氧化作用。最常用的氧化剂为过氧苯甲酸,过氧苯乙酸。通常反应在丙酮、乙醚。氯仿中进行。反应条件温和,对于制备很有用。
R R
O
R
H
R H
OOH O
COOH
O
CH
C
2+
+
CH 2=CH-CH=CH 反应活性:R 2C=CR 2>RHC=CR 2>R 2C=CH 2≈RCH=CHR>RCH=CH 2>H 2C=CH 2.羧基和羰
基起相反作用。反应如在水溶液中进行,环氧化物将进一步水解成1,2-二醇类。 67. Prins 反应
在酸催化下,甲醛与烯烃加成,生成m -二噁烷类和1,3-二醇类。反应中也可生成不饱
和醇。C
H 3
CH 2C
H 3C 3CH 2CH 2O
CH 22
O
C H 3C
H 3+
2CH 2O, H
稀硫酸是最好的催化剂。
磷酸、BF 3也可用。叔基取代烯烃和不对称烯烃,如丙烯或1-丁烯最容易反应,m -二噁烷通过酸解可以转变成1,3-二醇类,再经脱水即可形成共轭二烯类。 68. Reformatsky 合成法P322 69. Reimer -Tiemann 合成法
在碱性水溶液中,苯酚与氯仿作用,产生邻、对位取代醛类。两种产物的比例取决于取代基和溶剂,如果在吡啶中进行,仅产生邻位醛,产率20~30%,很少超过50%。酚本
身可得到60%水杨醛。
OH
CHCl +
苯环上有吸电
子取代基,如-SO 3H 、-CN 、-COOH 、-NO 2能使苯环钝化,产率大约降为25%。只有含有游离酚式羟基的化合物,才能转变成醛。溴仿、碘仿及三氯乙酸同氯仿一样,容易进行反应。此法产率虽低,但操作简单,仍为合成酚醛的重要方法。 70. Riley 氧化法
活泼甲基或亚甲基化合物用二氧化硒氧化,甲基或亚甲基被氧化成羰基。羧酸为进一步氧化副产物。溶剂为乙醇、冰醋酸、乙酸酐、苯、二甲苯等,活泼甲基、亚甲基化合物除一般醛、酮(R(H)COCH 3)外,酯环酮、杂环重键结构及稠环体系也可以。
RCH 2CHO
CH
2
2
RCOCHO CH 3COCH CH 3COCHO
SeO SeO 本氧化剂具有选择性,广泛用于有机合成和有机物结构研究方面。 71. Rosenmund 还原
纯的芳香或脂肪类酰氯在Pa -BaSO 4催化剂存在下,常压氢化得到相应醛类。
RCHO
H 2(Pd-BaSO 4)
气相或液相本法主要缺点是生成的醛类易进一步被还原成醇或烃类。
为了防止这个副反应的发生,在反应体系中可加入适量“抑制剂”,硫脲、异氰酸苯酯、喹啉-硫等最为适用。它既能防止副反应发生,又使酰氯的氢化不受到阻抑。本法广泛用于制备醛类,收率可达50~80%,有时达90%以上,但还原二酰氯制二元醛结果不好。在还原的化合物中,如有双键结构、硝基、卤素及酯基存在时不发生影响。但若有羟基存在,应预先酰化加以保护。 72. Rosenmund -Braun 芳腈合成法
芳香族溴化物和CuCN 在高温下反应,溴原子被氰基取代,生成芳腈类化合物。用稍过量的氰化物可获得极高产率的芳腈。加入少量的苄腈或CuSO 4能增进反应速度,对苯二
酚能抑制反应。
Br
CuBr
+
+
73. Sandmeyer 反应
芳香族重氮盐在亚铜盐
催化剂存在下,重氮基
(-N 2X )被-Br 、-Cl 、-CN 等置换,生成
芳香族取代物。反应副产物为二苯基衍生物。由于铜阳离子只起给予或接受电子的作用,所以当用容易氧化或还原
的取代基时便不需要使
用亚铜盐作催化剂。如用碘化物阴离子时,碘
离子本身即成为催化剂。此反应产率高,范围广。其重要性在于可以通过硝基使不能直接引入或不能引入预期位置的取代基到苯环上。 74. Saytzeff 消除反应
就仲烷基和叔烷基而言,消除反应可能按两种方向进行,导致双键位置不同的烯烃。双键上具有最多数目烷基的烯烃称为Saytzeff 烯烃。在Saytzeff 消除时,也有Hofmann 消除产物。一般来说,单分子消除反应主要产生Saytzeff 产物,如仲卤代烷和叔卤代烷以
+
R
C
C C C H X
H
C C C C H
C C C
C
H
αβ
βCH 3CH 2
CH 3
CH 3
H 3C
C H
CH 3CH 3
CH 3CH 2
CH 2
CH 3
+87.5%
12.5%
15%H 2SO 4
2
甲苯磺酸酯作溶剂脱卤化氢,以及仲醇和叔醇的脱水反应。在双分子消除反应中,反应取向主要取决于α位和β-位上取代基地性质以及脱去基团X 的性质。一般规则是:容易消去的基团有利于Saytzeff 倾向。 75. Schiemann 反应
Schiemann 反应是芳环上导入氟原子的反应。反应分两步进行,首先,芳香伯胺制成氟硼酸重氮盐,然后将其干燥后在适当条件下加热分解,生成芳香族氟化物。
++++++++C 6H 5-NH
2
2HCl NaNO 2C 6H 5-2Cl
NaCl 2H 2O
HBF 4
C 6H 5N 2BF 4
HCl
C 6H 5-F
N 2BF 3
重氮化
C 6H 5-2C 6H 5N 2BF △
氟硼酸重氮盐极
为安定,在大量制备时无危险。它大都具有一定的分解温度,分解速度很容易控制。氟化物收率一般为65%,有时达80~90%。 76. Schmidt 反应
在苯中,含羰基的化合物能被叠氮酸降解。一元羧基降解为胺,在两个羧基之间具有一个以上亚甲基的二元酸得到二元胺,醛类产生腈和胺的甲酰基衍生物,酮产生酰胺。
RCOOH ++
+
++
+
++
+
+
HN 3
H SO R-NH 2CO 2N 2HOOCCH 2CH 2COOH 2HN 2NCH 2CH 2NH 22CO 22N 2
RCHO RCN RNHCHO
RCOR
RCONHR 24H 2SO
424HN 3HN 3N 2
77. Schotten -Baumann 反应
在碱性化合物存在下,酰氯类使醇、酚等活泼氢化合物的酰化作用称为Schotten -Baumann 反应。芳香酰氯一般不如脂肪酰氯活泼,不易发生反应,对于易水解的酰氯类不适用于此法。上述反应中,生成的苯甲酸酯(分子量较高者)一般稍溶于水,结晶良好,具有固定熔点,所以Schotten -Baumann 反应常用来分离、鉴定醇和酚。
C 6H 5COCl
++++++NaCl H 2O ++NaCl H 2O
++NaCl H 2O ++NaCl H 2O
NaOH NaOH
NaOH
NaOH C 6H 5COCl C 6H 5COCl C 6H 5COCl ROH RNH RSH C 6H 5COOR C 6H 5COOAr
6H 5CONHR 6H 5COSR
78. Skraup 反应
在浓硫酸和氧化剂(硝基苯、As 2O 5、Fe 2O 3、苦味酸等)的存在下,苯胺和甘油反应合
成喹啉。NH 2
2
CH CH
O
H
+
式中丙烯醛是甘油由硫酸脱水而形成的,所用苯胺只要邻位无取代基者均可进行此反应。苯胺和甲基乙烯基酮缩合,生成4-
甲基喹啉。
NH 2
2
CH C
O
+
围极其广泛。 79. Sommelet 反应
卤代烷和六次甲基四胺作用,生成的季胺盐不需分离,再用60%稀醇液水解,生成醛类。
RCH 2X + (CH 2)6N H 2O
△
3 + CH 3NH 2
C 6H 5CH 2X + (CH 2)6N 4
6H 5CHO + NH 3H 2
O
[RCH 2(CH 2)6N 4]X
6H 5CH 2(CH 2)6N 4]X
80. Stephen 合成法
将干燥的HCl 气体通入腈类及无水SnCl 2的干醚饱和溶液中,氰基还原得到醛。
RCH + HCl
SnCl 2
反应结果好坏取决于腈的结构,邻甲苯腈和邻硝基苯甲腈
得到相应醛的收率都很低。
81. Stobbe 缩合反应
在醇钠作用下,丁二酸酯与醛酮缩合,得到烷叉丁二酸酯。丙酮和丁二酸酯缩合,产生
异丙叉丁二酸单酯:H 3C
H 3COOR H 2C
H 2C C
H 3H 3C
COOR
2COOH
+
NaOR'
亚甲基组分为丁二酸二甲(乙,t -丁)酯及其芳基、烷基、烷叉基衍生物。羰基组分除醛、酮氰酮外,在某些情况下,α、β-不饱和醛和酮、酮酯及二苯基乙二酮也可应用。 82. Stvecker 氨基酸合成法
在氨存在下,无水HCN 与醛的羰基加成,生成的α-氨基腈再经水解,产生α-氨基酸,产率75%。为方便起见也可用NaCN 代替HCN ,此法的缺点是氰化物剧毒,而且许多醛类难以得到。
R+CH NH)
(R R
CH3
N R
NH2
COOH
NH HCN H2O
H
83.Thorpe反应
在乙醇钠催化下,腈与活泼亚甲基化合物加成,生成亚胺化合物。如果一个分子内具有二个所需的官能团则发生环化反应。
ROOC CH2C H2
C COOR ROOC
H
C C CH2COOR
H2C H2C
CH2
CN
CH
C
C2H5ONa +
84.Tollens缩合
在Na2CO3或Ca(OH)2催化剂存在下,甲醛与含有α-H的醛和酮反应,生成多元醇类。
HCHO + CH3CHO + H2O2OH)4 + HCOOH
此反应实际上是醇醛缩合与交叉Cannizzaro反应的合并,利用此反应可制备多元醇类。
85.Ulmann反应
芳基卤代物在高温下(100~360℃)用铜粉处理,发生二芳基缩合反应。反应活性:ArI>ArBr>ArCl。碘化物特别适合。应用此法可制备对称和不对称二芳基类。
I
++
Cu CuI2
为调节反应,可用硝基苯、甲苯、苯或DMF作溶剂。
86.Ultee羟腈合成法
在微量KCN存在下,低温(0℃)时,醛、酮与无水HCN作用,产生羟腈化合物。
O R
R'
OH
CN R'
R
87.Urech羟腈合成法
金属氰化物在乙酸存在下,生成的氰化氢与醛、酮的羰基起加成反应生成羟腈。
O R
R'
OH
CN
R'
R
+ KCN + CH3COOH+ CH3COOK
丙酮的羟腈
产物可得78%。利用此反应可制得氨基酸、羟基酸。 88. Vilsmeier 反应
芳香化合物、杂环化合物及活性烯烃化合物用取代甲酰胺和磷酰氯处理,发生甲酰化作用得到醛类。常用的甲酰化试剂为N -甲基甲酰替苯胺。但DMF 和甲酰哌啶也可应用。
N
CHO
CH 3
3
3)2
N
+
POCl 3
在某些情况下,可用光气来代替磷酰氯,如烷基苯胺用N -甲基甲酰替苯胺和磷酰氯等克分子混合物处理,形成烷基氨基苯甲醛。该合成法应用范围较广,使用插烯的酰胺也可进行甲酰化,生成不饱和醛。常用溶剂为苯、氯苯和邻二氯苯,也可使用过量的DMF 。 89. V olhard -Erdmann 噻吩类合成法
丁二酸二钠盐衍生物在硫化磷的作用下,环化成噻吩类:此法可用来合成芳烷基噻吩,
并可控制取代位置,产率25~30%。ONa ONa
O
R
R'
S
R
R'
P S
90. Wagner -Meerwein 重排
此重排好像是片那酮重排的逆转。醇、卤代烷等进行消除反应时,位于季碳原子α-位的取代基(如羟基、卤素等)发生消除,同时烷基进行重排,生成Saytzeff 烯烃。如仲
醇的脱水反应:
H C CH 3
H 3C H 3C H 3C H C
H 3C
3C H 3C
H C 33
H 3C
H 3C
H 3H 3C CH 3
3
+CH 3-重排
-H +
91. Willaruson 合成法P236~237 92. Willgerodt -Kindler 反应
在高压下,烷基芳基酮被多硫化铵溶液氧化成碳原子数相同的ω-芳基烷基羧酸。
ArCO(CH 2)nCH 3(NH 4)2Sx H 2Ar(CH 2)n+1COOH
++式中甲基被氧化成
羧基,羰基被还原成次甲基。Rindler 进行改良,不用加压,用硫磺和仲胺(一般是吗啉)
Ar
C 3
Ar
H 2
C
C 2
Ar
H 2C + H 2S + R 2NH
S, R 2NH 2H 2O
有趣的化学小实验
有趣的化学小实验 第一篇:有趣的化学小实验黄皓锐 今天,我在家里做了一个实验。 首先,我拿来一个纸杯,往杯里倒满水,然后拿剪刀在纸杯底扎了一个小洞。我要计算一下,一杯水漏完,需要多久。我拿出手表计时,一分钟,两分钟,三分钟……过了十分钟,杯里的水漏完了。 我再拿出纸笔计算了一下,结果吓了我一大跳:照这样,一天24小时竟然可以漏掉144杯水!我想:平时经常看到有些水笼头关不紧,长年累月地流,该流掉多少宝贵的水啊!我觉得非常可惜。
我们一定要珍惜这宝贵的水啊! 第二篇:有趣的化学小实验莫雨翰 今天,王老师拿来一盒火柴,一管万能胶和一盆水,要给我做一个“会跳舞的火柴棍”的实验。 我们都很好奇,不知道火柴棍怎么跳舞。于是,我们都目不转睛地盯着王老师。王老师在一根火柴红红的一头涂上了厚厚一层万能胶,然后把它放在清水里。王老师说火柴上红红的是磷,它会和万能胶产生反应,生成气体,气体挥发时,火柴棍会竖在水中跳舞。真的吗?我们眼睛都一眨不眨地盯着那根火柴棍,可它一点变化也没有。我又耐心地等了几分钟,火柴棍还是没有跳舞。看来,今天的实验是失败了,我们心里真失望! 第三篇:有趣的化学小实验林子涵 今天,我做了一个神奇的实验。 中午,我把一个鸡蛋放在玻璃杯里,然后倒入醋精,立刻看到无数个小泡泡
从蛋壳上冒了出来。大约等到下午2:00的时候,我去看了下鸡蛋,我伸手一摸,妈呀,蛋壳软软的!真叫人吃惊啊。妈妈建议我把软鸡蛋放到清水中,看看会有什么变化。于是,我把醋倒掉,换了一杯清水,让鸡蛋沉没水中。过了一段时间,我把鸡蛋取出来,同原来的鸡蛋一比较,我发现鸡蛋变大了许多,真神奇呀。 小朋友,你们知道这是为什么吗?原来,醋精和鸡蛋壳发生了化学反应,让蛋壳变软了,放入清水以后,水渗入了软壳鸡蛋里,所以就变大了。 小朋友们,你们也来动手试试吧。 第四篇:有趣的化学小实验 如果把鸡蛋放在清水和盐水中会有什么不同呢?让我们做个实验吧。 我倒了一碗清水、一碗盐水。把鸡蛋放入清水中,鸡蛋沉下去了。我再把它放到盐水里,鸡蛋却浮了上来,好神奇呀!
高三一轮复习化学专题复习化学反应原理(一)
高三一轮复习化学专题复习——化学反应原理(一) 选择题(每小题只有一个选项符合题意) 1.废电池的污染引起人们的广泛重视,废电池中对环境形成污染的主要物质是() A.锌B.汞C.石墨D.二氧化锰 2.下列依据热化学方程式得出的结论正确的是() A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 B.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1 C.已知2C(s)+2O2(g)=2CO2(g) △H=a、2C(s)+O2(g)=2CO(g) △H=b,则a>b D.已知P(白磷,s)=P(红磷,s) △H<0,则白磷比红磷稳定 3.已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9kJ·mol-1,下列说法中正确的是()A.该反应中熵变、焓变皆大于0 B.该反应是吸热反应,因此一定不能自发进行 C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 () 4.下列说法不正确 ...的是 A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,。 若加入少量醋酸钠固体,则CH3COOH CH3COO-+H+向左移动,α减小,K a变小 C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 D.已知:Fe2O3(s)+3C(石墨)2Fe(s)+3CO(g),△H=+489.0 kJ/mol。 CO(g)+O2(g)CO2(g),△H=-283.0 kJ/mol。 C(石墨)+O2(g)CO2(g),△H=-393.5 kJ/mol。 则4Fe(s)+3O2(g)2Fe2O3(s),△H=-1641.0 kJ/mol 5.已知通过乙醇制取氢气有如下两条路线: a.CH3CH2OH(g)+H2O(g)=4H2(g)+2CO(g) △H =+255.6kJ·mol-1 b.CH3CH2OH(g)+1/2O2(g)=3H2(g)+2CO(g) △H =+13.8kJ·mol-1 则下列说法不正确 ...的是() A.降低温度,可提高b路线中乙醇的转化率 B.从能量消耗的角度来看,b路线制氢更加有利 C.乙醇可通过淀粉等生物原料发酵制得,属于可再生资源
很有趣的化学实验
?有趣化学实验 ?水中写字 ?灯塔实验 ?点水成冰 ?大象牙膏 ?肥皂制作 附件四:现场实验 实验1:水中写字 原料: 市售羧甲基纤维素(俗称化学浆糊,文具店有售;分子式为[C6H7O2(OH)2CH2COONa]n )三氯化铁(FeCl3)、硫氰化钾(KSCN)、亚铁氰化钾(K4[Fe(CN)6]) 仪器设备: 注射针筒、小烧杯、水果盘 原理: 一定浓度(约 1-2%)的羧甲基纤维素溶液,具有一定粘度,呈澄清透明状,有很好的流动性。该溶液有增稠、流动、赋形、保水、保护胶体、耐酸、耐盐等特性。铁盐是一种絮凝剂,水解产物能与溶液的羧甲基纤维素进行电中和脱稳、吸附架桥,形成粗大絮体。书写液体为铁盐,该絮体形成后在水中有一定的稳定性和塑形性,可以依此来在水中写字作画并有效抑制字画扩散。 FeCl3和KSCN反应变红色,和K4[Fe(CN)6]反应变蓝色,这是中学常用的铁盐
变色反应。利用能与FeCl3试剂产生颜色反应的KSCN试剂和K4[Fe(CN)6]等试剂,形成具有不同颜色的絮状物,而具有一定粘度的羧甲基纤维素溶液抑制了这些溶液的扩散和混合,因此水中形成了彩色的字画。 操作步骤: 1、称取羧甲基纤维素约 15克,加入 1000毫升清水,边加入边搅拌,至全部 溶解。溶液呈澄清透明状(市售羧甲基纤维素不纯,可能呈一定程度偏黄色,可考虑用纯试剂),将溶液倒入果盘中。 2、分别配置0.05摩尔/升的 FeCl3溶液、KSCN溶液和K4[Fe(CN)6]溶液于小 烧杯中。 3、用注射针管分别抽取一定量的KSCN溶液和 K4[Fe(CN)6]溶液,然后均匀调 和在水果盘中水溶液的左右两区(共分左中右三区,用以书写三个字)。 4、取注射针管,吸取FeCl3溶液,在盘中水溶液左中右三区分别写“化学年” 三个字。 实验现象描述: 水中写出了“化学年”三个字,三个字分别呈现鲜红色,黄色和海蓝色。 实验结果: 水中写出“化学年”三个不同颜色的字,字迹在水溶液中稳定存在。 注意事项及其他: 为保证实验效果,在左右两区将 KSCN溶液和 K4[Fe(CN)6]溶液调和到羧甲基纤维素溶液中时需要小心搅匀 实验2:灯塔实验 原料: 30%H2O2溶液,KIO32mol·L-1H2SO4),丙二酸MnSO4·H2O,淀粉。 仪器设备: 烧杯,锥形瓶,玻璃棒,试管。 实验操作:
化学反应原理期末试题含答案
化学反应原理期末试题含答案 1.下列有关说法正确的是() A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 B.NH3(g)+HCl(g))=NH4Cl(s)室温下能自发进行,说明该反应的ΔH<0 C.N2(g)+3H2(g) 3(g)ΔH<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 D.水的离子积常数K w随着温度的升高而增大,说明水的电离是放热反应 2.下列说法正确的是 A.将纯水加热至较高温度,K w变大、pH变小、呈酸性 B.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 C.向0.1 mol〃L-1醋酸溶液中加入少量冰醋酸,溶液的pH减小,醋酸电离程度变大 D.等体积、pH都为3的酸HA和HB分别与足量的Zn反应,HA放出的H2多, 说明HA的酸性小于HB 3. 分析下列硫燃烧时的能量变化图,判断有关热 化学方程式和说法正确的是( ) A.S(s,单斜)+O2(g)===SO2(g) ΔH=+297.16 kJ〃mol-1 B.S(s,正交)===S(s,单斜) ΔH=-0.33 kJ〃mol-1 C.S(s,正交)+O2(g)===SO2(g) ΔH=-296.83 kJ〃mol-1 D.单斜硫的稳定性大于正交硫的稳定性 4. 在密闭容器中进行反应CH4(g)+H2CO(g)+3H2(g) ΔH>0,测得c(CH4)随 反应时间(t)的变化如图所示。下列判断中正确的是( ) A.10 min时,改变的外界条件可能是减小压强 B.0~5 min内,v(H2)=0.1 mol〃(L〃min)-1 C.恒温下,缩小容器体积,平衡后c(H2)减小 D.12 min时,反应达平衡时,气体的平均摩尔质量不 再变化 5. CH4-CO2催化重整反应为: CH4(g)+ CO2(g) = 2CO(g) + 2H2(g) 。 已知:①C(s)+2H2(g)=CH4(g) ΔH=-75 kJ〃mol?1 ②C(s)+O2(g)=CO2(g) ΔH=-394 kJ〃mol?1 ③C(s)+ 1/2O2(g)=CO(g) ΔH=-111 kJ〃mol?1 则该催化重整反应的ΔH等于 A.-580 kJ〃mol?1 B.247 kJ〃mol?1 C.208 kJ〃mol?1 D.-430kJ〃mol?1 6. 向某密闭容器中加入0.3 mol A、0.1 mol C 和一定量的B 三种气体,一定条件下 发生如下反应:3A(g) +2C(g),各物 质的浓度随时间变化如图所示[t0~t1阶段的 c(B)变化未画出]。下列说法中正确的是 A.若t1=15s, A 的浓度变化表示t0~t1阶段的 平均反应速率为0.09 mol〃L-1〃s-1 B.t0~t1阶段,此过程中容器放出a kJ热量,该 反应的热化学方程式为:3A(g) +2C(g) ΔH=-50a kJ〃mol-1
2015年云南昆明理工大学化学反应工程考研真题A卷
2015年云南昆明理工大学化学反应工程考研真题A卷 一、判断题(正确的请打√,错的打×,全打一种符号的不得分,每题1.5分,共15分) 1.1 化学反应中任意反应组分均可作关键组分。 1.2 工业上一氧化碳与水蒸气生成二氧化碳和氢气的反应为均相反应。 1.3 间歇过程与连续过程的反应速率表示方法相同。 1.4 变容反应过程中反应混合物的体积和摩尔数均随反应率而变。 1.5 停留时间的分布函数与无因次停留时间的分布函数相等。 1.6 反应器中存在沟流时,其停留时间分布密度函数曲线存在滞后。 1.7 间歇反应器的优化可以平均生产强度最大为目标函数。 1.8 对绝热操作的CSTR,传热温差为反应器进出物料的温差。 1.9 催化剂的催化作用是通过改变反应前后的性质以降低反应活化能来实现的。 1.10 改变温度对外扩散速率的影响并不大。 二、填空题(每空1分,共15分) 2.1 化学反应器按操作方式可分为()、()和()。 2.2 写出化学反应速率的定义式(),其值应()。 2.3 当进口体积流量与标准状态下的体积流量相同时,空间时间τ=()/S V。 2.4 闭式系统是指在系统进口处(),在出口处()的系统。 2.5 平推流的无因次平均停留时间=()。 2.6 不可逆反应、可逆吸热反应、可逆放热反应等温操作时的最佳温度分别应选择()、 ()和()。 2.7 化学吸附按组分可分为()和()。 2.8 理想吸附和真实吸附的相同处是()。 三、简答题(每题12分,共48分) 3.1图1和图2对应的是什么反应,两图有什么相同和不同处? 图1 opt 3.2 什么是返混?为什么要消除返混?如何消除? 3.3 写出间歇反应器理论体积和实际体积的计算式,并说明式中符号的意义。 3.4 写出球形催化剂颗粒上等温一级可逆反应A B各步骤对反应都有影响时的宏观反应速率方 程,及各控制步骤下的反应速率式。 四、推导题(4.1:10分,4.2:4分,4.3:10分,共24分) 4.1由下列机理式导出动力学方程式:
人教版选修4《化学反应原理》期末测试题
化学反应原理期末测试题 测试时间:120分钟试卷满分:100分 第Ⅰ卷(选择题,共48分) 一、单项选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题) 1.废弃的电子产品称为电子垃圾,其中含铅、汞等有害物质、危害严重。下列对电子垃圾处理应予提倡的是() ①将电子垃圾掩埋地下②改进生产工艺,减少有害物质使用③依法要求制造商回收废旧电子产品④将电子垃圾焚烧处理 A.①③B.②④C.②③D.①④ 2.下列实验指定使用的仪器必须预先干燥的是() ①中和热测定中所用的小烧杯②中和滴定中所用的滴定管③配制一定物质的量浓度溶液中所用的容量瓶④喷泉实验中用于收集氨气的烧瓶 A.①②B.②③C.①④D.③④ 3.在一定温度下,可逆反应2A (g)+B (g) C (g)+D (g)达到平衡的标志是() A.C的生成速率和B的消耗速率相等 B.v正(A)=2v正(B) C.2v正(A)=v逆(B) D.反应混合物中A、B、C、D的浓度不再发生变化 4.某混合溶液中所含离子的浓度如下表,则M离可能为() 所含离子NO3-SO42-H+M 浓度/(mol·L-1) 2 1 2 1 A.Cl-B.Ba2+C.F-D.Mg2+ 5.强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)==H2O ( l ) ΔH=-57.3 kJ / mol,分别向1 L 0.5 mol / L的NaOH溶液中加入:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应时热效应分别为ΔH1、ΔH2、ΔH3,它们的关系正确的是() A.ΔH1>ΔH2>ΔH3B.ΔH1>H3>ΔH2 C.ΔH1=ΔH2=ΔH2D.ΔH1<ΔH3<ΔH2 6.下列事实中,不能用勒夏特列原理解释的是() A.对熟石灰的悬浊液加热,悬浊液中固体质量增加 B.实验室中常用排饱和食盐水的方式收集氯气 C.打开汽水瓶,有气泡从溶液中冒出 D.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 7.下列叙述中,正确的是() ①锌跟稀硫酸反应制取氢气,加入少量CuSO4溶液能提高反应速率②镀层破损后,白铁(镀锌的铁)比马口铁(铁锡的铁)更易腐蚀③电镀时应把镀件置于电解槽的阴极④冶炼铝时,把氧化铝加热成为熔融体后电解⑤钢铁表面常易腐蚀生成Fe2O3·n H2O A.①②③④⑤B.①③④⑤C.①③⑤D.②④ 8.2006年,科学家们发明了一种能够给电子设备提供动力的生物电池。该电池包括两个涂覆着酶的电极,它们
一些有趣又简单地化学实验
一些有趣又简单的化学实验 1、小木炭跳舞 亲爱的同学们,你们一定很喜欢化学吧,那么你就自行动手做一个有趣的小实验,这个实验的题目叫小木炭跳舞。取一只试管,里面装入3一4克固体硝酸钾,然后用铁夹直立地固定在铁架上,并用酒精灯加热试管。当固体的硝酸钾逐渐熔化后,取小豆粒大小木炭一块,投入试管中,并继续加热。过一会儿就会看到小木炭块在试管中的液面上突然地跳跃起来,一会儿上下跳动,一会儿自身翻转,好似跳舞一样,并且发出灼热的红光,有趣极了。请你们欣赏一下小木炭优美的舞姿吧。你能回答小木炭为什么会跳舞吗? 答案 原来在小木炭刚放入试管时,试管中硝酸钾的温度较低,还没能使木炭燃烧起来,所以小木炭还在那静止地躺着。对试管继续加热后温度上升,使小木炭达到燃点,
这时与硝酸钾发生激烈的化学反应,并放出大量的热,使小木炭立刻燃烧发光。因为硝酸钾在高温下分解后放出氧来,这个氧立刻与小木炭反应生成二氧化碳气体,这个气体一下子就将小木炭顶了起来。木炭跳起之后,和下面的硝酸钾液体脱离接触,反应中断了,二氧化炭气体就不再发生,当小木炭由于受到重力的作用落回到硝酸钾上面时,又发生反应,小木炭第二次跳起来。这样的循环往复,小木炭就不停地上下跳跃起来。 2、白糖变“黑雪” 白糖,是大家经常食用的一种物质,它是白色的小颗粒或粉未状,象冬天的白雪。然而,我却能将它立刻变成“黑雪”。如果你不信,那就请看下面的实验吧。在一个200毫升的烧杯中投入5克左右的白糖,再滴入几滴经过加热的浓硫酸,顿时白糖就变成一堆蓬松的“黑雪”,在嗤嗤地发热冒气声中,“黑雪”的体积逐渐增大,甚至满出烧杯。白糖顿时变成了
‘黑雪”,真有意思,谁知道这里的奥妙在什么地方? 答案 原来白糖和浓硫酸发生了一种叫做“脱水”的化学反应。浓硫酸有个特别古怪的爱好,就是它与水结合的欲望特别强烈,它充分利用空气中的水分,就是其他物质中的水分它也不放过,只要一相遇,它就非得把水夺过来不可。白糖是一种碳水化合物(C12H22O11),当它遇到浓硫酸时,白糖分子中的水,立刻被其夺走,可怜的白糖就剩下炭了,变成了黑色。浓硫酸夺过水为己有之后,并不满足,它又施展另外一个本领一氧化,它又把白糖中剩下来的炭的一部分氧化了,生成了二氧化碳气体跑出来。 C+2H2SO4=2H2O+2SO2+CO2 由于反应后所生成的二氧化碳和二氧化硫气体的跑出,所以体积越来越大,最后变成蓬松的“黑雪”。在浓硫酸夺水的“战斗”中,是个放热过程,所以发出嗤嗤的响声,并为浓硫酸继续氧化碳的过程提供热
化学反应原理期末考试试题
试卷类型:A 化学反应原理期末试题 2014.1 考生注意: 本试卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,共8页,满分100分,考试时间90分钟。 注意事项: 1.答卷前,考生将自己的姓名、准考证号、考试科目、试卷类型用2B铅笔涂写在答题卡上。 2.每小题选出答案后,用2B铅笔在答题卡上将对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,不能答在试卷上。 3.考试结束,监考人员将答题卡收回。 可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na: 23 Fe:56 Cu:64 第I卷(选择题共48分) 选择题(本题包括6小题,每小题2分,共12分。每小题只有一个选项符合题意) 1.高中化学《化学反应原理》选修模块从不同的视角对化学反应进行了探究、分析。以下观点中正确的是( ) A.放热反应在常温下均能自发进行 B.电解过程中,化学能转化为电能而“储存”起来 C.化学平衡常数的表达式与化学反应方程式的书写有关 D.强电解质溶液的导电能力一定强于弱电解质溶液 2.250℃和101 kPa时,反应2N2O5(g)= 4NO2(g)+ O2(g) ΔH = +56.76 kJ·mol-1,能自发进行的原因是( ) A.是吸热反应B.是放热反应 C.是熵减少的反应D.是熵增加的反应 3.下列说法正确的是( ) A.金属腐蚀的实质是金属被氧化 B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀 C.为保护地下铁管不受腐蚀,将其与直流电源正极相连 D.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 4.用惰性电极电解饱和 ..Na2SO4溶液,若保持温度不变,则一段时间后( ) A.溶液pH变大
2016年昆明理工大学831化学反应工程考研真题硕士研究生专业课考试试题
昆明理工大学2016年硕士研究生招生入学考试试题(A卷) 考试科目代码:831 考试科目名称:化学反应工程 考生答题须知 1.所有题目(包括填空、选择、图表等类型题目)答题答案必须做在考点发给的答题纸上,做在本试题册上无效。 请考生务必在答题纸上写清题号。 2.评卷时不评阅本试题册,答题如有做在本试题册上而影响成绩的,后果由考生自己负责。 3.答题时一律使用蓝、黑色墨水笔或圆珠笔作答(画图可用铅笔),用其它笔答题不给分。 4.答题时不准使用涂改液等具有明显标记的涂改用品。 一、判断题(正确的请打√,错的打×,全打一种符号的不得分,每题1.5分,共15分) 1.1 化学反应工程主要研究单体反应器的优化问题。 1.2 绝热反应属于变温反应。 1.3 当温度一定时,主副反应级数相等的平行反应,浓度增加,反应的瞬时选择性增加。 1.4 化学反应速率是瞬时反应速率。 1.5 流体粒子在系统进口处有进有出,在出口处有出无进的系统称为闭式系统。 1.6 返混存在总是对化学反应带来不利的影响。 1.7 间歇反应器设计的关键在于计算所需的反应时间。 1.8 当循环管式反应器的循环比β→∞时,浓度c A1(进口浓度)=c A0(进料浓度)。 1.9 真实吸附的活化能与覆盖率呈线性减少的关系。 1.10 对反应级数n>0的反应,n越高,Da越高,外扩散效率因子越小,外扩散影响越大。 二、填空题(每空1分,共15分) 2.1 化学反应按选择性可分为()和()。N2+3H22NH3按相数及类别分为()反应。 2.2 写出n级反应以反应率X A表示的速率方程式()。 对可逆放热反应,温度一定,反应率增加,速率();反应率一定,温度增加,速率()。 2.3 停留时间分布的实验测定方法有()、()和()。 2.4 等温反应、绝热吸热反应、绝热放热反应的绝热温升分别为()、()、()。 2.5 催化剂颗粒的密度有()、()和()三种。 三、简答题(每题12分,共48分) 3.1 写出阿累尼乌斯公式,说明反应速率常数k的单位与哪些因素有关以及速率常数k的计算方法。 3.2 在实际反应器里存在哪些非理想流动现象?并说出它们的E(θ)曲线具有什么特征? 3.3 绘制半间歇槽式反应器反应物和产物的浓度分布图,并分析图形形成的原因。 3.4 为什么要消除外扩散影响?如何通过实验判断外扩散已消除? 第 1 页共3页
(完整版)化学反应工程习题
化学反应工程习题 第一部分:均相反应器基本理论 1、试分别写出N 2+3H 2=2NH 3中用N 2、H 2、NH 3的浓度对时间的变化率来表示的该反应的速率;并写出这三种反应速率表达式之间的关系。 2、已知某化学计量式为 S R B A 2 121+=+的反应,其反应速率表达式为B A A C C r 5 .02=,试求反应速率B r =?;若反应的化学计量式写成S R B A +=+22,则此时反应速率A r =?为什么? 3、某气相反应在400 o K 时的反应速率方程式为2 21061.3A A P d dP -?=- τ h kPa /,问反应速率常数的单位是什么?若将反应速率方程改写为2 1A A A kC d dn V r =?-=τ h l mol ./,该反应速率常数k 的数值、单位如何? 4、在973 o K 和294.3×103Pa 恒压下发生下列反应:C 4H 10→2C 2H 4+H 2 。反应开始时,系统中含丁烷为116kg ,当反应完成50%时,丁烷分压以235.4×103Pa /s 的速率发生变化, 试求下列项次的变化速率:(1)乙烯分压;(2)H 2的摩尔数;(3)丁烷的摩尔分率。 5、某溶液反应:A+B →C ,开始时A 与B 摩尔数相等,没有C ,1小时后A 的转化率为75%,当在下列三种情况下,2小时后反应物A 尚有百分之几未反应掉? (1)对A 为一级、B 为零级反应; (2)对A 、B 皆为一级反应; (3)对A 、B 皆为零级反应。 6、在一间歇反应器中进行下列液相反应: A + B = R A + R = S 已知原料组成为C A0 = 2 kmol/m 3,C B0 = 4 kmol/m 3,C R0 = C S0 = 0。反应混合物体积的变化忽略不计。反应一段时间后测得C A = 0 .3 kmol/m 3,C R = 1.5 kmol/m 3。计算这时B 和S 的浓度,并确定A 的转化率、生成R 的选择性和收率。 7、一级可逆反应A = R 在等温下进行。已知C A0 = 500mol/m 3,C R0 = 0。若该反应在一间歇反应器中进行,且在反应温度下667.0=Ae x 。经480 s 后测得333.0=A x 。(1)试确定此反应的动力学方程;(2)计算A x 分别达到0.6和0.65所需的反应时间;(3)比较计算结果,你有什么体会?
选修四_化学反应原理综合测试题(含答案)
化学反应原理期末测试题二 一、选择题(共16小题,每题3分,共48分,每题有一个选项符合题意) 1.下列物质间的反应,其能量变化符合下图的是( ) A .铁与硫粉在加热条件下的反应 B .灼热的碳与二氧化碳反应 C .Ba(OH)2·8H 2O 晶体和NH 4Cl 晶体混合 D .碳酸钙的分解 2.已知:HCN(aq)与NaOH(aq)反应的ΔH =-12.1 kJ·mol -1; ΔH =-55.6 kJ·mol -1。则HCN 在水溶液中电离的ΔH 等于( ) A .-67.7 kJ·mo l -1 B .-43.5 kJ·mol -1 C .+43.5 kJ·mol -1 D .+67.7 kJ·mol -1 3.在同温同压下,下列各组热化学方程式中△H 1>△H 2的是 ( ) A. 2H 2(g)+O 2(g)=2H 2O(l);△H 1;2H 2(g)+O 2(g)=2H 2O(g);△H 2 B.S(g)+O 2(g)=SO 2(g);△H 1; S(s)+O 2(g)=SO 2(g);△H 2 C.C(s)+1/2O 2(g)=CO(g);△H 1; C(s)+O 2(g)=CO 2(g);△H 2 D.H 2(g)+Cl 2(g)=2HCl(g);△H 1; 1/2H 2(g)+1/2Cl 2(g)=HCl(g);△H 2。 4.某同学为了使反应2HCl+2Ag====2AgCl+H 2↑能进行,设计了如图所示的四个实验,你认为可行的方案是 ( ) 5.模拟铁的电化学防护的实验装置如右图所示,下列说法不正确...的是( ) A .若X 为碳棒,开关K 置于A 处可减缓铁的腐蚀 B .若X 为锌棒,开关K 置于A 或B 处均可减缓铁的腐蚀 C .若X 为锌棒,开关K 置于B 处时,铁电极上发生的反应为2H ++2e -=H 2↑ D .若X 为碳棒,开关K 置于A 处时,铁电极上发生的反应为2H ++2e -=H 2↑ 6.(2013届河北省邯郸一中第一学期中)如下图所示,各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为( ) A .②①③④⑤⑥ B .⑤④②①③⑥ C.⑤④③①②⑥ D .⑤③②④①⑥ 7.(2013届山东枣庄期中考试)将4 mol A 气体和2mol B 气体在2L 的容器中混合并在一定条件下发生反应:2 A (g ) +B (g ) 2 C (g ),经2s 后测得C 的浓度为0.6 mo l·L -1,下列几种说法中正确的是( ) A .用物质A 表示反应的平均速率为0.3 mol·L -1·s -1
化学反应工程基本概念
第一章 1. 化学反应工程是一门研究 (化学反应个工程问题)的科学。 2. 所谓数学模型是指 (用数学方法表达各变量间的关系)。 3. 化学反应器的数学模型包括 (动力学方程式、 物料横算式子、 热量衡算式、 动量衡算式 和 参数计算式) 4. 所谓控制体积是指 (能把反应速率视作定值的最大空间范围)。 5. 模型参数随空间而变化的数学模型称为 ( 分布参数模型)。 6. 模型参数随时间而变化的数学模型称为 (非定态模型)。 7. 建立物料、热量和动量衡算方程的一般式为 (累积量=输入量-输出量)。 第二章 1. 均相反应是指 (在均一的液相或气相中进行的反应)。 2. 对于反应aA + bB → pP + sS ,则r P =( p/a )r A 。 3.着眼反应物A 的转化率的定义式为(转化率Xa=转化了的物料A 的量/反应开始的物料A 的量)。 4. 产物P 的收率ΦP 与得率ХP 和转化率x A 间的关系为( Xp/Xa )。 5. 化学反应速率式为r A =k C C A αC B β,用浓度表示的速率常数为k C ,假定符合理想气体状态方 程,如用压力表示的速率常数k P ,则k C =[ (RT)的a+B 次方]k P 。 6.对反应aA + bB → pP + sS 的膨胀因子的定义式为 (P+S )-(A+B))/A 。 7.膨胀率的物理意义为 (反应物A 全部转化后系统的体积变化率)。 8. 活化能的大小直接反映了 (反应速率) 对温度变化的敏感程度。 9. 反应级数的大小直接反映了(反应速率) 对浓度变化的敏感程度。 10.对复合反应,生成主产物的反应称为 (主反应),其它的均为(副反应)。 11. 平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,选择性S p 与 (A 的浓度) 无关,仅是 (A 的浓度) 的函数。 12. 如果平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,提高选择性S P 应(提到 温度)。 13. 一级连串反应A → P → S 在平推流反应器中,为提高目的产物P 的收率,应(降 低)k 2/k 1。 14. 产物P 的收率的定义式为 (生成的全部P 的物质的量/反应掉的全部A 的物质的量) 15. 产物P 的瞬时收率φP 的定义式为(生成的物质的量/反应的A 的物质的量) 16. 产物P 的选择性S P 的定义式为(单位时间内产物P 的物质的量/单位时间内生成产物S 的物质的量) 17. 由A 和B 进行均相二级不可逆反应αA A+αB B = αS S ,速率方程为: r A =-dC A /dt=kC A C b 。 求: (1)当C A0/C B0=αA /αB 时的积分式 (2)当C A0/C B0=λ≠αA /αB 时的积分式 18. 反应A → B 为n 级不可逆反应。已知在300K 时要使A 的转化率达到20%需12.6min ,而在340K 时达到同样的转化率仅需3.20min ,求该反应的活化能E 。 第三章 1. 理想反应器是指(理想混合反应器 平推流反应器)。 2. 全混流反应器的空时τ是 (反应器容积) 与(进料的体积流量)之比。 3. 全混流反应器的放热速率Q G ={ 00()A A Hr Ft y x ? }。 4. 全混流反应器的移热速率Q r ={ 012()pm Ft C T T - } 5. 全混流反应器的定常态操作点的判据为{ G r Q Q = }。 6. 全混流反应器处于热稳定的定常态操作点的判据为{ G r Q Q = G r dQ dQ dT dT > }。
化学反应原理期末试题含答案复习课程
化学反应原理期末试 题含答案
化学反应原理期末试题含答案 1.下列有关说法正确的是() A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 B.NH3(g)+HCl(g))=NH4Cl(s)室温下能自发进行,说明该反应的ΔH<0 C.N2(g)+3H2(g) 2NH3(g)ΔH<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 D.水的离子积常数K w随着温度的升高而增大,说明水的电离是放热反应2.下列说法正确的是 A.将纯水加热至较高温度,K w变大、pH变小、呈酸性 B.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 C.向0.1 mol·L-1醋酸溶液中加入少量冰醋酸,溶液的pH减小,醋酸电离程度变大 D.等体积、pH都为3的酸HA和HB分别与足量的Zn反应,HA放出的 H2多, 说明HA的酸性小于HB 3. 分析下列硫燃烧时的能量变化图,判断有关热 化学方程式和说法正确的是( ) A.S(s,单斜)+O2(g)===SO2(g) ΔH=+297.16 kJ·mol-1 B.S(s,正交)===S(s,单斜) ΔH=-0.33 kJ·mol-1 C.S(s,正交)+O2(g)===SO2(g) ΔH=-296.83 kJ·mol-1 D.单斜硫的稳定性大于正交硫的稳定性 4. 在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断中正确的是( ) A.10 min时,改变的外界条件可能是减小压强 B.0~5 min内,v(H2)=0.1 mol·(L·min)-1 C.恒温下,缩小容器体积,平衡后c(H2)减小 D.12 min时,反应达平衡时,气体的平均摩尔质量不
化学反应工程
《化学反应工程》课程综合复习资料 一、填空题 1、全混流反应器的E 函数表达式为 ,其无因次方差2θσ= ,而平推流反应器的无因次方差 2θσ= 。 2、工业催化剂性能优劣的三种最主要的性质是 、 、和 。 3、在间歇反应器中进行一恒压气相反应32A B R +→,原料为A 和B 的混合物,其中A 含量为20%(mol),若物料初始体积为2升,则A 转化50%时,物料的总体积为 。 4、基元反应的分子数 (可能/不可能)是小数。 5、某液相反应A R →于50℃下在间歇反应器中进行,反应物A 转化80%需要10min ,如果于相同条件下在平推流反应器中进行,则达到同样的转化率需要的空时为 ;如果同样条件下在全混流反应器中进行,达到同样的转化率需要的空时 。 6、测定非理想流动的停留时间分布函数时,两种最常见的示踪物输入方法为 和 。 7、完全混合反应器(全混流反应器)内物料的温度和浓度 ,并且 (大于/小于/等于)反应器出口物料的温度和浓度。 8、多级混合模型的唯一模型参数为 ,轴向扩散模型的唯一模型参数为: 。 9、对于单一反应,在相同的处理量和最终转化率条件下,选择反应器时主要考虑 ;而对于复合反应,选择反应器时主要考虑的则是 。 10、对于反应23A B R +→,各物质反应速率之间的关系为:(-r A ):(-r B ):r R = 。 11、某重油催化裂化装置处理量为100吨重油/h ,未转化重油为6吨/h ,汽油产量为42吨/h ,则重油的转化率为_ _,工业上汽油的收率及选择性为_ _和_ _。 12、某反应的计量方程为A R S →+,则其反应速率表达式 。 13、反应级数 (可能/不可能)大于3, (可能/不可能)是0,基元反应的分子数 (可能/不可能)是0。 14、在一个完整的气—固相催化反应的七大步骤中,属于本征动力学范畴的三步为 、 和 。 15、在均相反应动力学中,利用实验数据求取化学反应速率方程式的两种最主要的方法为 和 。 16、对于一个在全混流反应器里进行的放热反应,一般可以出现三个定常态操作点M 1、M 2、M 3,如下图所示,其中M 1和M 3这两点我们称之为 的定常态操作点,M 2则称为 的定常态操作点。实际操作时,我们一般选择M 1、M 2、M 3中 做为操作点。 17、某一级液相反应在间歇式反应器中进行,5min 转化率为50%,则转化率达到80%需时间_____min 。 18、某反应的速率方程式为n A A r kC -= mol/,则反应级数n 为2时,k 的单位为 _。 19、某反应的计量方程为A R S →+,则其反应速率表达式 。
有趣的化学金属元素讲解
趣味元素化学知识(一)金属(主族) 身轻如燕的金属——锂 金属在我们的印象里总是沉甸甸的,比木柴啦,水啦砂石啦,都重得多。 但是,有一种金属却轻得出奇,它就是稀有金属——锂。 纯锂的比重跟干操木材差不多,等于号称轻金属的铝的比重的五分之一,几乎只有同体积水的重量的一半。即使把锂扔到汽油里,它也会像软木塞一样轻轻地浮起来。 锂不仅是自然界最轻的金属,而且也是在普通温度条件下呈固态的一般材料中最轻的一种。 除了体重特别轻之外,锂的另一个特点是非常软,富有延展性,可以打薄成片,可以拉伸成丝,压制加工都很方便。如果有人说,有一种金属可以用小刀切开成片时,你听后也许会不信。但是,确实有一种金属可以用小刀来毫不费力地把它切开,这种金属就是锂。 锂有一副漂亮的能发出耀眼的银白色光辉的外表。它的个性活泼,有很强的化学反应能力,一接触潮湿空气,外表就会黯然失色——锂跟空气中的氧、氮等气体迅速化合,生成一层淡黄色或黑色的薄膜覆盖在表面。 在自然界中,锂还算是含量比较多的一种元素,它占地壳总原子数的万分之二。在盐层、海水、盐湖、矿泉中,含有许多可溶的锂的化合物。 锂的化学性质非常活泼,它特别爱跟各种气体交朋友,比如像氧气、氮气、氢气等,因此它经常能帮冶金师傅的忙。 比如说,经过锂脱气的铸铜或铜线,导电性能大大加强。向铬镍不锈钢中加入极少量的锂钙合金,就可以增加它的硬度、强度和加工性能。 经过锂处理的金属或合金,它们的“体格”都变得非常强壮,不但能耐高温,而且不怕酸碱溶液的腐蚀,所以常被用来加工制造具有特殊要求的精密元件。 锂不但可用在冶金工业中,还可以用在其他部门。例如,在玻璃中加进锂和锂的化合物,可以增强玻璃的强度和韧性。有些含锂的特种玻璃,表面光滑,坚固耐用,不怕腐蚀,受热,膨胀也不太厉害,常常用到化工、电子和光学仪器上。电视机的荧光屏就是一种锂制被璃。 锂在日常的机械工业部门里也有它的踪迹。大家都知道,大大小小,各种各样的机器都要用润滑油来降低摩擦。但一般的润滑油都很“娇气”,热了会蒸发分解,冷了又会冻在一起。怎么办呢?人们用锂的化合物制造了一些特种的润滑材料,它们的能耐很大,在零下五十度的低温里不会冻结,在二百度的高温下不会变成气体。不管在烈日炎炎的赤道,还是在千里冰封的两极地区,它们都能胜任。 糖块能点燃吗? 试试看:划亮一根火柴,把糖块放在火焰上,可以看到糖开始熔化,却并不燃烧。 这是怎么了,题目写错了吗? 让我们再试试看,再划着一根火柴,把糖块放在火焰上,然后再往糖块上撤一些香烟灰,这时糖块就会像纸一样燃烧起来! 为什么往糖块上撤一些烟灰就可以燃烧呢? 原来在烟草中,含有许多锂的化合物,当烟草烧成灰烬后,锂就剩在灰烬中。锂不但化学性质很活泼,还能当催化剂,用来加快一些化学反应,糖块能燃烧就是一个例子。 狼是一种凶猛的野兽,经常以牛、羊等家富为食,使牧人们伤透了心。如果有一天狼能不吃羊,对牧人来说将是一件天大的喜事。
二轮复习——化学反应原理
2016学年化学选考二轮复习之化学反应原理 1.氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一。 ⑴ 传统哈伯法合成氨工艺中相关的反应式为:N 2+3H 2 催化剂高温、高压 2NH 3,⊿H <0。 ①该反应的平衡常数K 的表达式为:K=______。升高温度,K 值______(填“增大”“减小”或“不变”)。 ②不同温度、压强下,合成氨平衡体 系中NH 3的物质的量分数见右表(N 2和H 2 的起始物质的量之比为1∶3)。分析表中数 据,在 (填温度和压强)时 H 2转化率最高,实际工业生产不选用该条 件的主要原因是 。 ③下列关于合成氨说法正确是 。 A .使用催化剂可以提高氮气的转化率 B .寻找常温下的合适催化剂是未来研 究的方向 C .由于ΔH<0、ΔS>0,故合成氨反应一定能自发进行 ⑵ 最近美国Simons 等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。它既有液氢燃料电池的优点,又克服了液氢不易保存的不足。其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气。其电池反应为:4NH 3+3O 2=2N 2+6H 2O 。 你认为电解质溶液应显 (填“酸性”、“中性"、“碱性”),它的正极反应和钢铁的吸氧腐蚀一致,请写出负极电极反应式 。 2. 合成氨原理为:N 2(g)+3H 2(g) 催化剂 高温、高压2NH 3(g),ΔH =-92.4 kJ·mol -1。回答下列问题: ⑴写出平衡常数K 的表达式__________________________, 如 果降低温度,该反应K 值_________,N 2的转化率 ______(填“增 大”、“减小”或“不变”)。 ⑵在500℃、20 MPa 时,将N 2、H 2置于一个容积为2 L 的密闭容 器中发生反应,反应过程中各种物质的物质的量随时间的变化如图 所示,回答下列问题: ①在10~20 min 内,NH 3浓度变化的原因可能是( ) A .使用了催化剂 B .缩小容器体积 C .降低温度 D .增加NH 3物质的量 ②反应进行至25 min 时,曲线发生变化的原因 __________________ ________________,达第二次平衡时,新平衡的平衡常数K 2______K 1 (填“大于”、“小于”或“等于”)。 3. 物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。其中难溶电解质在水中的沉淀溶解平衡,其平衡常数称为溶度积常数或简称溶度积,用K sp 表示。如: BaSO 3(s)Ba 2+(aq)+SO 42-(aq) K sp =c (Ba 2+)·c (SO 42-) Fe(OH)3(s)Fe 3+(aq)+3OH -(aq) K sp =c (Fe 3+)·c 3(OH -) 请根据所学的知识回答: ⑴A 为0.1 mol/L 的(NH 4)2SO 4溶液,在该溶液中各种离子的浓度由大到小顺序为___________________。 ⑵B 为0.1 mol/L NaHCO 3溶液,请分析NaHCO 3溶液显碱性的原因(用离子方程式表示)__________。 ⑶C 为FeCl 3溶液,实验室中配制FeCl 3溶液时常加入________溶液以抑制其水解,若把B 和C 溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为___________________________________。 ⑷D 为含有足量AgCl 固体的饱和溶液,AgCl 在水中存在沉淀溶解平衡: AgCl(s) Ag +(aq)+Cl -(aq),在25℃时,氯化银的K sp =1.8×10-10。现将足量氯化银分别放入: ①100 mL 蒸馏水中;②100 mL 0.2 mol/L AgNO 3溶液中;③100 mL 0.1 mol/L 氯化铝溶液中;④100 mL0.1 mol/L 盐酸中,充分搅拌后,相同温度下c (Ag +)由大到小的顺序是______________________(填写序号); ②中氯离子的浓度为__________mol/L 。 4.现代炼锌的方法可分为火法和湿法两大类。火法炼锌是将闪锌矿(主要含ZnS )通过浮选、焙烧使它转化为氧化锌,再把氧化锌和足量焦炭混合,在鼓风炉中加热至1373~1573K ,使锌蒸馏出来。主要反应为: 焙烧炉中:2ZnS +3O 2=2ZnO +2SO 2 ①
2018年云南昆明理工大学高等化学反应工程考研真题
2018年云南昆明理工大学高等化学反应工程考研真题 一、判断题(10分,每题1分) ( ) 1.1 在恒容的间歇反应器中,A 的消失速率表示为–r A =dC A /dt 。 ( ) 1.2 对反应级数小于0的等温反应,达到相同的转化率时,PFR 的体积小于CSTR 的体积。 ( ) 1.3 反应2SO 2+ O 22SO 3的有限反应物是SO 2。 ( ) 1.4 若反应器距离一定,随膨胀率ε增加,转化率增加。 ( ) 1.5 在恒定体积的间歇反应器内进行一级反应,lnC A0/C A 与时间呈线性关系。 ( ) 1.6 对于连串反应A →B(目的产物)→C, 如果PFR 太长,则很难得到主产物B 。 ( ) 1.7 在带换热器的CSTR 中进行吸热反应,有T>T a2>T a1。 ( ) 1.8 如果停留时间τ增加,生热曲线向下移动。 ( ) 1.9 最大混合模型的离散度J 等于1。 ( ) 1.10 在空管中,Peclet 数的特征长度是管径。 二、填空题(15分,每空1分) 2.1 在系统体积V 内积累的任一化学组分j 的通用摩尔衡算方程为( )。 2.2 写出空间时间的定义式( )。 2.3 根据反应的分子性定义,反应92U 238→90Th 234+2He 4 为( )反应。 2.4 0级反应速率常数的单位为( )。 2.5 B 被缓慢地加入含有A 的反应器中,此类半间歇反应器的实例有( )、( )和( )。 2.6 复合反应的类型有( )、( )、( )和( )。 2.7 进口温度增加,放热反应的绝热平衡转化率( )。 2.8 微观混合的两种极限是( )和( )。 2.9 在密闭体系边界条件下,无因次平均停留时间( )。 三、简答题(32分,每题8分) 3.1 写出CSTR 的设计方程,说明其推导过程作的假设。 3.2 说明微反应器的特点和应用。 3.3 对平行反应:A+B → D 111β αB A D C C k r = A+B → U 222βαB A U C C k r = 当α1<α2 和 β1>β2,说明S D/U 最大时,反应器和条件的选择。
