第二章 - 无答案

第二章第一节
一、选择题
1.(2010·辽宁抚顺一中下学期月考)下列关于化学反应说法中不正确的是()
A.化学反应过程中一定有热量释放出来
B.化学反应的特征是有新物质生成
C.化学反应的过程实际上是一个旧键断裂,新键生成的过程
D.在一确定的化学反应关系中,反应物的总能量与生成物的总能量一定不相等
2.(2010·天津理综)以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济的是()
A.发展氢能和太阳能B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学D.尽量用纯液态有机物代替水作溶剂3.冰岛火山爆发再一次向人类敲响了警钟,必须发展“低碳经济”。氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车备受青睐。下列不是氢能优点的是()
A.原料来源广B.易燃烧,放出热量多
C.产物无污染D.制取H2简单易行
4.(2010·浙江元济中学第二学期月考)下列反应既属于氧化还原反应,又是吸热反应的是()
A.锌粒与稀硫酸的反应B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应5.关于吸热反应和放热反应,下列说法正确的是()
A.需要加热才能进行的化学反应一定是吸热反应
B.放热反应不需要加热即可发生
C.放热反应常温下易发生
D.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小,不能看反应条件
6.石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石。已知12 g石墨完全转化成金刚石时,要吸收1.9 kJ的能量。下列说法正确的是()
A.石墨不如金刚石稳定
B.金刚石不如石墨稳定
C.固体煤变成气体燃料后,燃烧效率变低
D.等质量的石墨与金刚石完全燃烧,石墨放出的能量更多
7.下列叙述正确的是()
①化学反应都遵循质量守恒定律②化学反应都遵循能量守恒定律③化学反应都有新物质生成④化学反应都伴随着能量变化⑤化学反应都有化学键的破坏和生成A.只有①B.只有①②⑤
C.只有①②③⑤D.①②③④⑤
8.下列能源是通过化学反应产生的是()
A.太阳能B.潮汐能
C.风能D.氢气燃烧产生的热能
9.航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物作为固体燃料,点燃时铝粉氧化引发高氯酸铵反应,其化学方程式可表示为:2NH4ClO4===N2↑+4H2O+Cl2↑+2O2↑。下列对此反应的叙述中错误的是()
A.上述反应属于分解反应
B.在反应中高氯酸铵只能起氧化剂作用
C.反应从能量变化上说,主要是化学能转变为热能和动能
D.上述反应瞬间产生大量高温气体推动航天飞机飞行
10.用中和热的测定方法,即保温、隔热的条件下,向盛有20 mL 2.08 mol/L的NaOH 溶液的试管中分五次加入5 mL未知浓度的H2SO4(边加边振荡,每次加1 mL,不考虑H2SO4溶于水的放热效应)后,测得溶液的温度分别是1.4 ℃、2.5 ℃、4.2 ℃、5.2 ℃、5.18 ℃,则
该硫酸的浓度是()
A.20.8 mol/L B.6.9 mol/L
C.5.2 mol/L D.4.16 mol/L
二、非选择题
11.某化学反应,设反应物总能量为E1,生成物总能量为E2,如果把化学反应中能量的变化看成是物质内部的能量与热能之间进行转变,则:
(1)若E1>E2,则该反应为________热反应,该反应的过程可看成是“贮存”在物质内部的能量转化为________能而被释放出来的过程。
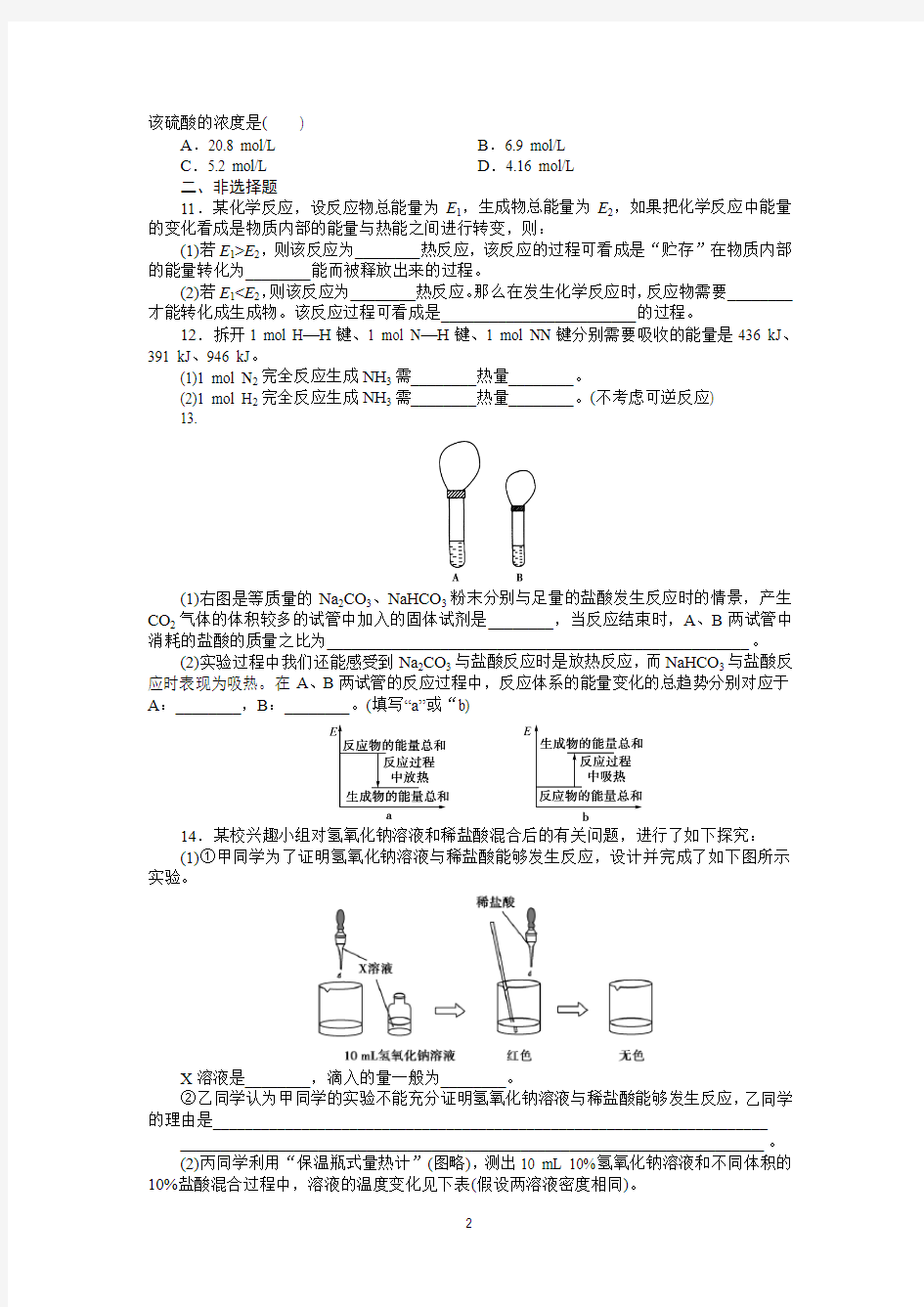
(2)若E1 12.拆开1 mol H—H键、1 mol N—H键、1 mol NN键分别需要吸收的能量是436 kJ、391 kJ、946 kJ。 (1)1 mol N2完全反应生成NH3需________热量________。 (2)1 mol H2完全反应生成NH3需________热量________。(不考虑可逆反应) 13. (1)右图是等质量的Na2CO3、NaHCO3粉末分别与足量的盐酸发生反应时的情景,产生CO2气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B两试管中消耗的盐酸的质量之比为____________________________________________________。 (2)实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管的反应过程中,反应体系的能量变化的总趋势分别对应于A:________,B:________。(填写“a”或“b) 14.某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究: (1)①甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如下图所示实验。 X溶液是________,滴入的量一般为________。 ②乙同学认为甲同学的实验不能充分证明氢氧化钠溶液与稀盐酸能够发生反应,乙同学的理由是_____________________________________________________________________ ________________________________________________________________________。 (2)丙同学利用“保温瓶式量热计”(图略),测出10 mL 10%氢氧化钠溶液和不同体积的10%盐酸混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。 ①盐酸和氢氧化钠的反应是________(填“吸热”或“放热”)反应。 ②请在下图中绘制出溶液的温度上升与加入盐酸体积之间的变化关系图。 第二章第二节 一、选择题 1.下列关于原电池的叙述中正确的是() A.正极和负极必须是两种不同的金属 B.原电池是把化学能转化成电能的装置 C.原电池工作时,正极和负极上发生的都是氧化还原反应 D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢气生成 2.(2009·广东理基)下列有关电池的说法不正确的是() A.手机上用的锂离子电池属于二次电池 B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 C.甲醇燃料电池可把化学能转化为电能 D.锌锰干电池中,锌电极是负极 3.如图为某兴趣小组制作的番茄电池,下列说法正确的是() A.电子由锌通过导线流向铜B.该装置将电能转化为化学能 C.锌电极发生还原反应D.铜电极上无气泡产生 4.下列四个化学反应中,你认为理论上不可用于设计原电池的是() A.2Al+2NaOH+2H2O===2NaAlO2+3H2↑B.2H2+O2===2H2O C.Mg3N2+6H2O===3Mg(OH)2+3NH3↑D.CH4+2O2―→CO2+2H2O 5.原电池的总反应的离子方程式是Zn+Cu2+===Zn2++Cu,该反应的原电池组成正确的是() 6 A.轮船水线以下的船壳上镶嵌有一定量的锌块 B.镀锌的铁制品比镀锡的铁制品耐用 C.铝片不用特殊方法保存 D.锌跟稀硫酸反应时,滴入少量硫酸铜溶液后,反应速率加快 7.(2010·浙江元济中学第二学期月考)如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是() A.a为负极,是铁片,烧杯中的溶液为稀硫酸 B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 C.a为正极,是碳棒,烧杯中的溶液为稀硫酸 D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液 8.能源可划分为一级能源和二级能源,自然界中以现成形式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源。氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(l)===2H2(g)+O2(g)(吸收能量),下列叙述正确的是(双选)() A.电能是二级能源B.水力是二级能源 C.天然气是一级能源D.焦炉气是一级能源 9.燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如下图所示,a、b均为惰性电极。下列叙述不正确的是() A.a极是负极,该电极上发生氧化反应B.b极反应是O2+4OH--4e-===2H2O C.总反应方程式为2H2+O2===2H2O D.氢氧燃料电池是一种具有应用前景的绿色电源 10. 芬兰Enfucell公司制造出一种纸质电池(如图所示),避免了传统电池所带来的金属及碱性化合物的泄漏问题,因而可作为一般的家庭废物加以处理。这种被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰,在纸内的带电离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn+2MnO2+H2O===2MnO(OH)+ZnO。下列说法正确的是() A.该电池的正极为锌 B.该电池反应中二氧化锰起催化剂作用 C.当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 D.电池正极反应式为:2MnO2+2e-+2H2O===2MnO(OH)+2OH- 二、非选择题 11.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如下图所示: (1)A中反应的离子方程式为________________。 (2)B中Sn极的电极反应式为________,Sn极附近溶液的pH________(填“升高”、“降低”或“不变”)。 (3)C中被腐蚀的金属是________,总反应式为______________________________。 (4)比较A、B、C中铁腐蚀的速率,由快到慢的顺序是 ______________________________________________________________________。 12.如下图所示,组成一种原电池,试回答下列问题(灯泡功率合适): (1)电解质溶液为稀H2SO4时,灯泡________(填“亮”或“不亮”)。若灯泡亮,则Mg 电极上发生的反应为______________________;Al电极上发生的反应为____________________(正、负电极的电极反应式要保持得失电子相等)。 (2)电解质溶液为NaOH(aq)时,灯泡________(填“亮”或“不亮”)。若灯泡亮,则Mg 电极上发生的反应为________________________;Al电极上发生的反应为________________________(正、负电极的电极反应式要保持得失电子相等)。 13.Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为: 4Li+2SOCl2===4LiCl+S+SO2。 请回答下列问题: (1)电池的负极材料为____,发生的电极反应为________________________________; (2)电池正极发生的电极反应为___________________; (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是 ________________________________________________________________________; 反应的化学方程式为 ________________________________________________________________________; (4)组装该电池必须在无水、无氧的条件下进行,原因是 ________________________________________________________________________。 14. 上海世博会期间,在德国馆的汉堡之家展馆人们看到一个1∶20飞机燃料电池的模型。燃料电池是一种通过氢氧结合来发电的电化学装置。某氢氧燃料电池的电池反应为2H2+O2===2H2O,电解液为KOH溶液。氢氧燃料电池的突出优点是把________能直接转化为________能,而不用经过________能这一中间形式。 (1)有关氢氧燃料电池的下列叙述中,正确的是() A.此电池能发出蓝色火焰 B.氢气为正极,氧气为负极 C.因为生成水,所以工作时溶液的碱性越来越强 D.负极上氢气失电子,发生氧化反应;正极上氧气得电子,发生还原反应 (2)该电池所产生的水可以作为饮用水,今欲制得常温下1 L水,则电池内转移电子的物质的量为________。 A.8.9×10-3 mol B.4.5×10-2 mol C.1.1×102 mol D.5.6×103 mol 第二章第三节(一) 一、选择题 1.(2011·盛同高一检测)下列说法不正确的是() A.参加反应物质的性质是决定化学反应速率的主要因素 B.光是影响某些化学反应速率的外界条件之一 C.对于一个化学反应,既可以用反应物表示其化学反应速率,也可以用生成物表示其化学反应速率 D.不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率2.加热氯酸钾制氧气时,在①锰、②二氧化锰、③高锰酸钾中,可以作催化剂的是() A.①②B.①②③ C.②D.②③ 3.四个不同容器在不同条件下进行合成氨反应,根据下列在相同时间内测定的结果判断,生成氨的速率最快的是() A.用H2表示的反应速率为0.1 mol·L-1·min-1 B.用N2表示的反应速率为0.04 mol·L-1·s-1 C.用N2表示的反应速率为0.2 mol·L-1·s-1 D.用NH3表示的反应速率为0.3 mol·L-1·s-1 4.下列措施肯定能使反应速率增大的是() A.增大反应物的量B.增大压强 C.适当升高温度D.降低反应物浓度 5.反应2SO2+O2 2SO3经过一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为() A.0.1 s B.2.5 s C.5 s D.10 s 6.100.0 mL 6.0 mol·L-1H2SO4溶液跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量的() A.Na2CO3(s) B.水 C.CuSO4(aq) D.NaHSO4(s) 7.把下列四种X溶液分别加入四个盛有10 mL 2 mol/L盐酸的烧杯中,均加水稀释到50 mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是() A.10 ℃ 20 mL 3 mol/L的X溶液B.20 ℃ 30 mL 2 mol/L的X溶液 C.20 ℃ 10 mL 4 mol/L的X溶液D.10 ℃ 10 mL 2 mol/L的X溶液8.把镁条投入到盛有盐酸的敞口容器里,产生H2的速率与时间的关系如下图所示,在下列因素中,影响反应速率的因素是() ①盐酸的浓度②镁条的表面积③溶液的温度④Cl-的浓度 A.①④B.③④ C.①②③D.②③ 9.为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是() A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 B.若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 C.用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间 D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 10.(2010·福建高考)化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min时间内的平均反应速率和推测反应16 min 时反应物的浓度,结果应是() A.2.5 mol·L-1·min-1和2.0 mol·L-1 B.2.5 mol·L-1·min-1和2.5 mol·L-1 C.3.0 mol·L-1·min-1和3.0 mol·L-1 D.5.0 mol·L-1·min-1和3.0 mol·L-1 二、非选择题 11.在密闭容器中发生下列反应:I2(g)+H2(g) 2HI(g)(正反应为吸热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的 第二章 第三节(二) 一、选择题 1.中国锅炉燃烧采用沸腾炉的逐渐增多,采用沸腾炉的好处在于( ) ①增大煤炭燃烧时的燃烧热并形成清洁能源 ②减少炉中杂质气体(如SO 2等)的形成 ③提高煤炭的热效率并减少CO 的排放 ④使燃料燃烧充分,从而提高燃料的利用率 A .①② B .③④ C .①③ D .②④ 2.(2009·广东理基)已知汽车尾气无害化处理反应为2NO(g)+2CO(g)N 2(g)+2CO 2(g),下列说法不正确的是( ) A .升高温度可使该反应的逆反应速率降低 B .使用高效催化剂可有效提高正反应速率 C .反应达到平衡后,NO 的反应速率保持恒定 D .单位时间内消耗CO 和CO 2的物质的量相等时,反应达到平衡 3.某温度下,在一固定容积的密闭容器中进行如下反应:H 2(g)+I 2(g) △2HI(g),下 列情况一定能说明反应已达到限度的是( ) A .压强不再随时间而改变时 B .气体的总质量不再改变时 C .混合气体中各组成成分的含量不再改变时 D .单位时间内每消耗1 mol I 2,同时有2 mol HI 生成时 4.在373 K 时,密闭容器中充入一定量的NO 2和SO 2,发生如下反应:NO 2+SO 2 催化剂 NO +SO 3,平衡时,下列叙述正确的是( ) ①NO 和SO 3的物质的量一定相等 ②NO 2和SO 2的物质的量一定相等 ③体系中的总物质的量一定等于反应开始时总物质的量 ④SO 2、NO 2、NO 、SO 3的物质的量一定相等 A .①和② B .②和③ C .①和③ D .③和④ 5.(2010·浙江元济中学月考)一定温度下,反应N 2(g)+3H 2(g)2NH 3(g)达到化学平衡状态的标志是( ) A .N 2,H 2和NH 3的质量分数不再改变 B .c (N 2)∶c (H 2)∶c (NH 3)=1∶3∶2 C .N 2与H 2的物质的量之和是NH 3的物质的量的2倍 D .单位时间里每生成1 mol N 2,同时消耗2 mol NH 3 6.下列措施,能使煤炭燃烧更充分,提高热能利用率的是( ) A .多加煤以使炉火更旺 B .把煤炭做成大煤球 C .把煤中掺和一些黄泥做成蜂窝煤 D .把煤粉碎,在煤粉燃烧器中燃烧 7.在一定条件下,将1 mol 的CO 和水蒸气通入容器中发生下述反应:CO +H 2O CO 2+H 2,达到平衡后,测得CO 2为0.6 mol ,再通入4 mol 水蒸气,又达到平衡后,CO 2的物质的量为( ) A .等于0.6 mol B .等于1 mol C .大于0.6 mol 小于1 mol D .大于1 mol 8.在密闭容器中充入4 mol X ,在一定温度下4X(g)3Y(g)+Z(g)达到平衡时,有30%的X 发生分解,则平衡时混合气体总的物质的量是( ) A .3.4 mol B .4 mol C .2.8 mol D .1.2 mol 9.在一密闭容器中进行反应:2SO 2(g)+O 2(g) 催化剂△ 2SO 3(g),已知反应过程中某一时刻SO 2、O 2和SO 3的浓度分别为0.2 mol/L 、0.1 mol/L 、0.2 mol/L 。当反应达平衡时,可能存在的数据是( ) A .SO 2为0.4 mol/L 、O 2为0.2 mol/L B .SO 2为0.25 mol/L C .SO 2为0.4 mol/L D .SO 2、SO 3均为0.15 mol/L 10.已知常温常压下,N 2(g)和H 2(g)生成2 mol NH 3(g)放出92.4 kJ 热量。在同温同压下向密闭容器中通入1 mol N 2和3 mol H 2,达到平衡时放出热量为Q 1 kJ ,向另一体积相同的密闭容器中通入0.5 mol N 2、1.5 mol H 2和1 mol NH 3,相同条件下达到平衡时放出热量为Q 2 kJ ,则下列关系式正确的是( ) A .2Q 2=Q 1=92.4 B .Q 2 C .Q 1 D .Q 1=Q 2<92.4 二、非选择题 11.在200 ℃时,将a mol H 2(g)和b mol I 2(g)充入到体积为V L 的密闭容器中,发生反应:I 2(g)+H 2(g)2HI(g)。 (1)反应刚开始时,由于c (H 2)=________,c (I 2)=________,而c (HI)=________,所以化学反应速率________最大,而________最小(为零)。 (2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c (H 2)________,c (I 2)________,而c (HI)______,从而化学反应速率v (正)______,而v (逆)________。 (3)当反应进行到v (正)与v (逆)________时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将________。 12.铁是工业生产的重要物资,也是地壳中的有限资源,自然界中铁矿石主要有赤铁矿(Fe 2O 3)和磁铁矿(Fe 3O 4)等,金属铁是在高炉中冶炼的,高炉炼铁除了加入铁矿石外,还需加入焦炭和生成炉渣的石灰石。 (1)请写出下列高炉炼铁中发生反应的化学方程式: ①磁铁矿被焦炭还原成铁: ________________________________________________________________________; ②部分焦炭在高炉中生成CO : ______________________________________________________________________; ③赤铁矿被CO 还原成铁: _______________________________________________________________________; (2)炼铁高炉的高度增加后,铁矿石与CO 接触更充分了,但高炉尾气的CO 比例并没有减少,原因是: _______________________________________________________________________。 13.作为国家正在实施的“西气东输”工程终点站,上海将逐步改变以煤、石油为主的能源结构,这对解决城市环境污染意义重大。 目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为燃料。管道煤气的主要成分是CO 、H 2和少量烃类,天然气的主要成分是CH 4。它们的燃烧反应如下: 2CO +O 2=====点燃2CO 2 2H 2+O 2=====点燃 2H 2O CH 4+2O 2――→点燃CO 2+2H 2O 根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________。 因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是________(填“增大”或“减小”)进风口,如不作改进可能产生的不良结果是________________。管道煤气中含有 并且呈断续状态的原因是_________________________________________________________________。 14.(1)氢气是合成氨的重要原料,合成氨反应的化学方程式如下:N 2(g)+3H 2(g)2NH 3(g) 该反应为放热反应且每生成2 mol NH 3,放出92.4 kJ 的热量。 当合成氨反应达到平衡后,改变某一外界条件(不改变N 2、H 2和NH 3的量),反应速率与时间的关系如图所示。图中表示反应处于化学平衡状态的时间段(t 1时刻后)为________。 (2)在一定温度下,向一个容积为1 L 的容器中通入2 mol 氮气和8 mol 氢气及固体催化 剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。 ①N 2的转化率为________。 ②反应达到平衡时,放出热量为________(填序号)。 A .小于92.4 kJ B .等于92.4 kJ C .大于92.4 kJ D .可能大于或小于或等于92.4 kJ (3)下列能证明反应已达化学平衡的标志为________。 A .压强不变 B .体系的温度不变 C .N 2、H 2、NH 3的分子数之比为1∶3∶2 D .v (N 2)正=13 (H 2)正 12.(2011·临沂高一检测)某温度时,在2 L 容器中X 、Y 、Z 三种物质随时间的变化曲线如图所示: 由图中的数据分析,该反应的化学方程式为_____________________________________。 反应开始至2 min 时Z 的平均反应速率为____________。 13.某研究性学习小组探究如下实验:在常温下,取两片质量相等,外形和组成相同且 表面经过砂纸打磨完全去掉氧化膜的铝片,分别加入到盛有相同体积、H +浓度相同的稀硫 酸和稀盐酸的两支大小相同的试管中,发现铝片在稀盐酸中产生氢气的速率比在稀硫酸中快。查阅相关资料后得知:化学反应速率主要由参加反应的物质的性质决定,其次是外界因素的影响。影响化学反应速率的因素主要有:①温度,其他条件不变时,升温反应加快;②浓度,其他条件不变时,浓度越大反应越快。另外,固体与液体反应,接触面越大,反应越快。 (1)写出以上反应的离子方程式: ________________________________________________________________________。 (2)出现上述现象的可能原因是:假设①SO 2-4对铝与H +的反应有抑制作用;假设 ②________________________________________________________________________。 (3)请设计实验对上述假设进行验证: ①________________________________________________________________________ ________________________________________________________________________; ②________________________________________________________________________ ________________________________________________________________________。 (4)如果上述假设都成立,要使上述稀硫酸与铝反应产生氢气的速率加快,可以采取的措施有:①____________________;②______________;③________;④____________________。 14.在25 ℃时,向100 mL 含14.6 g 氯化氢的盐酸溶液里放入5.6 g 纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min 末收集到氢气1.12 L(标准状况),在此之后,又经过4 min ,铁粉完全溶解。则: (1)在前2 min 内用FeCl 2表示的平均反应速率是多少? (2)在后4 min 内用HCl 表示的平均反应速率是多少? (3)前2 min 与后4 min 相比,反应速率哪个较快,为什么? 第二章 一、选择题(本题包括15小题,每题3分,共45分) 1.节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务。下列举措不符合这一要求的是() A.倡导开私家车的人乘公交车上下班 B.国家减免小排量轿车的购置税 C.政府鼓励科研和生产部门开发、利用太阳能 D.加快开发石油以缓解能源紧张问题 2.下列对化学反应的认识正确的是() A.氧化还原反应都是放热反应 B.化学反应过程中一定有化学键的断裂和形成 C.伴随能量变化的物质变化都是化学变化 D.化学反应过程中,分子的种类和数目一定发生改变 3.(2011·潮州高一检测)一种化学冰袋中含有Na2SO4·10H2O(96 g)、NH4NO3(50 g)、(NH4)2SO4(40 g)、NaHSO4(40 g)。将Na2SO4·10H2O和其他三种盐分别盛于两只塑料袋中,使用时把它们混合并用手揉搓就可制冷,制冷效果能维持2~3 h。以下关于制冷原因的猜测肯定错误的是() A.Na2SO4·10H2O脱水是吸热过程 B.较长时间制冷是由于Na2SO4·10H2O脱水过程较慢 C.铵盐发生了复分解反应,且为吸热反应 D.NH4NO3溶于水会吸收热量 4.(2010·南京高一检测)下列属于吸热反应的是() A.金属钠与水的反应B.氢气燃烧 C.浓硫酸的稀释D.Ba(OH)2·8H2O和NH4Cl(固体)混合 5.关于原电池的叙述,正确的是() A.任何化学反应,均可以设计成原电池 B.原电池是把化学能直接转化成电能的装置 C.原电池的两极必须都是金属 D.原电池可以提供持续稳定的电流,应用十分广泛 6.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是() A.利用电池外壳的金属材料 B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 C.防止电池中渗漏的电解质溶液腐蚀其他物品 D.回收其中的石墨电极 7.硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志。目前的重要生产方法是“接触法”,有关接触氧化反应 2SO3 2SO 2+O2催化剂 500 ℃ 的说法不正确的是() A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 D .在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 8.(2009·山东理综)2SO 2(g)+O 2(g)V 2O 5 △2SO 3(g)是制备硫酸的重要反应。下列叙述中, 正确的是( ) A .催化剂V 2O 5不改变该反应的逆反应速率 B .增大反应体系的压强,反应速率一定增大 C .该反应是放热反应,降低温度将缩短反应达到平衡的时间 D .在t 1、t 2时刻,SO 3(g)的浓度分别是c 1、c 2,则时间间隔t 1~t 2内,SO 3(g)生成的平 均速率为v =c 2-c 1 t 2-t 1 9.在一定温度下的恒容密闭容器中,能说明反应X 2(g)+Y 2(g) 2XY(g)已达到平衡的是( ) A .容器内的总压不随时间变化 B .容器中气体的平均相对分子质量不随时间变化 C .XY 气体的物质的量分数不变 D .X 2和Y 2的消耗速率相等 10.参照反应Br +H 2HBr +H 的能量对应反应历程的示意图,下列叙述中正确的是( ) A .正反应为吸热反应 B .吸热反应一定要加热后才能发生 C .反应物总能量高于生成物总能量 D .升高温度可增大正反应速率,降低逆反应速率 11.已知H ++OH -===H 2O 生成1 mol H 2O 放出热量57.3 kJ ,下列反应中能放出57.3 kJ 热量的是( ) A .1 mol 稀H 2SO 4与足量NaOH 溶液反应 B .稀盐酸与氨水反应生成1 mol H 2O C .稀盐酸与稀Ba(OH)2溶液反应生成1 mol 水 D .稀NaOH 与95%浓硫酸反应生成1 mol 水 12. 如图所示的装置中,M 为活动性顺序位于氢之前的金属,N 为石墨棒,关于此装置的 下列叙述中,不正确的是( ) A .N 上有气体放出 B .M 为负极,N 为正极 C .是化学能转变为电能的装置 D .导线中有电流通过,电流方向是由M 到N 13. 如图所示为普通锌锰电池(即干电池)的组成和结构示意图,其中MnO 2的作用是吸收正 极放出的H 2,下列说法正确的是( ) A .锌是正极,MnO 2是负极 B .锌是负极,MnO 2是正极 C .锌是正极,石墨棒是负极 D .锌是负极,石墨棒是正极 14.(2009·山东基能)硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na 2S 2O 3+ 该电池以金属锂和钢板为电极材料,以LiOH 为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( ) A .水既是氧化剂又是溶剂 B .放电时正极上有氢气生成 C .放电时OH -向正极移动 D .总反应为:2Li +2H 2O===2LiOH +H 2↑ 二、非选择题(本题包括5小题,共55分) 16.(11分)氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO 2)表面作用使海水分解得到氢气的新技术: 2H 2O=====激光 TiO 22H 2↑+O 2↑。制得的氢气可用于燃料电池。试回答下列问题: (1)分解海水时,实现了从________能转变为________能,二氧化钛作________。生成的氢气用于燃料电池时,实现________能转变为________能。水分解时,断裂的化学键为________键,分解海水的反应属于________反应(填“放热”或“吸热”)。 (2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为: A 极:2H 2+2O 2--4e -===2H 2O ; B 极:O 2+4e -===2O 2- 则A 极是电池的________极;电子从该极________(填“流入”或“流出”)。 (3)有人以化学反应:2Zn +O 2+4H +===2Zn 2++2H 2O 为基础设计一种原电池,移入人 体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O 2、H +、Zn 2+进行工作。 则原电池的负极材料是________,发生的电极反应为______________________。 17.(10分)(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上________(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来,组成一个原电池,负极为________,正极的电极反应式为____________________。 (2)如果烧杯中最初装入的是500 mL 2 mol·L -1的稀硫酸,构成铜锌原电池(假设产生的 气体没有损失),当在标准状况下收集到11.2 L 的氢气时,则此时烧杯内溶液中溶质的物质的量浓度应为(溶液体积变化忽略不计)__________________________。 18.(10分)(2011·济宁高一检测)化学电池在通讯、交通及日常生活中有着广泛的应用。 (1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为Cd +2NiO(OH)+2H 2O 放电 充电2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是________。 ①放电时NiO(OH)作负极 ②充电时Cd(OH)2发生还原反应 ③充电时化学能转变为电能 ④放电时化学能转变为电能 (2)废弃的镍镉电池已成为严重的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重,这是因为 ______________________________________________。 19.(12分)通常人们把拆开1 mol 某化学键所吸收的能量看成该化学键的键能。键能的 大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH ),化学反应的反应热等于化学键 Si —O Si —Cl H —H H —Cl Si —Si Si —C 键能/ kJ·mol -1 460 360 436 431 176 347 (1)已知Si 、SiC 、SiO 2熔化时必须断裂所含化学键,比较下列两组物质的熔点高低(填“>”或“<”):SiC________Si ,Si________SiO 2 (2)工业上高纯硅可通过下列反应制取: SiCl 4(g)+2H 2(g)=====高温 Si(s)+4HCl(g), 则2 mol H 2生成高纯硅需________(填“吸收”或“放出”)能量________kJ 。 20.(12分)在某一容积为2 L 的密闭容器中,A 、B 、C 、D 四种物质的物质的量n (mol)随时间t (min)的变化曲线如图所示: 回答下列问题: (1)该反应的化学方程式为 ________________________________________________________________________。 (2)前2 min 用A 的浓度变化表示的化学反应速率为________。在2 min 时,图象发生改变的原因是_______________________________________________________________(用字母表示)。 A .增大压强 B .降低温度 C .加入催化剂 D .增加A 的物质的量 第二章 矩阵及其运算 1 已知线性变换 ?????++=++=++=3 213321232113235322y y y x y y y x y y y x 求从变量x 1 x 2 x 3到变量y 1 y 2 y 3的线性变换 解 由已知 ? ??? ?????? ? ?=???? ??221321323513122y y y x x x 故 ???? ?????? ? ?=???? ??-3211 221323513122x x x y y y ? ??? ?????? ??----=321423736 947y y y ?????-+=-+=+--=3 21332123 211423736947x x x y x x x y x x x y 2 已知两个线性变换 ?????++=++-=+=321332123 11542322y y y x y y y x y y x ?????+-=+=+-=3 233122 11323z z y z z y z z y 求从z 1 z 2 z 3到x 1 x 2 x 3的线性变换 解 由已知 ???? ?????? ? ?-=???? ??221321514232102y y y x x x ??? ? ?????? ??--???? ??-=32131 010 2013514232102z z z ??? ? ?????? ??----=321161109412316z z z 所以有?????+--=+-=++-=3 21332123 2111610941236z z z x z z z x z z z x 3 设???? ??--=111111111A ??? ? ??--=150421321B 求3AB 2A 及A T B 解 ??? ? ??---???? ??--???? ??--=-1111111112150421321111111111323A AB ???? ??----=???? ??---???? ??-=2294201722213211111111120926508503 ??? ? ??-=???? ??--???? ??--=092650850150421321111111111B A T 4 计算下列乘积 (1)??? ? ?????? ??-127075321134 解 ???? ?????? ??-127075321134???? ???+?+??+?-+??+?+?=102775132)2(71112374??? ? ??=49635 (2)???? ??123)321( 解 ??? ? ??123)321((132231)(10) 第2章线性表 一选择题 1.下述哪一条是顺序存储结构的优点?( A ) A.存储密度大 B.插入运算方便 C.删除运算方 便 D.可方便地用于各种逻辑结构的存储表示 2.下面关于线性表的叙述中,错误的是哪一个?( B )A.线性表采用顺序存储,必须占用一片连续的存储单元。B.线性表采用顺序存储,便于进行插入和删除操作。 C.线性表采用链接存储,不必占用一片连续的存储单元。D.线性表采用链接存储,便于插入和删除操作。 3.线性表是具有n个( C )的有限序列(n>0)。 A.表元素 B.字符 C.数据元 素 D.数据项 E.信息项 4.若某线性表最常用的操作是存取任一指定序号的元素和在最后进行插入和删除运算,则利用( A )存储方式最节省时间。 AHA12GAGGAGAGGAFFFFAFAF A.顺序表 B.双链表 C.带头结点的双循环链表 D.单循环链表 5.某线性表中最常用的操作是在最后一个元素之后插入一个元素和删除第一个元素,则采用( D )存储方式最节省运算时间。 A.单链表 B.仅有头指针的单循环链 表 C.双链表D.仅有尾指针的单循环链表 6.设一个链表最常用的操作是在末尾插入结点和删除尾结点,则选用( D )最节省时间。 A. 单链表 B.单循环链表 C. 带尾指针的单循环链表 D.带头结点的双循环链表 7.若某表最常用的操作是在最后一个结点之后插入一个结点或删除最后一个结点。则采用( D )存储方式最节省运算时间。 AHA12GAGGAGAGGAFFFFAFAF A.单链表 B.双链表 C.单循环链 表 D.带头结点的双循环链表 8. 静态链表中指针表示的是( BC ). A.内存地址 B.数组下标 C.下一元素地址D.左、右孩子地址 9. 链表不具有的特点是( C ) A.插入、删除不需要移动元素 B.可随机访问任一元素C.不必事先估计存储空间 D.所需空间与线性长度成正比 10. 下面的叙述不正确的是( BC ) A.线性表在链式存储时,查找第i个元素的时间同i的值成正比 AHA12GAGGAGAGGAFFFFAFAF 外科学讲稿首页 讲授时间 2015 年 8 月 31 日课程名称外科学 课型理论(√)实践()计划用时 2 学时 教学内容及授课题目:第二章无菌术和手术基本操作 教学要求:掌握内容 1、掌握常用的灭菌法及消毒法。 2、学会外科洗手、穿无菌手术衣及戴无菌手套。 3、学会手术区的消毒和铺巾。 熟悉内容 1、熟悉手术时的无菌操作规则。 了解内容 1、外科基本操作技术。 2、外科手术的特殊设备 教学要点(重点、难点、疑点): 难点:1.树立无菌观念、认清无菌术的重要性。 重点:1、无菌术在手术切口感染及提高医疗质量中的作用。 2、各项外科基础操作技术 教学进程: (步骤)1、组织教学(2分钟) 2、情景模式带入新课(3分钟) (1)、(30分钟)无菌术的方法及其应用 (2)、(10分钟)手术人员外科洗手、穿无菌手术衣及戴无菌手套视频 (3)、(30分钟)手术人员和患者手术区域的准备及术中无菌原则 (4)、(10分钟)外科基本操作 4、小结(2分钟) 5、预习下次课内容(1分钟) 6、布置作业(2分钟)教学方法:_教学过程采用“教、学、做”一体化的教学模式。“以学生为主体,以能力为重点,以内因为驱动”进行教学导向。结合理论讲授、案例讨论教学法、情景模拟 教学法,通过启发、提问及讨论等多种形式组织教学。 课后记:希望同学们在理解外科无菌术在保证手术成功,促进疾病康复中起到的重要作用的基础上掌握各项无菌操作技术和树立无菌观念。 作业:1、无菌术的概念 2、外科的无菌原则有哪些? 辅助手段和时间分配基本内容1、组织教学 2分钟 2、情景导入新课 3分钟 3、第一部分课(30分钟) 第二章无菌术和手术基本操作 第一节无菌术 无菌术(asepsis):就是针对感染来源和途径所采取的一种有效的预防措施,由灭菌法、消毒法和一定的操作规则及管理制度组成。 1、灭菌法:是杀灭(与手术区或伤口接触的物品上的)一切活的微生物(包括芽孢等)。 2、抗菌法:(消毒法)是指杀灭病原微生物和其他有害微生物,但不要求清除或杀灭所有微生物(如芽胞等)。 3、有关的操作规则及管理制度是为了防止已经灭菌和消毒的物品、已行无菌准备的手术人员、无菌区域再被污染的保障措施。 一、无菌术的方法及其应用 (一)、灭菌法 1、高压蒸气灭菌法:应用最普遍,效果可靠。 (1)、下排气式压力蒸汽灭菌器:用蒸气压力104.0~137.3kPa(15~20 lbf/in2)时,温度可达121~126 ℃,维持30分钟,即能杀死包括具有顽强抵抗力的细菌芽胞在内的一切细菌,达到灭菌目的。 第二章 相互作用 第一单元 力的概念与常见力分析 典型例题答案 【例1】解析:有力存在,必有两个物体同时存在,由于力的相互性,每个物体既是受力物体,同时也是施力物体,故A 正确.力产生的效果不但跟力的大小有关,还与力的方向、作用点等有关,故B 错.力的作用效果除运动状态改变还有形变,故C 错.竖直向上升的物体,找不到施力物体,故此力不存在,D 错. 答案:A 说明:力具有物质性、相互性、矢量性、同时性等性质,要全面理解力的概念. 【例2】解析:物体受重力与运动状态是静止还是运动无关,故A 错.重力实际是万有引力的一个分力(另一个分力提供物体绕地球自转的向心力),万有引力方向指向地心,重力不一定 (只有两极或赤道重力指向地心)故B 错.在赤道上,物体的重力等于万有引力与物体随地球运动的向心力之差,而在赤道上向心力最大,故物体的重力最小,C 正确. 只有在弹簧静止或匀速运动时,测出的才是物体的重力,若弹簧秤拉着物体加速上升或下降则弹簧秤的示数不等于重力,故D 错. 答案:C 说明:重力与引力的关系:引力除产生重力外,还要提供物体随地球自转所需的向心力,因物体在地球上不同的纬度处随地球自转所需的向心力不同,故同一物体在地球上不同纬度处重力大小不同,在两极最大,赤道最小. 【例3】解析:如图2-7所示. 说明:弹力是一种接触力,一定在接触处发生,画弹力的方向时,作用点要画在接触处,最好有参照物如指向球心、加垂直号等. 【例4】解析:A 向上提起的高度为弹簧增加的长度.开始时,弹簧被压缩,对A 有mg=kx 1,离开地面时,弹簧被拉伸,对B 有2mg=kx 2,A 上提高度x =x 1+x 2=3mg/k 【例5】解析:因为f=μN=O.1×200N=2ON ,可认为最大静摩擦力fm=2ON ,所以静摩擦力的取值范围是O 第二章矩阵 一、知识点复习 1、矩阵的定义 由m n个数排列成的一个m行n列的表格,两边界以圆括号或方括号,就成为一个m n型矩阵。例如 2 -1 0 1 1 1 1 1 0 2 2 5 4 -2 9 3 3 3 -1 8 是一个45矩阵. 一个矩阵中的数称为它的元素,位于第i行第j列的数称为(i,j)位元素。 元素全为0的矩阵称为零矩阵,通常就记作0。 两个矩阵A和B相等(记作A=B),是指它的行数相等,列数也相等(即它们的类型相同),并且对应的元素都相等。 2、 n阶矩阵与几个特殊矩阵 行数和列数相等的矩阵称为方阵,行列数都为n的矩阵也常常叫做n阶矩阵。 n阶矩阵的从左上角到右下角的对角线称为主对角线。 下面列出几类常用的n阶矩阵,它们都是考试大纲中要求掌握的. 对角矩阵: 对角线外的的元素都为0的n阶矩阵. 单位矩阵: 对角线上的的元素都为1的对角矩阵,记作E(或I). 数量矩阵: 对角线上的的元素都等于一个常数c的对角矩阵,它就是c E. 上三角矩阵: 对角线下的的元素都为0的n阶矩阵. 下三角矩阵: 对角线上的的元素都为0的n阶矩阵. 对称矩阵: 满足A T=A矩阵,也就是对任何i,j,(i,j)位的元素和(j,i)位的元素总是相等的n阶矩阵. 反对称矩阵:满足A T=-A矩阵.也就是对任何i,j,(i,j)位的元素和(j ,i)位的元素之和总等于0的n阶矩阵.反对称矩阵对角线上的元素一定都是0.) 正交矩阵:若AA T=A T A=E,则称矩阵A是正交矩阵。 (1)A是正交矩阵?A T=A-1 (2)A是正交矩阵?2 A=1 阶梯形矩阵:一个矩阵称为阶梯形矩阵,如果满足: ①如果它有零行,则都出现在下面。 ②如果它有非零行,则每个非零行的第一个非0元素所在的列号自上而下严 格单调递增。 把阶梯形矩阵的每个非零行的第一个非0元素所在的位置称为台角。 每个矩阵都可以用初等行变换化为阶梯形矩阵,这种运算是在线性代数的各类 计算题中频繁运用的基本运算,必须十分熟练。 请注意:一个矩阵用初等行变换化得的阶梯形矩阵并不是唯一的,但是其非零 行数和台角位置是确定的。 3、矩阵的线形运算 (1)加(减)法:两个m n的矩阵A和B可以相加(减),得到的和(差)仍是m n 矩阵,记作A+B (A-B),运算法则为对应元素相加(减). (2)数乘: 一个m n的矩阵A与一个数c可以相乘,乘积仍为m n的矩阵, 记作c A,运算法则为A的每个元素乘c. 这两种运算统称为线性运算,它们满足以下规律: ①加法交换律:A+B=B+A. 2加法结合律:(A+B)+C=A+(B+C). ③加乘分配律:c(A+B)=c A+c B.(c+d)A=c A+d A. ④数乘结合律: c(d)A=(cd)A. ⑤ c A=0 c=0 或A=0. 4、矩阵乘法的定义和性质 (1)当矩阵A的列数和B的行数相等时,则A和B可以相乘,乘积记作AB. AB的行数和A相等,列数和B相等. AB的(i,j)位元素等于A的第i个行向量 和B的第j个列向量(维数相同)对应分量乘积之和. 第2章线性表习题解答 第2章习题 (2) 第2章习题 2.1若将顺序表中记录其长度的分量listlen改为指向最后一个元素的位置last,在实现各基本运算时需要做那些修改? 【解】 //用线性表最后一个元素的下标last代替listLen实现顺序表 #define MAXLEN 100 typedef int elementType; typedef struct sllLast { elementType data[MAXLEN]; int last; }seqList; //初始化 void initialList(seqList &S) { https://www.wendangku.net/doc/4015110873.html,st=-1; } //求表长度 int listLength(seqList S) { return https://www.wendangku.net/doc/4015110873.html,st+1; } //按序号取元素 bool getElement(seqList S,int i,elementType &x) { if(i<1 || i>https://www.wendangku.net/doc/4015110873.html,st+1) //i为元素编号,有效范围在https://www.wendangku.net/doc/4015110873.html,st+1之间 return false; else { x=S.data[i-1]; return true; } } //查找元素x,成功:返回元素编号;失败:返回0 int listLocate(seqList S,elementType x) { int i; for(i=0;i<=https://www.wendangku.net/doc/4015110873.html,st;i++) { if(S.data[i]==x) return i+1; //找到,转换为元素编号输出 } return 0; } //插入元素 int listInsert(seqList &S,elementType x, int i) 西综考研同步练习题之外科学第二章无菌术 1.(A1题型)不能用高压蒸气灭菌的物品是 A、刀、剪 B、布类敷料 C、内镜 D、瓶装溶液 [正确答案]C [考点定位]无菌术(9版外科学P6). 2.(A1题型)穿无菌手术衣和戴无菌手套后,无菌地带的范围 A、肩、上肢、胸、腹的前面 B、肩、上肢、腰部以上的前胸 C、肩、上肢、腰部以上的前胸和两侧 D、上肢、腰部以上的前胸和侧胸 [正确答案]D [考点定位]手术进行中的无菌原则(8版外科学P8). 3.(A1题型)对口腔、会阴部皮肤的消毒常用 A、2.5%碘酊 B、70%酒精 C、安尔碘溶液 D、碘伏 [正确答案]D [考点定位]消毒法(8版外科学)。 4.(A1题型)关于无菌原则下列哪项是错误的 A、手术病人手术区消毒是灭杀拟作切口处及周围皮肤上的细菌 B、有上呼吸道感染的病人不得进入手术室 C、手术者手臂消毒后,在手术过程中不一定是始终无菌的 D、手术进行时不应开窗通风或使用电风扇 [正确答案]B [考点定位]手术进行中的无菌原则(8版外科学)。 5.(A1题型)临床上最常用的灭菌方法是 A、高压蒸汽灭菌法 B、煮沸法 C、干热灭菌法 D、药物浸泡法 [正确答案]A [考点定位]灭菌法(8版外科学)。 6.(A1题型)手术敷料最常用的消毒方法 A、高压蒸气灭菌法 B、甲醛蒸气熏蒸法 C、煮沸灭菌法 D、蒸气灭菌法 [正确答案]A [考点定位]高压蒸气灭菌法(8版外科学)。 7.(A1题型)手术器械和敷料的常用灭菌方法是 A、甲醛熏料法 B、紫外线消毒 C、高压蒸气灭菌 D、电离辐射法 [正确答案]C [考点定位]灭菌法(8版外科学)。 第一章 行列式 习题1.1 1. 证明:(1)首先证明)3(Q 是数域。 因为)3(Q Q ?,所以)3(Q 中至少含有两个复数。 任给两个复数)3(3,32211Q b a b a ∈++,我们有 3 )()3()3)(3(3)()()3()3(3)()()3()3(2121212122112121221121212211b a a b b b a a b a b a b b a a b a b a b b a a b a b a +++=++-+-=+-++++=+++。 因为Q 是数域,所以有理数的和、差、积仍然为有理数,所以 ) 3(3)()3()3)(3()3(3)()()3()3()3(3)()()3()3(2121212122112121221121212211Q b a a b b b a a b a b a Q b b a a b a b a Q b b a a b a b a ∈+++=++∈-+-=+-+∈+++=+++。 如果0322≠+b a ,则必有22,b a 不同时为零,从而0322≠-b a 。 又因为有理数的和、差、积、商仍为有理数,所以 )3(33) (3)3() 3)(3()3)(3(3 32 2 22212122222121222222112211Q b a b a a b b a b b a a b a b a b a b a b a b a ∈--+--= -+-+= ++。 综上所述,我们有)3(Q 是数域。 (2)类似可证明)(p Q 是数域,这儿p 是一个素数。 (3)下面证明:若q p ,为互异素数,则)()(q Q p Q ?。 (反证法)如果)()(q Q p Q ?,则q b a p Q b a +=? ∈?,,从而有 q ab qb a p p 2)()(222++==。 由于上式左端是有理数,而q 是无理数,所以必有02=q ab 。 所以有0=a 或0=b 。 如果0=a ,则2 qb p =,这与q p ,是互异素数矛盾。 如果0=b ,则有 a p =,从而有“有理数=无理数”成立,此为矛盾。 所以假设不成立,从而有)()(q Q p Q ?。 (A )需经常修改L 中的结点值 (E )需不断对L 进行删除插入 第二部分线性表 、选择题 1 ?关于顺序存储的叙述中,哪一条是不正确的 (B ) A. 存储密度大 B. 逻辑上相邻的结点物理上不必邻接 C. 可以通过计算直接确定第 i 个结点的位置 D. 插入、删除操作不方便 2.长度为n 的单链表连接在长度为 m 的单链表后的算法的时间复杂度为 (C ) A 0( n ) B 0(1) C 0(m ) D 0(m+n ) 3 .在n 个结点的顺序表中,算法的时间复杂度是 0(1)的操作是:(A ) A 访问第i 个结点(1<=i<=n )和求第i 个结点的直接前趋(2<=i<=n ) B 在第i 个结点(1<=i<=n )后插入一个新结点 C 删除第i 个结点(1<=i<=n ) D 将n 个结点从小到大排序 4.一个向量第一个兀素的存储地址是 100 ,每个兀素的长度为 2 ,则第5 个兀素的地址是 (B ) ( A ) 110 ( B ) 108 (C ) 100 ( D ) 120 5 .已知一个顺序存储的线性表, 设每个结点需要占 m 个存储单元,若第一个结点的地址为 da , 则第i 个结点的地址为:(A ) 7 .链表是一种采用( B )存储结构存储的线性表。 (A )顺序 (B )链式 (C )星式 (D )网状 8 .线性表若采用链式存储结构时,要求内存中可用存储单兀的地址: (D ) (A )必须是连续的 (B )部分地址必须是连续的 (C )一定是不连续的 (D )连续或不连续都可以 9 .线性表L 在_ ( B )情况下适用于使用链式结构实现。 A ) da+(i-1)*m B ) da+i*m 6.在具有n 个结点的单链表中,实现( A )遍历链表和求链表的第 i 个结点 C )删除开始结点 C ) da-i*m D ) da+(i+1)*m A )的操作,其算法的时间复杂度为 0(n )。 B )在地址为p 的结点之后插入一个结点 D ) 删除地址为p 的结点的后继结点 第二章线性表练习题 一、选择题 1.线性表是具有n个的有限序列。 A、表元素 B、字符 C、数据元素 D、数据项 E、信息项 2.线性表的静态链表存储结构与顺序存储结构相比优点是。 A、所有的操作算法实现简单 B、便于随机存储 C、便于插入和删除 D、便于利用零散的存储器空间 3.若长度为n的线性表采用顺序存储结构,在其第i个位置插入一个新元素算法的时间复杂度为。 A、O(log2n) B、O(1) C、O(n) D、O(n2) 4.(1)静态链表既有顺序存储的特点,又有动态链表的优点。所以,它存取表中第i个元素的时间与i无关; (2)静态链表中能容纳元素个数的最大数在定义时就确定了,以后不能增加;(3)静态链表与动态链表在元素的插入、删除上类似,不需做元素的移动。 以上错误的是。 A、(1)、(2) B、(1) C、(1)、(2)、(3) D、(2) 6.在双向链表存储结构中,删除p所指的结点时须修改指针。 A、p->next->prior=p->prior; p->prior->next=p->next; B、p->next=p->next->next;p->next->prior=p; C、p->prior->next=p;p->prior=p->prior->prior; D、p->prior=p->next->next;p->next=p->prior->prior; 7.在双向循环链表中,在P指针所指的结点后插入q所指向的新结点,其修改指针的操作是。 A、p->next=q; q->prior=p;p->next->prior=q;q->next=q; B、p->next=q;p->next->prior=q;q->prior=p;q->next=p->next; C、q->prior=p; q->next=p->next; p->next->prior=q; p->next=q; D、q->next=p->next;q->prior=p;p->next=q;p->next=q; 8.将两个各有n个元素的有序表归并成一个有序表,其最少的比较次数是。 A、 n b、2n-1 c、2n d、n-1 9.在一个长度为n的顺序表中,在第i个元素(1≤i≤n+1)之前插入一个新元素时须向后移动个元素。 A、n-i B、n-i+1 C、n-i-1 D、i 10.线性表L=(a1,a2,……an),下列说法正确的是。 A、每个元素有有一个直接前驱和一个直接后继 B、线性表中至少有一个元素 C、表中诸元素的排列必须是由小到大或由大到小。 D、除第一个和最后一个元素外,其余每个元素都有一个且仅有一个直接前驱和直接后继。 11.对单链表表示法,以下说法错误的是。 A、数据域用于存储线性表的一个数据元素 B、指针域(或链域)用于存放一指向本结点所含数据元素的直接后继所在结点的指针 C、所有数据通过指针的链接而组织成单链表 D、NULL称为空指针,它不指向任何结点只起标志作用 第二章相互作用 第 1 课时力、重力、弹力 基础知识归纳 1.力的概念 (1)力的概念:力是物体对物体的作用. (2)力的基本特征: ①物质性:力不能脱离物体而独立存在. ②相互性:力的作用是相互的. ③矢量性:既有大小,又有方向,其运算法则为平行四边形定则. ④独立性:一个力作用在某一物体上产生的效果与这个物体是否同时受到其他力的作用无关. ⑤同时性:物体间的相互作用总是同时产生,同时变化,同时消失. (3)力的作用效果:使物体发生形变或使物体的运动状态发生改变(即产生加速度). (4)力的表示 可用力的图示或力的示意图表示,其中力的图示包含力的大小、方向和作用点三要素. (5)力的分类 ①按性质分:重力、弹力、摩擦力、分子力、电磁力、核力等. ②按效果分:压力、支持力、拉力、动力、阻力、向心力、回复力等. ③按研究对象分:内力和外力. 2.重力 (1)重力的产生:由于地球的吸引而产生的.地球周围的物体,无论与地球接触与否,运动状态如何,都要受到地球的吸引力,因此任何物体都要受到重力的作用. (2)方向:总是竖直向下. (3)大小:G=mg. (4)重心:重力的等效作用点.重心的位置与物体的形状和质量的分布有关.重心不一定在物体上.质量分布均匀、形状规则的物体的重心在几何中心上.薄板类物体的重心可用悬挂法确定. 3.弹力 (1)定义:发生弹性形变的物体,对跟它接触的物体产生力的作用,这种力叫弹力. (2)产生条件:两物体直接接触、接触处有弹性形变;两者缺一不可,并且弹力和形变同时产生,同时消失. (3)方向:与施力物体形变的方向相反,弹力的受力物体是引起形变的物体,施力物体是发生形变的物体. (4)大小:弹簧类物体在弹性限度内遵循胡克定律:F=kx.非弹簧类弹力大小应由平衡条件或动力学规律求解. 第二章线性表习题及答案 一、基础知识题 2.1 试描述头指针、头结点、开始结点的区别、并说明头指针和头结点的作用。 答:始结点是指链表中的第一个结点,也就是没有直接前趋的那个结点。 链表的头指针是一指向链表开始结点的指针(没有头结点时),单链表由头指针唯一确定,因此单链表可以用头指针的名字来命名。 头结点是我们人为地在链表的开始结点之前附加的一个结点。有了头结点之后,头指针指向头结点,不论链表否为空,头指针总是非空。而且头指针的设置使得对链表的第一个位置上的操作与在表其他位置上的操作一致(都是在某一结点之后)。 2.2 何时选用顺序表、何时选用链表作为线性表的存储结构为宜? 答:在实际应用中,应根据具体问题的要求和性质来选择顺序表或链表作为线性表的存储结构,通常有以下几方面的考虑: 1.基于空间的考虑。当要求存储的线性表长度变化不大,易于事先确定其大小时,为了节约存储空间,宜采用顺序表;反之,当线性表长度变化大,难以估计其存储规模时,采用动态链表作为存储结构为好。 2.基于时间的考虑。若线性表的操作主要是进行查找,很少做插入和删除操作时,采用顺序表做存储结构为宜;反之,若需要对线性表进行频繁地插入或删除等的操作时,宜采用链表做存储结构。并且,若链表的插入和删除主要发生在表的首尾两端,则采用尾指针表示的单循环链表为宜。 2.3 在顺序表中插入和删除一个结点需平均移动多少个结点?具体的移动次数取决于哪两个因素? 答:在等概率情况下,顺序表中插入一个结点需平均移动n/2个结点。删除一个结点需平均移动(n-1)/2个结点。具体的移动次数取决于顺序表的长度n以及需插入或删除的位置i。i 越接近n则所需移动的结点数越少。 2.4 为什么在单循环链表中设置尾指针比设置头指针更好? 答:尾指针是指向终端结点的指针,用它来表示单循环链表可以使得查找链表的开始结点和终端结点都很方便,设一带头结点的单循环链表,其尾指针为rear,则开始结点和终端结点的位置分别是rear->next->next 和rear, 查找时间都是O(1)。 若用头指针来表示该链表,则查找终端结点的时间为O(n)。 2.5 在单链表、双链表和单循环链表中,若仅知道指针p指向某结点,不知道头指针,能否将结点*p从相应的链表中删去?若可以,其时间复杂度各为多少? 答:我们分别讨论三种链表的情况。 1. 单链表。当我们知道指针p指向某结点时,能够根据该指针找到其直接后继,但是由于不知道其头指针,所以无法访问到p指针指向的结点的直接前趋。因此无法删去该结点。 2. 双链表。由于这样的链表提供双向链接,因此根据已知结点可以查找到其直接前趋和直接后继,从而可以删除该结点。其时间复杂度为O(1)。 3. 单循环链表。根据已知结点位置,我们可以直接得到其后相邻的结点位置(直接后继),又因为是循环链表,所以我们可以通过查找,得到p结点的直接前趋。因此可以删去p所指结点。其时间复杂度应为O(n)。 2.6 下述算法的功能是什么? LinkList Demo(LinkList L){ // L 是无头结点单链表 ListNode *Q,*P; if(L&&L->next){ Q=L;L=L->next;P=L; 第2章习题 (1) 第2章习题 2.1若将顺序表中记录其长度的分量listlen改为指向最后一个元素的位置last,在实现各基本运算时需要做那些修改? 【解】 //用线性表最后一个元素的下标last代替listLen实现顺序表 #define MAXLEN 100 typedef int elementType; typedef struct sllLast { elementType data[MAXLEN]; int last; }seqList; //初始化 void initialList(seqList &S) { https://www.wendangku.net/doc/4015110873.html,st=-1; } //求表长度 int listLength(seqList S) { return https://www.wendangku.net/doc/4015110873.html,st+1; } //按序号取元素 bool getElement(seqList S,int i,elementType &x) { if(i<1 || i>https://www.wendangku.net/doc/4015110873.html,st+1) //i为元素编号,有效范围在https://www.wendangku.net/doc/4015110873.html,st+1之间 return false; else { x=S.data[i-1]; return true; } } //查找元素x,成功:返回元素编号;失败:返回0 int listLocate(seqList S,elementType x) { int i; for(i=0;i<=https://www.wendangku.net/doc/4015110873.html,st;i++) { if(S.data[i]==x) return i+1; //找到,转换为元素编号输出} return 0; } //插入元素 int listInsert(seqList &S,elementType x, int i) { int k; if(https://www.wendangku.net/doc/4015110873.html,st>MAXLEN-1) return 0; //表满,返回0 else if(i<1 || i>https://www.wendangku.net/doc/4015110873.html,st+2) return 1; //插入位置查处范围,返回1 else { for(k=https://www.wendangku.net/doc/4015110873.html,st;k>=i-1;k--) S.data[k+1]=S.data[k]; S.data[i-1]=x; https://www.wendangku.net/doc/4015110873.html,st++; return 2; } } //删除元素 int listDelete(seqList &S,int i) { int k; if(https://www.wendangku.net/doc/4015110873.html,st==-1) return 0; //空表,返回0 else if(i<1 || i>https://www.wendangku.net/doc/4015110873.html,st+1) return 1; //删除元素编号超出范围,返回1 else 第二章 相互作用 第1单元 力 重力和弹力 摩擦力 【例1】如图所示,两物体重力分别为G 1、G 2,两弹簧劲度系数分别为k 1、k 2,弹簧两端与物体和地面相连。用竖直向上的力缓慢向上拉G 2,最后平衡时拉力F=G 1+2G 2,求该过程系统重力势能的增量。 练习 1.关于两物体之间的弹力和摩擦力,下列说法中正确的是( ) A.有摩擦力一定有弹力 B.摩擦力的大小与弹力成正比 C.有弹力一定有摩擦力 D.弹力是动力,摩擦力是阻力 2.如图,两本书A 、B 逐页交叉后叠放在一起并平放在光滑的水平桌面 上,设每张书页的质量为5g ,每本书均是200张,纸与纸之 间的动摩擦因数为0.3,问至少要用多大的水平力才能将它们 拉开?(g 取10米/秒2) 3、弹簧秤的读数是它受到的合外力吗? 【例2】 小车向右做初速为零的匀加速运动,物体恰好沿车后壁匀速下滑。试分析下滑过程中物体所受摩擦力的方向和物体速度方向的关系。 例题分析: 例3、下面关于摩擦力的说法正确的是: A 、阻碍物体运动的力称为摩擦力; B 、滑动摩擦力方向总是与物体的运动方向相反; C 、静摩擦力的方向不可能与运动方向垂直; D 、接触面上的摩擦力总是与接触面平行。 例4、如图所示,物体受水平力F 作用,物体和放在水平面上 的斜面都处于静止,若水平力F 增大一些,整个装置仍处于静 止,则: A 、 斜面对物体的弹力一定增大; B 、 斜面与物体间的摩擦力一定增大; C 、 水平面对斜面的摩擦力不一定增大; F k 2 Δx 2/ k 1 G 1 Δx 2 G 2 Δx 1 Δx 1/ F G 1 G 2 k 2 k 1 a v 相对 第二章 矩阵及其运算 1 已知线性变换 ?????++=++=++=3 21332123 2113235322y y y x y y y x y y y x , 求从变量x 1 x 2 x 3到变量y 1 y 2 y 3的线性变换 解 由已知 ? ??? ?????? ? ?=???? ??22 1321323513122y y y x x x 故 ???? ?????? ? ?=???? ??-3211 221323513122x x x y y y ? ??? ?????? ??----=321423736 947y y y ?????-+=-+=+--=3 21332123 211423736947x x x y x x x y x x x y 2 已知两个线性变换 ?????++=++-=+=3 2133 2123 11542322y y y x y y y x y y x ?????+-=+=+-=3 233122 11323z z y z z y z z y 求从z 1 z 2 z 3到x 1 x 2 x 3的线性变换 解 由已知 ???? ?????? ? ?-=???? ??221321514232102y y y x x x ??? ? ?????? ??--???? ??-=32131 010 2013514232102z z z ??? ? ?????? ??----=32 1161109412316z z z 所以有?????+--=+-=++-=3 2133 2123 2111610941236z z z x z z z x z z z x 3 设???? ??--=111111111A ??? ? ??--=150421321B 求3AB 2A 及A T B 解 ??? ? ??---???? ??--???? ??--=-1111111112150421321111111111323A AB ???? ??----=???? ??---???? ??-=2294201722213211111111120926508503 ??? ? ??-=???? ??--???? ??--=092650850150421321111111111B A T 4 计算下列乘积 (1)??? ? ?????? ??-127075321134 解 ???? ?????? ??-127075321134???? ???+?+??+?-+??+?+?=102775132)2(71112374?? ? ? ??=49635 (2)???? ??123)321( 解 ??? ? ??123)321((132231)(10) 第二章相互作用 2.1 重力弹力摩擦力 高频考点一力的基本概念和重力 知识点一力 1.定义:力是物体与物体间的相互作用. 2.作用效果:使物体发生形变或改变物体的运动状态(即产生加速度). 3.性质:力具有物质性、相互性、共存性、矢量性、独立性等特征. 知识点二重力 1.产生:由于地球吸引而使物体受到的力.注意:重力不是万有引力,而是万有引力竖直向下的一个分力. 2.大小:G=mg,可用弹簧测力计测量.G的变化是由在地球上不同位置处g的变化引起的. 3.方向:总是竖直向下.注意:竖直向下是和水平面垂直,不一定和接触面垂直,也不一定指向地心. 4.重心:物体的每一部分都受重力作用,可认为重力集中作用于一点即物体的重心. (1)影响重心位置的因素:物体的几何形状;物体的质量分布. (2)不规则薄板形物体重心的确定方法:悬挂法. 例1.(2020·浙江金华调研)下列有关力的说法中正确的是() A.力的产生离不开施力物体,但可以没有受力物体,例如,一个人用很大的力挥动网球拍,却没击中球,有施力物体而没有受力物体 B.力的产生离不开受力物体,但可以没有施力物体,例如物体冲上光滑斜面,在沿斜面上升过程中受到沿斜面向上的冲力,这个力没有施力物体 C.力是物体对物体的作用,如果找不到施力物体或受力物体,说明这个力就不存在 D.不接触的物体间也可以产生力的作用,例如,磁铁吸引铁钉,可见力可以离开物体单独存在 【答案】C 【解析】力的产生离不开施力物体,也离不开受力物体.一个人用很大的力挥动网球拍,却没击中球,球拍对球并没有力的作用,故A错误;力的产生离不开受力物体和施力物体,物体冲上光滑斜面的过程中,并没有受到向上的冲力,故B错误;力是一个物体对另一个物体的作用,如果找不到施力物体或受力物体,说明这个力就不存在,故C正确;不接触的物体间也可以产生力的作用,磁铁吸引铁钉,是磁铁的磁场对铁钉产生的作用,不能说明力可以离开物体单独存在,故D错误. 例2.下列生活现象中关于力的说法正确的是D A. 拳击手一拳击出,没有击中对方,这时只有施力物体,没有受力物体 B. 向上抛出后的小球能够向上运动是因为小球受到向上的作用力 习 题 2-1 1.由6名选手参加乒乓球比赛,成绩如下:选手1胜选手2、4、5、6而负于选手3;选手2胜选手4、5、6而负于选手1、3;选手3胜选手1、2、4而负于选手5、6;选手4胜选手5、6而负于选手1、2、3;选手5胜选手3、6而负于选手1、2、4;选手6胜选手2而负于选手1、3、4、5.若胜一场得1分,负一场得0分,使用矩阵表示输赢状况,并排序. 解: ????? ?? ? ? ? ??000010 100100110000001011 1110001110106543216 54321,选手按胜多负少排序为:6,5,4,3,2,1. 2.设矩阵???? ??-=???? ?? +-=2521 ,03231 z x y x B A ,已知B A =,求z y x ,,. 解:由于B A =得?????=-=+=-0253223z x y x ,解得:?? ? ??===211 z y x 。 习 题 2-2 1.设???? ??=0112A ,??? ? ??-=4021B ,求 (1)B A 52-; (2)BA AB -; (3)2 2B A -. 解:(1)??? ? ??--=???? ??--???? ??=???? ??--???? ??=-202892001050224402150112252B A ; (2)???? ??--=???? ??--???? ??--=???? ?????? ??--???? ??-???? ??=-2592041021820112402140210112BA AB ; (3)??? ? ??--=???? ??-???? ??=???? ??-???? ??--???? ?????? ??=-152441606112254021402101120112B A 22. 2.已知????? ??--=230412301321A ,??? ? ? ??---=052110 35123 4B ,求B A 23-. 解:??? ? ? ??----????? ??--=052110351234223041230 13 21 323B -A ??? ? ? ??----=????? ??----????? ??--=61941016151055011010422061024686901236903963 3.设??? ? ? ??----=????? ??=101012121234,432112 122121B A ,求 第二章线性表 一、填空题 1、数据逻辑结构包括线性结构、树型结构、图型结构这三种类型,树形结构和图形结构合称为非线性结构。 2、在线性结构中,第一个结点没有前驱结点,其余每个结点有且只有个前驱结点,最后一个结点没有后续结点,其余每个结点有且只有一个后续结点。 3、在顺序表中插入或删除一个元素,需要平均移动一半元素,具体移动的元素个数与插入或删除的位置有关。 4、在顺序表中,逻辑上相邻的元素,其物理位置一定相邻。在单链表中,逻辑上相邻的元素,其物理位置不一定相邻。 5、在带头结点的非空单链表中,头结点的存储位置由头指针指示,首元素结点的存储位置由头结点的next域指示,除首元素结点外,其它任一元素结点的存储位置由其直接前趋结点的next域指示。 6、阅读下列算法,并补充所缺内容。 void purge_linkst( ListNode *& la ) { // 从头指针为 la 的有序链表中删除所有值相同的多余元素,并释放被删结点空间ListNode *p,*q; if(la==NULL) return; q=la; p = la->link; while (p) { if (p && ___(1)p->data!=q->data___) {q=p; p = p->link;} else { q->link= ___(2)p->link___; delete(p); p=___(3)q->link___; } }//while }// purge_linkst 二、选择题 1、在数据结构中,从逻辑上可以把数据结构分成 C。 A、动态结构和静态结构 B、紧凑结构和非紧凑结构 C、线性结构和非线性结构 D、内部结构和外部结构 2、线性表的逻辑顺序与存储顺序总是一致的,这种说法 B。 A、正确 B、不正确 3、线性表若采用链式存储结构时,要求内存中可用存储单元的地址D。 A、必须是连续的 B、部分地址必须是连续的 C、一定是不连续的 D、连续或不连续都可以 4、在以下的述叙中,正确的是B。 A、线性表的线性存储结构优于链表存储结构 B、二维数组是其数据元素为线性表的线性表 C、栈的操作是先进先出 D、队列的操作方式是先进后出 三、综合题 1、已知L是无表头结点的单链表,且P结点既不是首元结点,也不是尾元结点,试从下列提供的答案中选择合适的语句序列。 A、在P结点后插入S结点的语句序列是((4)、(1)); B、在P结点前插入S结点的语句序列是((7)、(11)、(8)、(4)、(1)); C、在表首插入S结点的语句序列是((5)、(12)); I.单选题(共 12 题,0 分) 1. (0 分)关于煮沸灭菌法,下列哪项是错误的? A. 物品应完全放浸没于水中 B. 缝线和橡胶类煮沸的温度及持续时间与金属器械一样 C. 玻璃类物品消毒时应沙布包好 D. 灭菌时间应从水煮沸后算起 E. 高原地区煮沸的时间应适当延长 2. (0 分)手术人员的术前准备,不规范的是 A. 手及臂部皮肤有破损时不能参加手术 B. 手术前不能进行任何换药操作 C. 术前应剪短指甲 D. 术前应先穿衣,后戴手套 E. 手套未破,需更换手术时,可直接戴手套上台手术 3. (0 分)横结肠造口术后患者施行瘘口关闭术,手术区皮肤消毒涂擦消毒剂的顺序是: A. 由手术区中心部向四周涂擦 B. 由手术区外周涂向瘘口周围 C. 由手术区的上方涂向下方 D. 由手术区的一侧涂向另一侧 E. 无需按一定的顺序 4. (0 分)消毒的要求是: A. 杀灭一切活的微生物 B. 杀灭病原微生物 C. 杀灭所有微生物 D. 杀灭有害微生物 E. 杀灭病原微生物及其他有害微生物 5. (0 分)下列哪项是错误的: A. 手术病人手术区消毒是消灭拟作切口处及其周围皮肤上的细菌 B. 上呼吸道感染者不得进入手术室 C. 手或臂部有化脓性感染者不能参加手术 D. 手术人员完成手臂消毒后,在手术过程中便始终是无菌的 E. 手术人员在术中,其背部、腰部以下、肩部以上均为有菌带 6. (0 分)下列哪项有违手术的无菌原则 A. 术中手套破损,应立即更换 B. 手不能接触到背部、腰以下和肩部以上 C. 可在手术人员的背后传递器械 D. 手术人员换位时,应背对背 E. 缝合皮肤前,应再次消毒皮肤一次 7. (0 分)下列哪项违反了无菌操作规则: A. 室内空调机风口吹向手术台 B. 手术中刁;能接触手术台边缘以下布单 C. 坠落到手术台边缘的器械不准拾回再用 D. 术中同侧人员调换位置时应背对背,勿接触对方背部不洁区 E. 缝合皮肤切口前,需用70%乙醇再涂擦皮肤消毒一次 8. (0 分)原发性甲亢施行双叶甲状腺次全切除术后,术者手套有破口,需接连施行手术时,术者双手消毒要求是: A. 仅更换手套 B. 加戴无菌手套,穿无菌衣 C. 更换手套、更换手术衣 D. 重新洗手,时间缩短为1分钟 E. 重新洗手 9. (0 分)铺好无菌中单后,如果位置不准确,移动无菌巾位置的原则是: A. 只能由手术区向外移 B. 只能由手术区向下移 C. 只能由手术区向上移 D. 只能向手术区内移 E. 只能由手术区向对侧移 10. (0 分)横结肠造口术后患者施行瘘口关闭术,手术区皮肤消毒涂擦消毒剂的顺序是: A. 由手术区中心部向四周涂擦 B. 由手术区外周涂向瘘口周围 C. 由手术区的上方涂向下方 D. 由手术区的一侧涂向另一侧 E. 无需按一定的顺序 11. (0 分)灭菌和消毒的要求是达到无菌术的要求,故两者都必须:线性代数第二章答案
第二章线性表答案
第二章无菌术和手术基本操作
习全套教学案第二章相互作用答案
线性代数第二章矩阵试题及答案
第2章线性表习题解答
西综考研同步练习题之外科学第二章 无菌术
线性代数课后习题答案(陈维新)
(完整版)数据结构第二章线性表1答案
第2章线性表习题解析(答)
第二章__相互作用 教师用版本
第二章线性表习题及答案
第2章线性表习题解答
高考复习 第二章 相互作用
线性代数第二章答案
第二章 相互作用参考答案
线性代数第二章习题答案
第二章_线性表(参考答案)
第二章无菌术
- 第二章 无菌术
- 第二章无菌术答案
- 西综考研同步练习题之外科学第二章 无菌术
- 外科学第八版第二章无菌术
- 无菌术和手术基本操作
- 细胞工程第二章 细胞工程实验室组成及无菌操作技术
- 第二章无菌术和手术基本操作一 ppt课件
- 第二章-无菌术及手术基本操作(二)PPT课件
- 外科学总论 第二章 无菌术
- 第二章无菌术和手术基本操作
- 细胞工程第二章 细胞工程实验室组成及无菌操作技术-精选文档
- 第二章 无菌术
- 第八版外科学配套02无菌术
- 人卫第九版普外科课件-第二章 无菌术
- 第2章 医院内感染的预防与控制技术 第3节 无菌技术(张新平)
- 2 第二章 无菌术
- 第二章无菌术
- 第二章无菌术和手术基本操作
- 外科学题库及答案-无菌术
- 外科学(总论)_王柏群_第二章无菌术
