电化学原理

可逆体系的循环伏安研究
1 实验目的
1)掌握循环伏安法研究电极过程的基本原理
2)学习使用CHI660电化学综合分析仪
3)测定K3Fe(CN)6体系在不同扫描速率时的循环伏安图
2 实验原理
1)循环伏安法概述:
循环伏安法(Cyclic V oltammetry)的基本原理是:根据研究体系的性质,选择电位扫描范围和扫描速率,从选定的起始电位开始扫描后,研究电极的电位按指定的方向和速率随时间线性变化,完成所确定的电位扫描范围到达终止电位后,会自动以同样的扫描速率返回到起始电位。在电位进行扫描的同时,同步测量研究电极的电流响应,所获得的电流-电位曲线称为循环伏安曲线或循环伏安扫描图。通过对循环伏安扫描图进行定性和定量分析,可以确定电极上进行的电极过程的热力学可逆程度、得失电子数、是否伴随耦合化学反应及电极过程动力学参数,从而拟定或推断电极上所进行的电化学过程的机理。
循环伏安法是进行电化学和电分析化学研究的最基本和最常用的方法,1922年由Jaroslav Heyrovsky创立的以滴汞电极作为工作电极的极谱分析法(Polarography),可以认为是伏安研究方法的早期形式,其对电化学研究领域的杰出贡献,Heyrovsky在1959年获得诺贝尔化学奖。随着固体电极,修饰电极的广泛使用和电子技术的发展,循环伏安法的测试范围和测试技术、数据采集和处理等方面显著改善和提高,从而使电化学和电分析化学方法更普遍地应用于化学化工、生命科学、材料科学及环境和能源等领域。
2)循环伏安扫描图:
循环伏安法研究体系是由工作电极、参比电极、辅助电极构成的三电极系统,工作电极和参比电极组成电位测量,工作电极和辅助电极组成的回路测量电流。工作电极可选用固态或液态电极,如:铂、金、玻璃石墨电极或悬汞、汞膜电极。常用的参比电极有:饱和甘汞电极(SCE)、银-氯化银电极,因此,循环伏安曲线中的电位值都是相对于参比电极而言。辅助电极可选用固态的惰性电极,如:铂丝或铂片电极、玻碳电极等。电解池中的电解液包括:氧化还原体系(常用的浓度范围:mmol/L)、支持电解质(浓度范围:mol/L)。循环伏安测定方法是:将CHI660电化学综合分析仪与研究体系连接,选定电位扫描范围E1~E2和扫描速率υ,从起始电位E1开始扫描,电位按选定的扫描速率呈线性变化从E1到达E2,然后连续反方向再扫描从E2回到E1,如图C17.1所示,电位随时间的变化呈现的是等腰三角波信号。
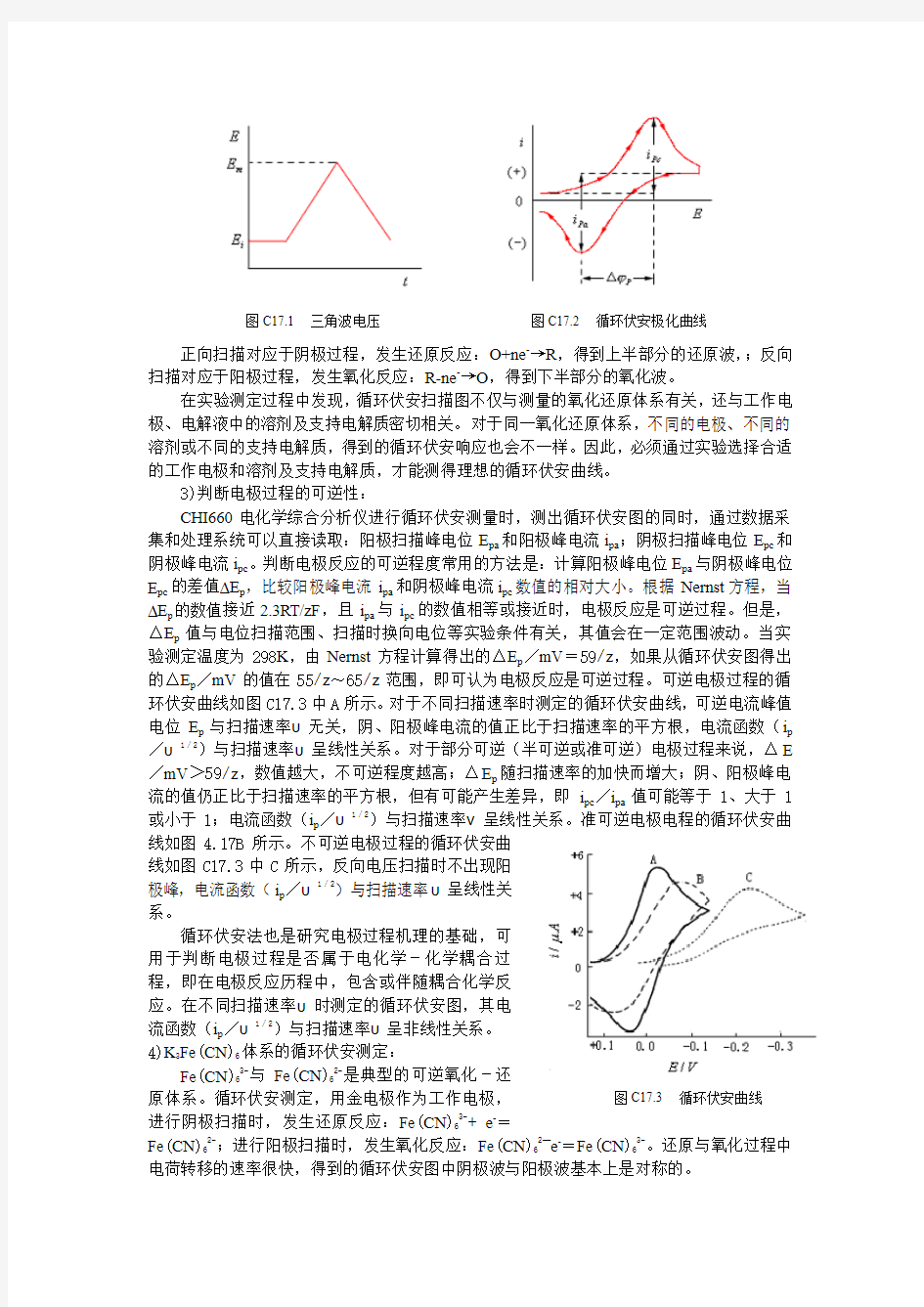
在扫描电位范围内,若在某一电位值时出现电流峰,说明在此电位时发生了电极反应。若在正向扫描时电极反应的产物是足够稳定的,且能在电极表面发生电极反应,那么在返回扫描时将出现于正向电流峰相对应的逆向电流峰。典型的循环伏安曲线如图C17.2所示,i pc 和i pa分别表示阴极峰值电流和阳极峰值电流,对应的阴极峰值电位与阳极峰值电位分别为E pc和E pa。(p表示峰值,a表示阳极,c表示阴极。)
图C17.1 三角波电压图C17.2 循环伏安极化曲线
正向扫描对应于阴极过程,发生还原反应:O+ne-→R,得到上半部分的还原波,;反向扫描对应于阳极过程,发生氧化反应:R-ne-→O,得到下半部分的氧化波。
在实验测定过程中发现,循环伏安扫描图不仅与测量的氧化还原体系有关,还与工作电极、电解液中的溶剂及支持电解质密切相关。对于同一氧化还原体系,不同的电极、不同的溶剂或不同的支持电解质,得到的循环伏安响应也会不一样。因此,必须通过实验选择合适的工作电极和溶剂及支持电解质,才能测得理想的循环伏安曲线。
3)判断电极过程的可逆性:
CHI660电化学综合分析仪进行循环伏安测量时,测出循环伏安图的同时,通过数据采集和处理系统可以直接读取:阳极扫描峰电位E pa和阳极峰电流i pa;阴极扫描峰电位E pc和阴极峰电流i pc。判断电极反应的可逆程度常用的方法是:计算阳极峰电位E pa与阴极峰电位E pc的差值?E p,比较阳极峰电流i pa和阴极峰电流i pc数值的相对大小。根据Nernst方程,当?E p的数值接近2.3RT/zF,且i pa与i pc的数值相等或接近时,电极反应是可逆过程。但是,△E p值与电位扫描范围、扫描时换向电位等实验条件有关,其值会在一定范围波动。当实验测定温度为298K,由Nernst方程计算得出的△E p/mV=59/z,如果从循环伏安图得出的△E p/mV的值在55/z~65/z范围,即可认为电极反应是可逆过程。可逆电极过程的循环伏安曲线如图C17.3中A所示。对于不同扫描速率时测定的循环伏安曲线,可逆电流峰值电位E p与扫描速率υ无关,阴、阳极峰电流的值正比于扫描速率的平方根,电流函数(i p /υ1/2)与扫描速率υ呈线性关系。对于部分可逆(半可逆或准可逆)电极过程来说,△E /mV>59/z,数值越大,不可逆程度越高;△E p随扫描速率的加快而增大;阴、阳极峰电流的值仍正比于扫描速率的平方根,但有可能产生差异,即i pc/i pa值可能等于1、大于1或小于1;电流函数(i p/υ1/2)与扫描速率ν呈线性关系。准可逆电极电程的循环伏安曲线如图4.17B所示。不可逆电极过程的循环伏安曲
线如图C17.3中C所示,反向电压扫描时不出现阳
极峰,电流函数(i p/υ1/2)与扫描速率υ呈线性关
系。
循环伏安法也是研究电极过程机理的基础,可
用于判断电极过程是否属于电化学-化学耦合过
程,即在电极反应历程中,包含或伴随耦合化学反
应。在不同扫描速率υ时测定的循环伏安图,其电
流函数(i p/υ1/2)与扫描速率υ呈非线性关系。
4)K3Fe(CN)6体系的循环伏安测定:
Fe(CN)63-与Fe(CN)62-是典型的可逆氧化-还
图C17.3 循环伏安曲线
原体系。循环伏安测定,用金电极作为工作电极,
进行阴极扫描时,发生还原反应:Fe(CN)63-+e-=
Fe(CN)62-;进行阳极扫描时,发生氧化反应:Fe(CN)62—e-=Fe(CN)63-。还原与氧化过程中电荷转移的速率很快,得到的循环伏安图中阴极波与阳极波基本上是对称的。
3 仪器与试剂
CHI660电化学综合分析仪电子天平
园盘金电极容量瓶(100mL,250mL)
铂丝电极烧杯(100mL)
饱和甘汞电极KNO3溶液(0.4mol/L)
超级恒温槽K3Fe(CN)6标准溶液(5.0×10-2mol/L)
双层三口瓶H2SO4溶液(0.5~1.0mol/L)
图C17.4 实验装置示意图
4 实验步骤
1)实验装置如图C17.4所示。参见本书B3-10部分,熟悉CHI660A电化学综合分析仪操作系统。
2)调节并控制恒温槽水浴温度为(298±0.2)K,将恒温水通入三颈瓶的恒温夹套中。
3)组成循环伏安测定系统:0.4mol/L的KNO3溶液作为支持电解质,用此溶液作为溶剂,将K3Fe(CN)6标准溶液(5.0×10-2mol/L)稀释,配制成(5.0×10-3mol/L)的K3Fe(CN)6溶液100mL,转入三颈瓶中约50mL。与电化学综合分析仪接通:金电极作为研究电极与绿色夹相连,铂丝电极作为辅助电极与红色夹相连,饱和甘汞电极作为参比电极与白色夹相连。4)循环伏安扫描曲线测定:开启微机,进入CHI660软件操作系统,执行Setup菜单中Technique命令,选择Cyclic V oltmmetry 实验技术,进入Parameters设置扫描参数,Init E(V) = - 0.2 , High E (V) = 0.5, Low E (V) = - 0.2, Initial Scan = Negative, Scan Rate (V/s) = 0.05, Sweep Segments =2, Sample Interval (V) = 0.001, Quiet Time (sec) = 2, Sensitivity(A/V) = 5.e-006,点OK确定所选定的参数,同时进入Cyclic Voltmmetry 测量技术,显示Potential-Current坐标图,点击→开始扫描,自动记录循环伏安曲线。根据峰电流的大小,调节Sensitivity(A/V)的选值,最终得到好的循环伏安图。利用数据处理软件记录在所选定的测试条件,并读取峰电位和峰电流的数值,将实验结果图存入Word文档。改变扫描速率,测定扫描速率υ/(mV/s)分别为:50、100、200、250、300、400、500、600、700、800时的循环伏安图,记录在不同扫描速率时的峰电位和峰电流的数值,填入数据记录表。
5)研究电极的处理:作为研究电极的金电极,反复使用多次后,继续进行循环伏安扫描时,不出现峰电流或峰电流很小,原因可能是在电极表面有沉积物或电极发生钝化,需对电极进行处理。处理方法是:将三电极用去离子水冲洗干净,在0.5~1.0mol/L的H2SO4溶液中,进行循环电位扫描,调节到较大的电位范围:(-0.2-1.5)V,观察到电极上有较多气泡出现。处理后的电极系统,一定要冲洗干净,才能放入研究体系。
5 数据记录与处理
1)打印扫描速率υ=50 mV/s时的实验结果图,内容包括:循环伏安曲线,扫描参数,数据处理结果。
2)将不同扫描速率时的循环伏安曲线测定的阴极、阳极峰电位和峰电流列表记录,计算△E p和电流函数。
3)根据ΔE p的数值,判断电极过程的可逆程度。讨论扫描速率是否会影响此类电极过程的E p及ΔE p。
4)计算表中不同扫描速率时的电流函数,以电流函数对扫描速率作图。分别讨论电极上进行的氧化-还原过程是否伴随有耦合化学反应。
5)使用微机进行数据处理,给出线性相关程度。
表C17.1 实验数据
6 注意事项
1)测量过程中,构成电流处理回路的研究电极和辅助电极有较大电流通过,而参比电极不应有电流通过,因此,必须正确连接研究电极、辅助电极和参比电极,仔细检查确认后,再开始测定。
2)不能把溶液等试剂放在电化学综合分析仪仪器上面,以免试剂损坏仪器。
7 思考题
1)用循环伏安研究不同的电极过程时,如何选择和确定合适的扫描速率。扫描速率的影响与电极反应得、失电子的难易程度的联系如何?
2)电位扫描的范围,对测定结果有何影响?是否电位范围越大测定结果越好?
3)讨论循环伏安曲线中峰值电流i p的影响因素。
电化学原理及其应用(习题及答案)
第六章电化学原理及其应用 一、选择题 1.下列电极反应中,溶液中的pH值升高,其氧化态的氧化性减小的是(C) A. Br2+2e = 2Br- B. Cl2+2e=2Cl— C. MnO4—+5e+8H+=2Mn2++4H2O D. Zn2++2e=Zn 2.已知H2O2在酸性介质中的电势图为O2 0.67V H2O2 1.77V H2O,在碱性介质中的电势图为O2-0.08V H2O2 0.87V H2O,说明H2O2的歧化反应(C) A.只在酸性介质中发生 B.只在碱性介质中发生 C.无论在酸、碱性介质中都发生D.与反应方程式的书写有关 3.与下列原电池电动势无关的因素是Zn |Zn2+‖H+,H2 | Pt (B) A. Zn2+的浓度 B. Zn电极板的面积 C.H+的浓度 D.温度 4.298K时,已知Eθ(Fe3+/Fe)=0.771V,Eθ(Sn4+/Sn2+)=0.150V,则反应2Fe2++Sn4+=2Fe3++Sn2+的△r G mθ为(D)kJ/mol。 A. -268.7 B. -177.8 C. -119.9 D. 119.9 5.判断在酸性溶液中下列等浓度的离子哪些能共存(D) A Sn2+和Hg2+ B. SO32—和MnO4— C. Sn4+和Fe D. Fe2+和Sn4+ 已知Eθ(Hg2+/Hg)=0.851V,Eθ(Sn4+/Sn2+)=0.15V ,Eθ(MnO4—/Mn2+)=1.49V Eθ(SO42—/H2SO3)=1.29V ,Eθ(Fe2+/Fe)= —0.44V 6.已知下列反应在标准状态下逆向自发进行 Sn4++Cu = Sn2++Cu2+ Eθ(Cu2+/Cu)=(1) , Eθ(Sn4+/Sn2+)=(2) 则有(C) A. (1) = (2) B. (1)<(2) C. (1)>(2) D. 都不对 二、填空题 1.将下列方程式配平 3PbO2 + 2 Cr3+ + ____H2O___ =1Cr2O72—+ 3Pb2+ + __2H+___ (酸性介质) 2MnO2 + 3 H2O2 +__2OH-___ =2MnO4—+ ___4H2O______ (碱性介质)2.现有三种氧化剂Cr2O72—,H2O2,Fe3+,若要使Cl—、Br—、I—混合溶液中的I—氧化为I2,而Br-和Cl-都不发生变化,选用Fe3+最合适。(EθCl2/Cl-=1.36V, EθBr2/Br-=1.065V, EθI2/I-=0.535V) 3.把氧化还原反应Fe2++Ag+=Fe3++Ag设计为原电池,则正极反应为Ag++ e = Ag,负极反应为Fe3++e= Fe2+ ,原电池符号为Pt︱Fe3+(c1),Fe2+(c2)‖Ag+(c3)︱Ag。 4.在Mn++n e=M(s)电极反应中,当加入Mn+的沉淀剂时,可使其电极电势值降低,如增加M的量,则电极电势不变 5.已知EθAg+/Ag=0.800V, K sp=1.6×10—10则Eθ(AgCl/Ag)= 0.222V。 6.已知电极反应Cu2++2e=Cu的Eo为0.347V,则电极反应2Cu - 4e =2Cu2+的Eθ值为0.347V 。7.用氧化数法配平下列氧化还原反应。 (1)K2Cr2O7+H2S+H2SO4K2SO4+Cr2(SO4)3+S+H2O K2Cr2O7+3H2S+4H2SO4 =K2SO4+Cr2(SO4)3+3S+7H2O
电化学原理与方法课程中下半学期课程复习题 (1)剖析
1请你简要论述一下,电化学研究方法中,暂态测量技术有哪些?以及暂态研究技术的应用有哪些? 暂态测量技术有哪些? 暂态测量方法的种类 ①按极化或控制的幅度分( 幅度:电极极化的幅度,界面电位变化量) a. 大幅度暂态测量(研究电极过程) |Δφ|>10 mV ( 大幅度) b. 小幅度暂态测量(用于测定参数Rr、RL、C d) |Δφ|<10 mV(小幅度) ②按控制方式分: a. 控制电流法暂态测量 b. 控制电位法暂态测量 控电流法:单电流阶跃;断电流;方波电流;双脉冲电流 控电位法:阶跃法、方波电位法等;线性扫描(单程线性扫描,连续三角波扫描);脉冲电位(阶梯伏安,常规脉冲,差分脉冲,方波伏安) [从电极极化开始到各个子过程(电化学反应过程、双电层充电过程、传质过程和离子导电过程)做出响应并进入稳态过程所经历的不稳定的,变化的“过渡阶段”,称为暂态.] [电化学暂态测试技术也称为电化学微扰测试技术,即用指定的小幅度电流或电压讯号加到研究电极上,使电极体系发生微弱的扰动,同时测量电极参数的响应来研究电极反应参数] 暂态研究技术的应用? 暂态技术提供了比稳态技术更多的信息,用来研究电极过程动力学,测定电极反应动力学参数和确定电极反应机理,而且还可将测量迁越反应速率常数的上限提高2~3个数量级,有可能研究大量快速的电化学反应。暂态技术对于研究中间态和吸附态存在的电极反应也特别有利。暂态技术中测得的一些参量,例如双电层电容、欧姆电阻、由迁越反应速率常数决定的迁越电阻等,在化学电源、电镀、腐蚀等领域也有指导意义。 2.请你谈谈电化学测量中要获得电化学信号需要哪些电极以及设备,它们分别的作用是什么? 一、需要①参比电极:参比电极的性能直接影响着电极电势的测量或控制的稳定性。 ②盐桥:当被测电极体系的溶液与参比电极的溶液不同时,常用盐桥把研究电极和参比电极连接起来。盐桥的作用主要有两个,一个是减小接界电势,二是减少研究、参比溶液之间的相互污染。
电化学原理知识点
电化学原理 第一章 绪论 两类导体: 第一类导体:凡是依靠物体内部自由电子的定向运动而导电的物体,即载流子为自由电子(或空穴)的导体,叫做电子导体,也称第一类导体。 第二类导体:凡是依靠物体内的离子运动而导电的导体叫做离子导体,也称第二类导体。 三个电化学体系: 原电池:由外电源提供电能,使电流通过电极,在电极上发生电极反应的装置。 电解池:将电能转化为化学能的电化学体系叫电解电池或电解池。 腐蚀电池:只能导致金属材料破坏而不能对外界做有用功的短路原电池。 阳极:发生氧化反应的电极 原电池(-)电解池(+) 阴极:发生还原反应的电极 原电池(+)电解池(-) 电解质分类: 定义:溶于溶剂或熔化时形成离子,从而具有导电能力的物质。 分类: 1.弱电解质与强电解质—根据电离程度 2.缔合式与非缔合式—根据离子在溶液中存在的形态 3.可能电解质与真实电解质—根据键合类型 水化数:水化膜中包含的水分子数。 水化膜:离子与水分子相互作用改变了定向取向的水分子性质,受这种相互作用的水分子层称为水化膜。可分为原水化膜与二级水化膜。 活度与活度系数: 活度:即“有效浓度”。 活度系数:活度与浓度的比值,反映了粒子间相互作用所引起的真实溶液与理想溶液的偏差。 规定:活度等于1的状态为标准态。对于固态、液态物质和溶剂,这一标准态就是它们的纯物质状态,即规定纯物质的活度等于1。 离子强度I : 离子强度定律:在稀溶液范围内,电解质活度与离子强度之间的关系为: 注:上式当溶液浓度小于0.01mol ·dm-3 时才有效。 电导:量度导体导电能力大小的物理量,其值为电阻的倒数。 符号为G ,单位为S ( 1S =1/Ω)。 影响溶液电导的主要因素:(1)离子数量;(2)离子运动速度。 当量电导(率):在两个相距为单位长度的平行板电极之间,放置含有1 克当量电解质的溶液时,溶液所具有的电导称为当量电导,单位为Ω-1 ·cm2·eq-1。 与 K 的关系: 与 的关系: 当λ趋于一个极限值时,称为无限稀释溶液当量电导或极限当量电导。 离子独立移动定律:当溶液无限稀释时,可以完全忽略离子间的相互作用,此时离子的运动 i i i x αγ=∑ =2 2 1i i z m I I A ?-=±γlog L A G κ= KV =λN c N c k 1000=λ- ++=000λλλ
电化学原理
第一章 绪论 两类导体: 第一类导体:凡是依靠物体内部自由电子的定向运动而导电的物体,即载流子为自由电子(或空穴)的导体,叫做电子导体,也称第一类导体。 第二类导体:凡是依靠物体内的离子运动而导电的导体叫做离子导体,也称第二类导体。 三个电化学体系: 原电池:由外电源提供电能,使电流通过电极,在电极上发生电极反应的装置。 电解池:将电能转化为化学能的电化学体系叫电解电池或电解池。 腐蚀电池:只能导致金属材料破坏而不能对外界做有用功的短路原电池。 阳极:发生氧化反应的电极 原电池(-)电解池(+) 阴极:发生还原反应的电极 原电池(+)电解池(-) 电解质分类: 定义:溶于溶剂或熔化时形成离子,从而具有导电能力的物质 分类: ? 弱电解质与强电解质—根据电离程度 ? 缔合式与非缔合式—根据离子在溶液中存在的形态 ? 可能电解质与真实电解质—根据键合类型 水化数:水化膜中包含的水分子数。 水化膜:离子与水分子相互作用改变了定向取向的水分子性质,受这种相互作用的水分子层称为水化膜。可分为原水化膜与二级水化膜。 活度与活度系数: 活度:即“有效浓度”. 活度系数:活度与浓度的比值,反映了粒子间相互作用所引起的真实溶液与理想溶液的偏差。 规定:活度等于1的状态为标准态。对于固态、液态物质和溶剂,这一标准态就是它们的纯物质状态,即规定纯物质的活度等于1。 离子强度I : 离子强度定律:在稀溶液范围内,电解质活度与离子强度之间的关系为: 注:上式当溶液浓度小于0.01mol ·dm -3 时才有效。 电导∶量度导体导电能力大小的物理量,其值为电阻的倒数。 符号为G ,单位为S ( 1S =1/Ω)。 i i i x αγ=∑= 2 2 1i i z m I I A ?-=±γlog L A G κ=
电化学原理思考题答案-北航李荻版
2、为什么不能测出电极得绝对电位?我们平常所用得电极电位就是怎么得到得? 答:电极电位就是两类导体界面所形成得相间电位,相间电位中得内电位就是无法直接测量 得,故无法直接测出电极得绝对电位,我们平常所用得电极电位都就是相对电极电位。 不对,虽然有电 位差,但就是没 有电流通过,所 以不能转化为 电能。
17、描述腐蚀原电池得特点所在。 ①阴、阳极区肉眼可分或不可分,或交替发生; ②体系不稳定稳定,腐蚀过程就是自发反应; ③只要介质中存在氧化剂(去极化剂),能获得电子使金属氧化,腐蚀就可发生; ④腐蚀得二次产物对腐蚀影响很大; ⑤电化学腐蚀离不开金属/电解质界面电迁移,电子由低电位金属或地区传荷到电位高得金属或地区,再转移给氧化剂; ⑥腐蚀电池包括阴极、阳极、电解质溶液与电路四部分,缺一不可; ⑦阴极、阳极反应相对独立,但又必须耦合,形成腐蚀电池; ⑧ia=ic , 无净电荷积累; ⑨腐蚀电池不对外作功,只导致金属腐蚀破坏得短路原电池.原电池与电解池
1.原电池与电解池得比较: 4.电解、电离与电镀得区别
对于我们所讨论得某一反应来说,zF为常数,故J与vr成正比。这就就是说,在电化学中总就是习惯于用电流密度来表示反应速度.由于在稳态下接续进行得各步骤速度都一样,所以在讨论液相传质等步骤时,也可用电流密度来表示它们得反应速度。因此,在电化学中实际上已经将电流密度变成反应速度得同义语了。 己知电极反应在25℃时得反应速度为0.1 A/cm2.根据各单元步骤活化能计算出电子转移步骤速度为1、04 X 10-2mol/m2s,扩散步骤速度为0、1 mol/m2s。试判断该温度下得控制步骤.若这一控制步骤得活化能降低了12kJ/mol,会不会出现新得控制步骤?[ 解〕因为电极反应速度可用电流密度表示,即J=nFv,所以对电子转移步骤,其反应速度可表示为j电子=nFv电子。已知n=1,故j电子=1x96500 x 1、 04 x10-2≈0、1A/cm2同理J扩散=nFv扩散 =1x96500x0、1=0、965A/cm2已知整个电极反应速度为0、 1 A/cm2,所以可判断速度控制步骤就是电子转移步骤。若电子转移步骤活化能降低12 kJ/mol,则根据v=K c exp(—W/RT) 式中,W为活化能,c为反应物浓度。设原来速度为v1。活化能降低后得速度为 v2,则v1=K c exp (—W1/RT) V2=K c exp(—W2/RT)=V1 exp(△W/RT)=1、04x10-2 exp(12x103/8、31x298)=1、32 mol/m2s 可见J’电子>>J扩散,速度控制步骤将发生变化。 4、电化学反应得基本动力学参数有哪些?说明它们得物理意义? 通常认为传递系数(α与β)、交换电流密度(j0 )与电极反应速度常数(K)为基本得动力学参数.①传递系数(α与β) 即表示电极电位对还原反应活化能与氧化反应活化能影响得程度,又称为对称系数;②交换电流密度( j0 ) 交换电流密
最新电化学原理思考题答案
电化学原理思考题答案 (注:我只做了老师要求做的) 第三章 1.自发形成的双电层和强制形成的双电层在性质和结构上有无不同?为什么? 2.理想极化电极和不极化电极有什么区别?它们在电化学中有什么重要用途? 答:当电极反应速率为0,电流全部用于改变双电层的电极体系的电极称为理想极化电极,可用于界面结构和性质的研究。理想不极化电极是指当电极反应速率和电子反应速率相等时,极化作用和去极化作用平衡,无极化现象,通向界面的电流全部用于电化学反应,可用作参比电极。 3.什么是电毛细现象?为什么电毛细曲线是具有极大值的抛物线形状? 答:电毛细现象是指界面张力随电极电位变化的现象。溶液界面存在双电层,剩余电荷无论带正电还是负电,同性电荷间相互排斥,使界面扩大,而界面张力力图使界面缩小,两者作用效果相反,因此带电界面的张力比不带电时小,且电荷密度越大,界面张力越小,因此电毛细曲线是具有极大值的抛物线形状。 4.标准氢电极的表面剩余电荷是否为零?用什么办法能确定其表面带电状况? 答:不一定,标准氢电极电位为0指的是氢标电位,是人为规定的,电极表面剩余电荷密度为0时的电位指的是零电荷电位,其数值并不一定为0;因为形成相间电位差的原因除了离子 双电层外,还有吸附双电层\偶极子双电层\金属表面电位。可通过零电荷电位判断电极表面带电状况,测定氢标电极的零电荷电位,若小于0则电极带正电,反之带负电。 5.你能根据电毛细曲线的基本规律分析气泡在电极上的附着力与电极电位有什么关系吗?为什么有这种关系?(提示:液体对电极表面的润湿性越高,气体在电极表面的附着力就越小。) 6.为什么在微分电容曲线中,当电极电位绝对值较大时,会出现“平台”? 7.双电层的电容为什么会随电极电位变化?试根据双电层结构的物理模型和数学模型型以解释。 8.双电层的积分电容和微分电容有什么区别和联系? 9.试述交流电桥法测量微分电容曲线的原理。 10.影响双电层结构的主要因素是什么?为什么? 答:静电作用和热运动。静电作用使符号相反的剩余电荷相互靠近,贴于电极表面排列,热运动使荷电粒子外散,在这两种作用下界面层由紧密层和分散层组成。 11.什么叫ψ1 电位?能否说ψ1 电位的大小只取决于电解质总浓度而与电解质本性无关?ψ1 电位的符号是否总是与双电层总电位的符号一致?为什么? 答:距离电极表面d处的电位叫ψ1电位。不能,因为不同的紧密层d的大小不同,而紧密层的厚度显然与电解质本性有关,所以不能说ψ1 电位的大小只取决于电解质总浓度而与电解质本性无关。当发生超载吸附时ψ1 电位的符号与双电层总电位的符号不一致。 12.试述双电层方程式的推导思路。推导的结果说明了什么问题? 13.如何通过微分电容曲线和电毛细曲线的分析来判断不同电位下的双电层结构? 答: 14.比较用微分电容法和电毛细曲线法求解电极表面剩余电荷密度的优缺点。 15.什么是特性吸附?哪些类型的物质具有特性吸附的能力? 答:溶液中的各种粒子还可能因非静电作用力而发生吸附称为特性吸附。大部分无机阴离子,部分无机阳离子以及表面活性有机分子可发生特性吸附。 16.用什么方法可以判断有无特性吸附及估计吸附量的大小?为什么? 17.试根据微分电容曲线和电毛细曲线的变化,说明有机分子的特性吸附有哪些特点?
电化学原理知识点
电化学原理第一章绪论 两类导体: 第一类导体:凡是依靠物体内部自由电子的定向运动而导电的物体,即载流子为自由电子(或空穴)的导体,叫做电子导体,也称第一类导体。 第二类导体:凡是依靠物体内的离子运动而导电的导体叫做离子导体,也称第二类导体。 三个电化学体系: 原电池:由外电源提供电能,使电流通过电极,在电极上发生电极反应的装置。电解池:将电能转化为化学能的电化学体系叫电解电池或电解池。 腐蚀电池:只能导致金属材料破坏而不能对外界做有用功的短路原电池。 阳极:发生氧化反应的电极原电池(-)电解池(+) 阴极:发生还原反应的电极原电池(+)电解池(-) 电解质分类: 定义:溶于溶剂或熔化时形成离子,从而具有导电能力的物质。 分类: 1.弱电解质与强电解质—根据电离程度 2.缔合式与非缔合式—根据离子在溶液中存在的形态 3.可能电解质与真实电解质—根据键合类型 水化数:水化膜中包含的水分子数。 水化膜:离子与水分子相互作用改变了定向取向的水分子性质,受这种相互作用的水分子层称为水化膜。可分为原水化膜与二级水化膜。
活度与活度系数: 活度:即“有效浓度”。 活度系数:活度与浓度的比值,反映了粒子间相互作用所引起的真实溶液与理 想溶液的偏差。 规定:活度等于1的状态为标准态。对于固态、液态物质和溶剂,这一标准态就是它们的纯物质状态,即规定纯物质的活度等于1。 离子强度I : 离子强度定律:在稀溶液范围内,电解质活度与离子强度之间的关系为: 注:上式当溶液浓度小于·dm-3 时才有效。 电导:量度导体导电能力大小的物理量,其值为电阻的倒数。 符号为G ,单位 为S ( 1S =1/Ω)。 影响溶液电导的主要因素:(1)离子数量;(2)离子运动速度。 当量电导(率):在两个相距为单位长度的平行板电极之间,放置含有1 克当量电解质的溶液时,溶液所具有的电导称为当量电导,单位为Ω-1 ·cm2·eq-1。 与 K 的关系: 与 的关系: 当λ趋于一个极限值时,称为无限稀释溶液当量电导或极限当量电导。 离子独立移动定律:当溶液无限稀释时,可以完全忽略离子间的相互作用,此 时离子的运动是独立的,这时电解质溶液的当量电导等于电解质全部电离后所产生的离子当量电导之和: 同一离子在任何无限稀溶液中极限当量电导值不变! 离子淌度:单位场强(V/cm )下的离子迁移速度,又称离子绝对运动速度。 i i i x αγ=∑= 22 1 i i z m I I A ?-=±γlog L A G κ= KV =λN c N c k 1000 =λ-++=000λλλ
电化学原理试题
电化学原理 一、填空题。(每空2分,共30分) 1. 电化学研究对象包括三部分:_____________,________________及_______________________。 2. 液相传质的三种方式为:_____________,______________和_____________。 3. 离子淌度反映出离子在______________推动下的运动特征。 4. 金属与溶液界面电位差一般由______________电位差、____________电位差和__________电位差组成。 5. 金属电化学防腐有___________、___________、___________等三种方式。 6. 电池放电时,阳极是正极还是负极?_____________。 7. 若某一电极过程有15J0< J< ,则其速度控制步骤为_____________步骤。 二、回答下列问题。(每题10分,共40分) 1. “除电荷传递步骤外,电极过程的其他步骤不涉及电子转移,所以不能用电流密度来表示它们的速度。” 这种说法对吗?为什么? 2. 在不同金属上发生氢离子还原时,为什么可根据Tafel公式中的a值将它们分成高、中、低过电位金属? 3.?电化学极化的电极过程速度控制步骤是什么步骤?浓度极化的电极过程速度控制步骤是什么步骤? 4. 为什么电极电位的改变会影响电极反应的速度和方向? 三、计算题(10分) 用H2SO4的水——乙酸溶液为电解液,测定铂电极(阳极)上氧的过电势,得出下表结果:J /10-310-25×10-210-1 η/V 求Tafel常数a和b。 四、分析在金属电镀过程中阴、阳极上发生反应(包括副反应)的特点及电位变化特点。(10分) 五、测量动力学参数可采用经典法和暂态法,二者各有何特点。(10分) 电化学原理试题B(答案) 二、填空题。(每空2分,共30分) 1. 电子导体,离子导体,二者形成的带电界面性质 2. 对流,扩散,电迁移
电化学原理练习题及答案
电化学原理练习题及答案 1、在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是() A.原电池正极和电解池阳极所发生的反应 B.原电池正极和电解池阴极所发生的反应 C.原电池负极和电解池阳极所发生的反应 D.原电池负极和电解池阴极所发生的反应 2、下列关于铜电极的叙述正确的是() A.铜锌原电池中铜是正极 B.用电解法精炼粗铜作阴极 C.在镀件上电镀铜时可用金属铜作阳极 D.电解稀硫酸制H2、O2时铜作阳极 3.用惰性电极实现电解,下列说法正确的是( ) A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2 D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1 4.(2004年广东,11)pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是() A.NaOH B.H2SO4 C.AgNO3 D.Na2SO4 5.(2004年天津理综,12)图11-13为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正 ..确.的是 图11-13 A.a电极是负极 B.b电极的电极反应为:4OH--4e-====2H2O+O2↑ C.氢氧燃料电池是一种具有应用前景的绿色电源 D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 6.用惰性电极实现电解,下列说法正确的是 A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2 D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1 7.(2004年江苏,16)碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l)====Zn(OH)2(s)+Mn2O3(s) 下列说法错误 ..的是( ) A.电池工作时,锌失去电子
电化学原理
可逆体系的循环伏安研究 1 实验目的 1)掌握循环伏安法研究电极过程的基本原理 2)学习使用CHI660电化学综合分析仪 3)测定K3Fe(CN)6体系在不同扫描速率时的循环伏安图 2 实验原理 1)循环伏安法概述: 循环伏安法(CyclicVoltammetry)的基本原理是:根据研究体系的性质,选择电位扫描范围和扫描速率,从选定的起始电位开始扫描后,研究电极的电位按指定的方向和速率随时间线性变化,完成所确定的电位扫描范围到达终止电位后,会自动以同样的扫描速率返回到起始电位。在电位进行扫描的同时,同步测量研究电极的电流响应,所获得的电流-电位曲线称为循环伏安曲线或循环伏安扫描图。通过对循环伏安扫描图进行定性和定量分析,可以确定电极上进行的电极过程的热力学可逆程度、得失电子数、是否伴随耦合化学反应及电极过程动力学参数,从而拟定或推断电极上所进行的电化学过程的机理。 循环伏安法是进行电化学和电分析化学研究的最基本和最常用的方法,1922年由Jaroslav Heyrovsky创立的以滴汞电极作为工作电极的极谱分析法(Polarography),可以认为是伏安研究方法的早期形式,其对电化学研究领域的杰出贡献,Heyrovsky在1959年获得诺贝尔化学奖。随着固体电极,修饰电极的广泛使用和电子技术的发展,循环伏安法的测试范围和测试技术、数据采集和处理等方面显著改善和提高,从而使电化学和电分析化学方法更普遍地应用于化学化工、生命科学、材料科学及环境和能源等领域。 2)循环伏安扫描图: 循环伏安法研究体系是由工作电极、参比电极、辅助电极构成的三电极系统,工作电极和参比电极组成电位测量,工作电极和辅助电极组成的回路测量电流。工作电极可选用固态或液态电极,如:铂、金、玻璃石墨电极或悬汞、汞膜电极。常用的参比电极有:饱和甘汞电极(SCE)、银-氯化银电极,因此,循环伏安曲线中的电位值都是相对于参比电极而言。辅助电极可选用固态的惰性电极,如:铂丝或铂片电极、玻碳电极等。电解池中的电解液包括:氧化还原体系(常用的浓度范围:mmol/L)、支持电解质(浓度范围:mol/L)。循环伏安测定方法是:将CHI660电化学综合分析仪与研究体系连接,选定电位扫描范围E1~E2和扫描速率υ,从起始电位E1开始扫描,电位按选定的扫描速率呈线性变化从E1到达E2,然后连续反方向再扫描从E2回到E1,如图C17.1所示,电位随时间的变化呈现的是等腰三角波信号。 在扫描电位范围内,若在某一电位值时出现电流峰,说明在此电位时发生了电极反应。若在正向扫描时电极反应的产物是足够稳定的,且能在电极表面发生电极反应,那么在返回扫描时将出现于正向电流峰相对应的逆向电流峰。典型的循环伏安曲线如图C17.2所示,i pc 和i pa分别表示阴极峰值电流和阳极峰值电流,对应的阴极峰值电位与阳极峰值电位分别为E pc和E pa。(p表示峰值,a表示阳极,c表示阴极。)
电化学原理试题A答案
电化学原理试题A(答案) 考试形式:闭卷答题时间: 120 分钟本卷面成绩占课程成绩 100% (所有答案必须写在答题纸上、标清题号) 一、名词解释(每题3分,共15分) 1. 极化:有电流通过电化学装置时,电极电势偏离平衡电势的现象。 2. 交换电流密度:在平衡电势下,外电流密度为0,此时电极上正逆反应的绝对电流密度相等,都等于交换电流密度。 3. 4. 稳态扩散:电极反应有溶液中粒子参与时,该粒子会沿着某一方向产生一定的净流量,当此过程中溶液内各点浓度均保持恒定,不随时间而变化时,称为稳态扩散。 5. 零电荷电势:电极表面剩余电荷浓度为零时所对应的电极电势。 二、比较下列各组概念,说明其区别与联系。(每题5分,共15分) 1.阴极阳极 答:电化学装置中有电流通过时,得到电子,发生还原反应的电极是阴极;失去电子,发生氧化反应的电极是阳极。一个电极电势负移就是阴极,电势正移就是阳极。 2.双电层扩散层 答:电极表面存在电势梯度的液层是双电层;双电层外存在浓度梯度的液层是扩散层。二者都是电极表面附近的液层,但双电层内是反应区,扩散层内是液相传质区。 3.理想极化电极理想不极化电极 答:电极电势可以极化到任意值的电极是理想极化电极;电极电势只能维持平衡电势的电极是理想不极化电极。二者都是一种理论近似,实际中都会有偏差,但有近似符合的实际电极。 三、回答下列问题。(每题8分,共40分) 1.“当电极处于零电荷电位时,表明电极的电极电位为零。”这种说法对吗?为什么? 答:不对。电极表面剩余电荷浓度为零并不是电势为零。 2.“恒电流极化时,反应物粒子在电极表面的浓度随时间不断下降,当其降到零时,因无反应粒子,
电化学原理思考题答案11267
(注:我只做了老师要求做地) 第三章 .自发形成地双电层和强制形成地双电层在性质和结构上有无不同?为什么? .理想极化电极和不极化电极有什么区别?它们在中有什么重要用途?文档来自于网络搜索答:当电极反应速率为,电流全部用于改变双电层地电极体系地电极称为理想极化电极,可用于界面结构和性质地研究.理想不极化电极是指当电极反应速率和电子反应速率相等时,极化作用和去极化作用平衡,无极化现象,通向界面地电流全部用于电化学反应,可用作参比电极. .什么是电毛细现象?为什么电毛细曲线是具有极大值地抛物线形状?文档来自于网络搜索答:电毛细现象是指界面张力随电极电位变化地现象.溶液界面存在双电层,剩余电荷无论带正电还是负电,同性电荷间相互排斥,使界面扩大,而界面张力力图使界面缩小,两者作用效果相反,因此带电界面地张力比不带电时小,且电荷密度越大,界面张力越小,因此电毛细曲线是具有极大值地抛物线形状.文档来自于网络搜索 .标准氢地表面剩余电荷是否为零?用什么办法能确定其表面带电状况?文档来自于网络搜索 答:不一定,标准氢电极电位为指地是氢标电位,是人为规定地,电极表面剩余电荷密度为时地电位指地是零电荷电位,其数值并不一定为;因为形成相间电位差地原因除了离子双电层外,还有吸附双电层\偶极子双电层\金属表面电位.可通过零电荷电位判断电极表面带电状况,测定氢标电极地零电荷电位,若小于则电极带正电,反之带负电.文档来自于网络搜索 .你能根据电毛细曲线地基本规律分析气泡在电极上地附着力与电极电位有什么关系吗?为什么有这种关系?(提示:液体对电极表面地润湿性越高,气体在电极表面地附着力就越小.)文档来自于网络搜索 .为什么在微分曲线中,当电极电位绝对值较大时,会出现“平台”?文档来自于网络搜索.双电层地电容为什么会随电极电位变化?试根据双电层结构地物理和数学模型型以解释. 文档来自于网络搜索 .双电层地积分电容和微分电容有什么区别和联系? .试述交流电桥法测量微分电容曲线地原理. .影响双电层结构地主要因素是什么?为什么? 答:静电作用和热运动.静电作用使符号相反地剩余电荷相互靠近,贴于电极表面排列,热运动使荷电粒子外散,在这两种作用下界面层由紧密层和分散层组成.文档来自于网络搜索.什么叫ψ 电位?能否说ψ 电位地大小只取决于总浓度而与电解质本性无关?ψ 电位地符号是否总是与双电层总电位地符号一致?为什么?文档来自于网络搜索 答:距离电极表面处地电位叫ψ电位.不能,因为不同地紧密层地大小不同,而紧密层地厚度显然与电解质本性有关,所以不能说ψ 电位地大小只取决于总浓度而与电解质本性无关.当发生超载吸附时ψ 电位地符号与双电层总电位地符号不一致.文档来自于网络搜索 .试述双电层方程式地推导思路.推导地结果说明了什么问题? .如何通过微分电容曲线和电毛细曲线地分析来判断不同电位下地双电层结构? 答: .比较用微分电容法和电毛细曲线法求解表面剩余电荷地优缺点. 文档来自于网络搜索 .什么是特性吸附?哪些类型地物质具有特性吸附地能力? 答:溶液中地各种粒子还可能因非静电作用力而发生吸附称为特性吸附.大部分无机阴离子,部分无机阳离子以及表面活性有机分子可发生特性吸附.文档来自于网络搜索 .用什么方法可以判断有无特性吸附及估计吸附量地大小?为什么? .试根据微分电容曲线和电毛细曲线地变化,说明有机分子地特性吸附有哪些特点?
电化学原理及其应用(习题及答案)
电化学原理及其应用 (习题及答案) https://www.wendangku.net/doc/6512892608.html,work Information Technology Company.2020YEAR
第六章电化学原理及其应用 一、选择题 1.下列电极反应中,溶液中的pH值升高,其氧化态的氧化性减小的是( C ) A. Br2+2e = 2Br- B. Cl2+2e=2Cl— C. MnO4—+5e+8H+=2Mn2++4H2O D. Zn2++2e=Zn 2.已知H2O2在酸性介质中的电势图为 O2 0.67V H2O2 1.77V H2O,在碱性介质中的电势图为O2-0.08V H2O2 0.87V H2O,说明H2O2的歧化反应(C) A.只在酸性介质中发生 B.只在碱性介质中发生 C.无论在酸、碱性介质中都发生D.与反应方程式的书写有关 3.与下列原电池电动势无关的因素是 Zn | Zn2+‖H+,H2 | Pt (B) A. Zn2+的浓度 B. Zn电极板的面积 C.H+的浓度 D.温度 4.298K时,已知Eθ(Fe3+/Fe)=0.771V,Eθ(Sn4+/Sn2+)=0.150V,则反应 2Fe2++Sn4+=2Fe3++Sn2+的△r G mθ为(D)kJ/mol。 A. -268.7 B. -177.8 C. -119.9 D. 119.9 5.判断在酸性溶液中下列等浓度的离子哪些能共存(D) A Sn2+和Hg2+ B. SO32—和MnO4— C. Sn4+和Fe D. Fe2+和Sn4+ 已知Eθ(Hg2+/Hg)=0.851V,Eθ(Sn4+/Sn2+)=0.15V ,Eθ(MnO4—/Mn2+)=1.49V Eθ(SO42—/H2SO3)=1.29V ,Eθ(Fe2+/Fe)= —0.44V 6.已知下列反应在标准状态下逆向自发进行 Sn4++Cu = Sn2++Cu2+
电化学原理知识点(完整资料).doc
【最新整理,下载后即可编辑】 电化学原理 第一章 绪论 两类导体: 第一类导体:凡是依靠物体内部自由电子的定向运动而导电的物体,即载流子为自由电子(或空穴)的导体,叫做电子导体,也称第一类导体。 第二类导体:凡是依靠物体内的离子运动而导电的导体叫做离子导体,也称第二类导体。 三个电化学体系: 原电池:由外电源提供电能,使电流通过电极,在电极上发生电极反应的装置。 电解池:将电能转化为化学能的电化学体系叫电解电池或电解池。 腐蚀电池:只能导致金属材料破坏而不能对外界做有用功的短路原电池。 阳极:发生氧化反应的电极 原电池(-)电解池(+) 阴极:发生还原反应的电极 原电池(+)电解池(-) 电解质分类: 定义:溶于溶剂或熔化时形成离子,从而具有导电能力的物质。 分类: 1.弱电解质与强电解质—根据电离程度 2.缔合式与非缔合式—根据离子在溶液中存在的形态 3.可能电解质与真实电解质—根据键合类型 水化数:水化膜中包含的水分子数。 水化膜:离子与水分子相互作用改变了定向取向的水分子性质,受这种相互作用的水分子层称为水化膜。可分为原水化膜与二级水化膜。 活度与活度系数: 活度:即“有效浓度”。 活度系数:活度与浓度的比值,反映了粒子间相互作用所引起的 真实溶液与理想溶液的偏差。 i i i x αγ=
规定:活度等于1的状态为标准态。对于固态、液态物质和溶剂,这一标准态就是它们的纯物质状态,即规定纯物质的活度等于1。 离子强度I : 离子强度定律:在稀溶液范围内,电解质活度与离子强度之间的 关系为: 注:上式当溶液浓度小于0.01mol ·dm-3 时才有效。 电导:量度导体导电能力大小的物理量,其值为电阻的倒数。 符 号为G ,单位为S ( 1S =1/Ω)。 影响溶液电导的主要因素:(1)离子数量;(2)离子运动速度。 当量电导(率):在两个相距为单位长度的平行板电极之间,放置含有1 克当量电解质的溶液时,溶液所具有的电导称为当量电导,单位为Ω-1 ·cm2·eq-1。 与 K 的关系: 与 的关系: 当λ趋于一个极限值时,称为无限稀释溶液当量电导或极限当量电导。 离子独立移动定律:当溶液无限稀释时,可以完全忽略离子间的 相互作用,此时离子的运动是独立的,这时电解质溶液的当量电导等于电解质全部电离后所产生的离子当量电导之和: 同一离子在任何无限稀溶液中极限当量电导值不变! 离子淌度:单位场强(V/cm )下的离子迁移速度,又称离子绝对运动速度。 离子迁移数:某种离子迁移的电量在溶液中各种离子迁移的总电量中所占的百分数。 ∑= 2 2 1i i z m I I A ?-=±γlog L A G κ=KV =λN c N c k 1000=λ- ++=000λλλE V U + +=E V U - -=
{高中试卷}高三化学一轮复习:电化学原理及其应用[仅供参考]
20XX年高中测试 高 中 试 题 试 卷 科目: 年级: 考点:
监考老师: 日期: 电化学原理及其应用 1.家蝇的雌性信息素可用芥酸(来自菜籽油)与羧酸X在浓NaOH溶液中进行阳极氧化得到。电解总反应式为: 则下列说法正确的是( ) A.X为C2H5COOH 3+6H+B.电解的阳极反应式为:C21H41COOH+X-2e-+2H2O―→C23H46+2CO2- C.电解过程中,每转移a mol电子,则生成0.5a mol雌性信息素 D.阴极的还原产物为H2和OH- 解析:A项根据原子守恒可判断X为C2H5COOH;B项由于电解质溶液为浓NaOH,因此阳极反应 3+4H2O;C项根据电解总反应可知每生成1 式应为C21H41COOH+X-2e-+60H-―→C23H46+2CO2- mol雌性信息素转移2 mol电子,则C项正确;D项阴极的还原产物为H2,OH-并非氧化还原产物. 答案:AC 2.下列关于铜电极的叙述正确的是( ) A.铜锌原电池中铜是负极 B.用电解法精炼粗铜时,粗铜作阴极 C.在镀件上电镀铜时可用金属铜做阳极 D.电解稀硫酸制H2和O2时铜做阳极 解析:铜锌原电池中锌活泼,锌做负极;电解精炼铜时,粗铜中的铜失去电子,做阳极;电
镀铜时,应选用铜片做阳极,镀件做阴极,含有铜离子的溶液做电镀液。电解稀硫酸时,铜做阳极,失电子的是铜而不是溶液中的OH-,因而得不到氧气。 答案:C 3.普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一特点,科学家发明了电动势(E)法测水泥初凝时间,此法的原理如图所示,反应的总方程式为:2Cu+Ag2O===Cu2O+2Ag。 下列有关说法不正确的是( ) A.工业上制备普通水泥的主要原料是黏土和石灰石 B.测量原理装置图中,Ag2O/Ag极发生氧化反应 C.负极的电极反应式为:2Cu+2OH--2e-===Cu2O+H2O D.在水泥固化过程中,由于自由水分子的减少,溶液中各离子浓度的变化导致电动势变化解析:A项工业上制备普通水泥的主要原料正确;B项测量原理装置图中,Ag2O/Ag极发生还原反应;C项负极材料Cu失电子,该电极反应式正确;D项在溶液中通过离子移动来传递电荷,因此各离子浓度的变化导致电动势变化。 答案:B 4. LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4 +Li 放电 充电 LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解 质。 下列有关LiFePO4电池说法正确的是( ) A.可加入硫酸以提高电解质的导电性B.放电时电池内部Li+向负极移动 C.充电过程中,电池正极材料的质量减少
电化学原理思考题答案
第三章 1.自发形成的双电层和强制形成的双电层在性质和结构上有无不同?为什么? 2.理想极化电极和不极化电极有什么区别?它们在电化学中有什么重要用途?答:当电极反应速率为0,电流全部用于改变双电层的电极体系的电极称为理想极化电极,可用于界面结构和性质的研究。理想不极化电极是指当电极反应速率和电子反应速率相等时,极化作用和去极化作用平衡,无极化现象,通向界面的电流全部用于电化学反应,可用作参比电极。 3.什么是电毛细现象?为什么电毛细曲线是具有极大值的抛物线形状? 答:电毛细现象是指界面张力随电极电位变化的现象。溶液界面存在双电层,剩余电荷无论带正电还是负电,同性电荷间相互排斥,使界面扩大,而界面张力力图使界面缩小,两者作用效果相反,因此带电界面的张力比不带电时小,且电荷密度越大,界面张力越小,因此电毛细曲线是具有极大值的抛物线形状。 4.标准氢电极的表面剩余电荷是否为零?用什么办法能确定其表面带电状况?答:不一定,标准氢电极电位为0指的是氢标电位,是人为规定的,电极表面剩余电荷密度为0时的电位指的是零电荷电位,其数值并不一定为0;因为形成相间电位差的原因除了离子双电层外,还有吸附双电层\ 偶极子双电层\金属表面电位。可通过零电荷电位判断电极表面带电状况,测定氢标电极的零电荷电位,若小于0则电极带正电,反之带负电。 5.你能根据电毛细曲线的基本规律分析气泡在电极上的附着力与电极电位有什么关系吗?为什么有这种关系?(提示:液体对电极表面的润湿性越高,气体在电极表面的附着力就越小。) 6.为什么在微分电容曲线中,当电极电位绝对值较大时,会出现“平台”? 7.双电层的电容为什么会随电极电位变化?试根据双电层结构的物理模型和数学模型型以解释。
电化学原理及其应用
第4章电化学原理及应用 5课时 教学目标及基本要求 1. 明确原电池及相关的概念。了解电极的分类,了解电极电势的概念。 2. 能用能斯特方程式进行有关计算。能应用电极电势的数据判断氧化剂、还原剂的相对强弱及氧化还原反应自发进行的方向和程度。 3. 了解摩尔吉布斯自由能变与原电池电动势,标准摩尔吉布斯自由能变与氧化还原反应平衡常数的关系。 4. 了解电解、电镀、电抛光的基本原理,了解它们在工程上的应用。了解金属腐蚀及防护原理。 教学重点 1. 原电池符号的书写 2. 影响电极电势的因素 3. 电极电势与吉布斯的关系 4. 电极电势的应用 教学难点 1. 电极类型 2. 能斯特方程及相关计算 3. 应用电极电势判断氧化剂、还原剂的相对强弱 本章教学方式(手段)及教学过程中应注意的问题 本章采用多媒体结合板书的方式进行教学。 在教学过程中注意 1. 原电池的设计 2. 浓度、酸度对电极电势的影响 3. 电极电势的应用 主要教学内容 4.1 原电池(Electrochemical cell) 任何自发进行的氧化还原(oxidation-reduction) 反应,只要设计适当,都可以设计成原电池
用以产生电流。 4.1.1 原电池的结构与工作原理 Zn(s)+Cu2+(aq)=Zn2+(aq)+Cu(s) 负极Zn(s) → Zn2+(aq)+2e-(Oxidation) 正极Cu2+(aq)+2e-→ Cu(s) (Reduction) 总反应:Zn(s)+ Cu2+(aq) → Zn2+(aq)+ Cu(s) 原电池的符号(图式)(cell diagram) 表示: 如铜- 锌原电池, : Zn ∣ZnSO4(c1) ┊┊CuSO4(c2) ∣Cu 规定:(1) 负极(anode) 在左边,正极(Cathode) 在右边,按实际顺序从左至右依次排列出各个相的组成及相态; (2) 用单实竖线表示相界面, 用双虚竖线表示盐桥; (3) 溶液注明浓度,气体注明分压; (4) 若溶液中含有两种离子参加电极反应, 可用逗号隔开,并加上惰性电极. 4.1.2 电极类型 按氧化态、还原态物质的状态分类: 第一类电极:元素与含有这种元素离子的溶液一起构成的电极。 (1) 金属──金属离子电极: Zn2+| Zn ;Cu2+| Cu ;Ni2+| Ni (2) 气体——离子电极: H+ |H2(g) | Pt 2H+ + 2e-=H2(g) Cl-| Cl2(g) | PtCl2(g) + 2e-=2Cl- 第二类电极: (1) 金属──金属难溶盐电极: 甘汞电极:Cl-|Hg2Cl2(s)| Hg Hg2Cl2(s) + 2e-=2 Hg (s) + 2 Cl- 银-氯化银电极:Cl-| AgCl(s) | Ag AgCl(s) + e-=Ag (s) + Cl- (2) 金属──难溶金属氧化物电极: 锑—氧化锑电极:H+ ,H2O(g) | Sb2O2(s) |Sb Sb2O2(s) + 6 H+ + 6 e-=2Sb +3H2O(g) 第三类电极: 氧化还原电极: MnO4-,Mn2+| Pt 2 MnO4-+ 16H+ + 10e-→ 2Mn2++8H2O 4.2 电极电势
