响应面法优化微波辅助萃取柠檬皮中果胶的研究2010

第27卷第1期2010年1月精细化工
FI NE C H E M I CAL S
Vo.l27,No.1
J an.2010
中药现代化技术
响应面法优化微波辅助萃取柠檬皮中果胶的研究*
章 凯,黄国林*,黄小兰,张高飞
(东华理工大学化学生物与材料科学学院,江西抚州 344000)
摘要:该文以离子液体[B M I M]C l(氯化1 丁基 3 甲基咪唑)水溶液为萃取剂,采用微波辅助萃取技术提取柠檬皮中的果胶,系统考察了[B M I M]Cl浓度、萃取温度、萃取时间和萃取溶剂体积等因素的影响,并通过响应面法对提取工艺进行了优化,得出最佳工艺条件为[B M I M]C l浓度1 0mo l/L,萃取温度88 ,萃取时间9 6m i n,每克干柠檬皮用萃取溶剂22 7mL,在该条件下,果胶的提取率为24 68%,与拟合的二次回归模型预测值基本相符。
关键词:离子液体;响应面法;微波辅助萃取;果胶提取;柠檬皮;中药现代化技术
中图分类号:TQ041.8 文献标识码:A 文章编号:1003-5214(2010)01-0052-05
Opti m i zati on ofM icro w ave assisted Extraction Technology of Pecti n fro m L e m on Peel U si ng R esponse Surface M ethodology
Z HANG Ka,i HUANG Guo li n*,HUANG X iao lan,ZHANG Gao fei (School of Che m istry,B io logy and M ater i al Science,East Ch i na Institute of T echnology,Fuzhou344000,J i angx i,China)
Abstract:The effects o f[B M I M]C l concentra ti o n,ex traction te mperature,ex traction ti m e and ex traction so lvent vo lu m e on the ex traction process of pectin using i o nic liqu i d s[B M I M]C l as t h e ex tractant fro m le m on pee l w ith the m icro w ave assisted ex tracti o n techno logy were investigated syste m atically in this paper.The extracti o n para m eters w ere opti m ized by t h e response surface m et h odology.The opti m um cond iti o ns are sho w n as fo ll o w s:[B M I M]C l concentration is1 0m ol/L, ex traction te m perature is88 ,the volum e of ex tracti o n so lvent used per gra m dried le m on peel is
22 7m L,ex traction ti m e is9 6m i n,and the ex traction rate can be up to24 68%.The pred iction
values o f the fitted quadratic regressi o n m ode lw ell agreed w ith t h e experi m enta l va l u es.
Key words:i o nic liqu i d s;response surface m ethodo logy;m icr ow ave assisted extraction;pecti n ex traction;le m on pee;l modern izati o n techno l o gy of traditi o na lCh i n ese m ed ici n es
Foundation ite m:The science and techno l o gy project for educati o n depart m ent in Jiangx i province (Gan jiaokejihan[2007]32)
柠檬皮大约占柠檬质量的20%~30%,是一种可以开发的再生性生物资源。柠檬皮中含有许多生物活性成分,其中果胶质量分数为25%~30%[1]。果胶具有抗菌、降血脂、抗辐射和抗癌等多种生理功能作用,近年来在食品、化工、医药等行业已经得到广泛的应用[2,3]。如果柠檬皮直接丢弃,不仅极大地浪费资源,而且对周边环境造成污染。因此,有效地提取柠檬皮中的果胶,提高产品附加值,减少环境污染具有重要意义。
目前,果胶提取一般有沸水抽提、酸法萃取、离子交换法、微生物法和草酸铵提取法,其中最常用的方法是酸法提取[4]。传统的酸法提取存在着强酸
*收稿日期:2009-08-09;定用日期:2009-10-22
基金项目:江西省教育厅科技项目(赣教科技函[2007]32号)
作者简介:章 凯(1983-),男,江西进贤人,硕士研究生,师从黄国林教授,主要从事化工分离和绿色化学工艺的研究,E-ma i:l zhangka i0907@hot m ai.l co m。
联系人:黄国林,男,教授,博士,硕士生导师,E-m ai:l guoli nhuang@s i na.co m。
性溶液消耗多、耗能大、工作强度大、提取效率低等缺点,其进一步发展已经受到限制。微波萃取技术是近年来发展较快的绿色分离技术,具有简便、高效、选择性强等优点,颇具发展潜力。然而,强酸性萃取剂会腐蚀设备,还会引起果胶中的糖苷键发生断裂。因此,选择利用高效、环保性的萃取溶剂十分必要。近年来,离子液体作为一种绿色溶剂已广泛
应用于生物活性物质的萃取分离[5~8],但是用于果胶的萃取鲜见报道。
响应面法是一种综合实验设计和数学建模的优化方法,可以在小区域内采用多元二次回归方程来拟合因素与响应值之间的函数关系,通过对回归方程的分析来寻求最优工艺参数,计算方便[9]。目前大多数果胶提取工艺的优化采用正交实验,响应面法优化果胶提取工艺很少报道。本研究以离子液体水溶液为萃取剂,采用微波法从柠檬皮中提取果胶,在单因素实验基础上,通过响应面法对工艺条件进行优化,为进一步开发利用提供有价值的工艺参数。
1 实验部分
1 1 材料和仪器
柠檬购自抚州市洪客隆超市,产地四川安岳,经东华理工大学生物系黄德娟副教授鉴定为尤克力柠檬;D 半乳糖醛酸、浓硫酸、咔唑均为AR;离子液体[B M I M]C l(氯化1 丁基 3 甲基咪唑)在文献[10]方法基础上合成,离子液体水溶液直接由相应的离子液体和二次蒸馏水配制而成。
W F-4000C微波萃取仪(上海屹尧微波化学有限公司),F W-100万能粉碎机(北京中兴伟业仪器有限公司),721E可见分光光度计(上海光谱仪器有限公司),DHG-903385-型电热鼓风干燥箱(上海新苗医疗器械有限公司)。
1 2 方法
1 2 1 样品预处理
新鲜柠檬皮搅碎,加入其3 5倍质量的水,微波处理15m in,用蒸馏水漂洗原料至漂洗液呈无色,60 烘箱中干燥48h,干燥后粉碎、过筛(80目),储存备用。
1 2 2 微波辅助萃取果胶
准确称取1 0g干柠檬皮,置于50mL三口烧瓶中,再加入15mL1 0m o l/L离子液体[B M I M]C l 水溶液,放入搅拌子,转速调至中速,在萃取温度80 、微波功率400W条件下,置于W F-4000C型微波萃取仪中提取5m in,经减压过滤后,得到上层清液。将其稀释一定倍数后,采用咔唑比色法[11]测定提取液中果胶含量,并按下式计算果胶提取率:果胶提取率/%=(提取液中果胶的质量/干柠
檬皮的质量)!1002 结果与讨论
2 1 单因素实验
2 1 1 [B M I M]C l浓度对提取率的影响
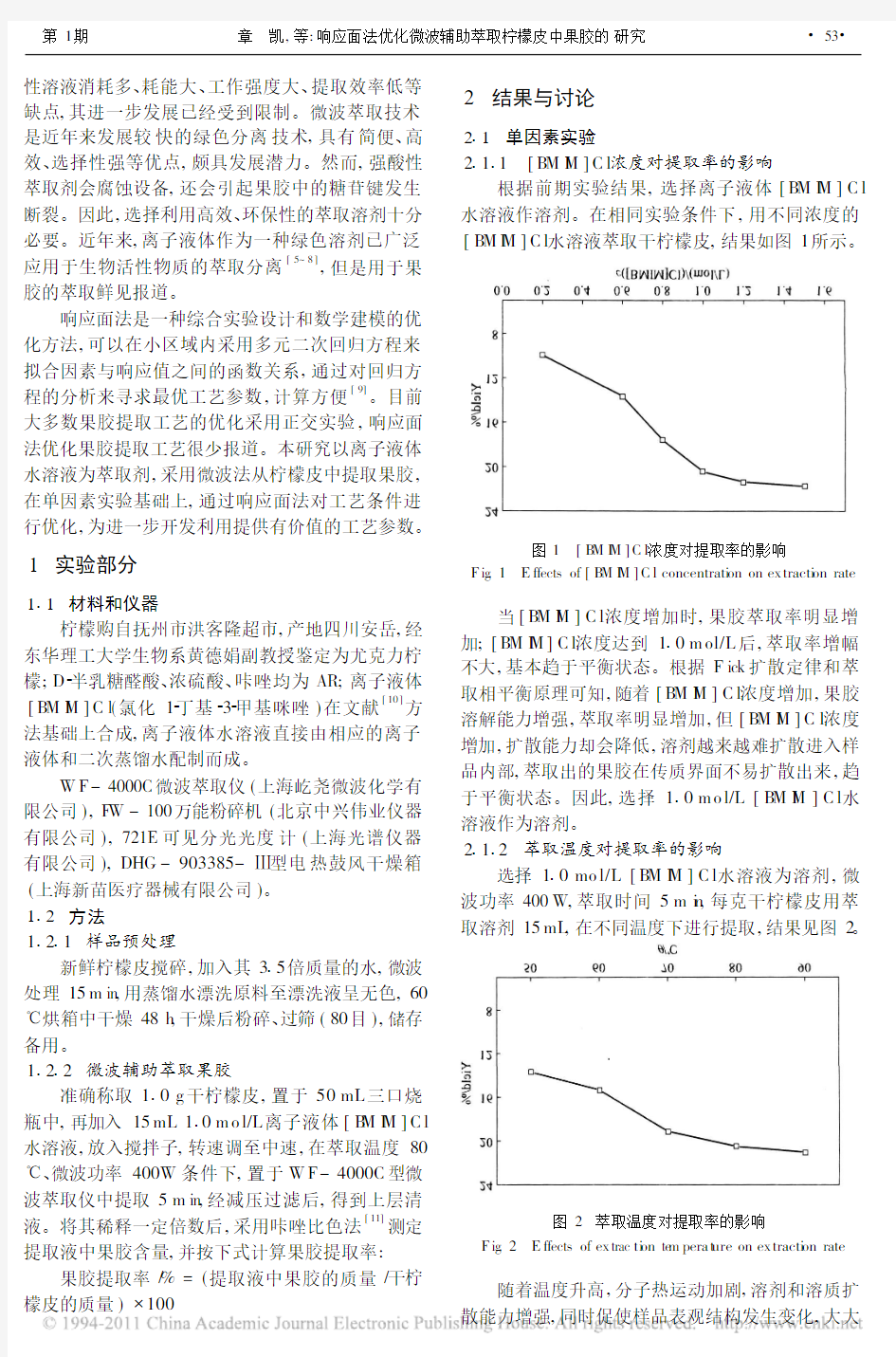
根据前期实验结果,选择离子液体[B M I M]C l 水溶液作溶剂。在相同实验条件下,用不同浓度的[B M I M]C l水溶液萃取干柠檬皮,结果如图1所示。
图1 [B M I M]C l浓度对提取率的影响
F ig.1 E ffects of[B M I M]C l concentrati on on ex tracti on rate
当[B M I M]C l浓度增加时,果胶萃取率明显增加;[B M I M]C l浓度达到1 0m ol/L后,萃取率增幅不大,基本趋于平衡状态。根据F ick扩散定律和萃取相平衡原理可知,随着[B M I M]C l浓度增加,果胶溶解能力增强,萃取率明显增加,但[B M I M]C l浓度增加,扩散能力却会降低,溶剂越来越难扩散进入样品内部,萃取出的果胶在传质界面不易扩散出来,趋于平衡状态。因此,选择1 0m o l/L[B M I M]C l水溶液作为溶剂。
2 1 2 萃取温度对提取率的影响
选择1 0mo l/L[B M I M]C l水溶液为溶剂,微波功率400W,萃取时间5m i n,每克干柠檬皮用萃取溶剂15mL,在不同温度下进行提取,结果见图2。
图2 萃取温度对提取率的影响
F ig.2 E ffects of ex trac ti on te m pera t ure on ex tracti on rate
随着温度升高,分子热运动加剧,溶剂和溶质扩散能力增强,同时促使样品表观结构发生变化,大大
?
53
?
第1期章 凯,等:响应面法优化微波辅助萃取柠檬皮中果胶的研究
加速提取过程,果胶萃取率明显增加。温度在50~
80 ,果胶提取率逐渐增大,80 后趋于平缓,温度过高会使果胶分子发生酯化降解,颜色加深发生褐变,对其性质和结构有所影响。故选择萃取温度为80 。
2 1
3 萃取时间对提取率的影响
选择1 0m ol/L[B M I M ]C l 水溶液为溶剂,微波功率400W,萃取温度80 ,每克干柠檬皮用萃取溶剂15mL ,考察萃取时间的影响,结果见图3
。
图3 萃取时间对提取率的影响
F i g .3 Effects o f ex traction ti m e on ex tracti on rate
可以看出,萃取时间1~8m in 内,随着提取时间增加,果胶提取率逐渐增加,8m in 之后,提取率略微下降,这是因为萃取时间过长导致果胶分子发生部分降解。故萃取时间8m i n 左右较好。2 1 4 溶剂体积对提取率的影响
选择1 0m o l/L [B M I M ]C l 水溶液为溶剂,微波功率400W,萃取温度80 ,萃取时间8m i n ,考察每克干柠檬皮用萃取溶剂量的影响,结果见图4
。
图4 溶剂量对提取率的影响
F i g .4 Effects o f so lvent vo l u m e on ex tracti on rate
可以看出,随着溶剂量增加,果胶提取率明显提高,溶剂20mL 时果胶提取率达最大,而后略微下降。溶剂量不足,溶剂难于扩散到样品内部;溶剂量大,提取液浓缩困难,经济成本增加,所以应该选择合适的溶剂用量。故选择每克干柠檬皮用萃取溶剂20mL 左右较佳。
2 2 响应面法优化工艺条件
2 2 1 中心组合实验设计
根据中心组合实验设计原理,在单因素实验基础上,确定1 0m o l/L [B M I M ]C l 水溶液为溶剂,微波功率400W,选取萃取温度(x 1)、萃取时间(x 2)、溶剂体积(x 3)为自变量,以果胶提取率y 为响应值,进行如下优化实验,实验因素与水平见表1,实验设计与结果见表2。
表1 因素与水平选择表
T ab l e 1 F ac t o rs and l eve l s of the experi m ent
因素
水平
-1 682-101+1 682温度(x 1)/ 58 1865758591 82时间(x 2)/m i n 4 64681011 36溶剂量(x 3)/mL
11 59
15
20
25
28 41
表2 实验设计与结果
T able 2 D esi gns and resu lts o f the exper i m ent
编号
水平
x 1x 2x 3响应值/%实验值预测值1-1-1116 4516 41200021 3921 863-11118 7919 21401 682021 5521 40511-122 3222 05600021 9321 867-1 6820015 3715 348001 68221 1720 82900-1 68216 8817 66101 6820024 5425 01111-1-122 0421 3112-11-116 5816 37130-1 682017 8518 43141-1122 3222 221500022 4321 861611124 4524 5117-1-1-115 4815 121800021 6521 861900021 8621 8620
21 95
21 86
2 2.2 回归模型方差分析
利用Design Expert 7 0软件对表2数据进行二次多元回归拟合,得到果胶提取率y 对自变量x 1、x 2和x 3的二次多项回归方程:
y =+21 85594+2 87416x 1+0 88400x 2+
0 93762x 3-0 12875x 1x 2-0 09625x 1x 3+
0 38625x 2x 3-0 59548x 12-0 68564x 22
-0 92428x 3
2
对上述回归模型进行方差分析,见表3。
?
54?精细化工 FI N E CHE M I C ALS
第27卷
表3 回归模型方差分析表
T able 3 V a riance ana l ysis o f regression equati on
方差来源平方和自由度
均方F 值P 值显著性
模型157 31917 4860 62<0 0001显著x 1112 821112 82391 28<0 0001显著x 210 67110 6737 010 0001显著x 312 01112 0141 64<0 0001显著x 1x
2
0 1310 130 460 5130不显著x 1x 30 07410 0740 260 6231不显著x 2x 3
1 1911 194 140 0693不显著x 21
5 1115 1117 720 0018显著x 2
2
6 7716 7723 500 0007显著x 23
12 31112 3142 70
<0 0001显著
残差2 88100 29失拟项2 2850 463 790 0852不显著
纯误差0 6050 12
总和
160 20
19
由表3可以看出,F 回归=60 62>F 0 01(9,5)=10 15776;P =0 0001<0 01,表明此回归模型极其显著。F 失拟=3 79
系数R 2
=0 9820,说明模型拟合程度良好,实验误差小。校正决定系数R 2
ad j 为0 9658,说明此模型能解释96 58%响应值的变化,仅有总变异的3 42%不能用此模型来解释。因此,实验值与预测值非常接近,此模型是合适的,可以用此模型对果胶提取率进行分析和预测。由表3还可知:模型一次项x 1、x 3极显著,x 2显著;交互项x 1x 2、x 1x 3、x 2x 3不显著;二次项x 2
3极显著,x 2
1、x 2
2显著。2 2 3 响应面分析
根据二次回归方程绘制的响应面及其等高线见图5~7
。
图5 萃取时间和温度对提取率影响的响应面和等高线F ig .5 R esponse surface and contours of the e ffect o f extraction
ti m e and temperat u re on ex tracti on rate
由图5可以看出,萃取温度不变,提取率随提取时间增加而增大,8~9 68m i n 达最大值,之后逐渐减小。提取时间不变,果胶提取率随温度升高而呈
上升趋势,增加比较明显,适当地提高温度有利于果胶提取,可缩短提取时间。等高线呈圆形,萃取时间和温度交互作用不显著,与模型的方差分析结果一致。图6与图5情况类似,萃取溶剂体积20~24 21mL 达最大值,之后逐渐减小,不过变化梯度比时间要大,溶剂体积和温度交互作用也不显著。由图7可以看出,萃取时间不变,随着溶剂体积增大,提取率先增大后减小;溶剂体积不变,随着萃取时间增加,提取率先增大后减小。二者变化明显,有一定的交互影响。回归模型预测的最佳工艺条件为[B M I M ]C l 浓度1 0m o l/L,萃取温度88 36 ,萃取时间9 63m i n ,每克干柠檬皮用萃取溶剂22 71mL ,果胶提取率理论值为25 10%。
?
55?第1期章 凯,等:响应面法优化微波辅助萃取柠檬皮中果胶的研究
2 3 验证实验
为了验证模型方程的适用性与可靠性,采用上述最佳工艺条件进行果胶提取实验,考虑到实际操作,将最佳工艺条件修正为[B M I M ]C l 浓度1 0m o l/L,萃取温度88 ,萃取时间9 6m i n ,每克干柠檬皮用萃取溶剂22 7mL,进行3次平行实验,结果表明,在此条件下,果胶平均提取率为24 68%,与预测值基本相符,说明此方程与实际情况拟合很好,充分验证了模型的合适性。
3 结论
本研究在单因素实验的基础上,采用响应面法
对提取工艺进行了优化,得出最佳工艺条件为[B M I M ]C l 浓度1 0m o l/L ,温度88 ,萃取时间9 6m in ,每克干柠檬皮用萃取溶剂22 7mL 。果胶提取率理论值为25 10%,实际验证值为24 68%,理论值与验证值基本相符。从而证明了此模型合理可靠,有一定实用价值。参考文献:
[1] 付 敏.蚕沙低甲氧基果胶提取工艺的研究[D ].四川大学,
2004.
[2] 全国中草药汇编编写组.全国中草药汇编[M ].北京:人民卫
生出版社,1996.
[3] 章 凯,黄国林.微波萃取技术及其在果胶提取中的应用[J ].
中国酿造,2009,(4):9-13.
[4] 周 坚,肖安红.功能性膳食纤维食品[M ].北京:北京工业出
版社,2004.
[5] Du F Y ,Xiao X H,Luo X J ,et al .App licati on of i on ic li qu i ds i n
the m icrowave assisted ex traction of pol yph enolic compound s fro m m ed i ci na l plants[J].Talanta ,2009,78:1177-1184.
[6] Lu Y B,M a W Y ,Hu R L ,et al .Ion ic li quid based m i cro w ave
assisted extracti on of phenolic al kaloi ds fro m the m ed i ci na l p lant Nel um bo nucifera Gaert n [J].Jou rnal of Chromatography A ,2008,1208(1-2):42-46.
[7] Du F Y ,Xi ao X H,Luo X J ,et al .App li cati on of i onic li qu i ds i n t he
m i cro w ave assist ed extracti on of trans res verat rol fro m Rh i z m a Pol ygon i Cuspi dati [J].J ournal of Chro matogra phy A ,2007,1140:56-62.[8] 杜甫佑,肖小华,李攻科.离子液体微波辅助萃取石蒜中生物
碱的研究[J].分析化学,2007,34(5):1570-1574.
[9] 赖红芳,林翠梧,陈海燕,等.响应面法优化微波提取扶芳藤抗
氧化物[J].精细化工,2008,25(9):869-871.
[10] Hudd leston J G ,V iss er A E ,Re i chertW M,et al .Characteri zation
and comparis on of hydroph ili c and hydrophob i c roo m te m perat ure i on ic li qu i ds incorporati ng t he i m i daz oli u m cati on [J ].Green C he m i stry ,2001,(3):156-164.
[11] NY 82 11#1988.果汁测定方法:果胶的测定[S].
(上接第29页)
参考文献:
[1] 刘国杰,耿耀宗.涂料应用科学与工艺学[M ].北京:中国轻工
业出版社,1999:518-520.
[2] B rauneckerW A ,M atyj asze w s k iK.C ontro ll ed /li vi ng rad ical
po l y m eri zati on :features ,developm ents ,and p ers pecti ves [J ].P rog Pol y m Sc,i 2007,32:93-146.
[3] H uyb rech ts J ,Bruy l an ts P ,K i rs henbau m K ,et a l .N e w app licati ons
of catal yti c ch ai n transfer pol ym eriz ati on to w aterborne b i nd ers for auto m oti ve pai n t s yste m s[J].Progress i n Organ i c Coati ngs ,2002,45:173-183.
[4] C reu t z S ,Jero m e R .E ffecti veness of b lock copo l y m ers as stab ili zers
f or aqu eous titan i um d i oxi de dispersi ons of a h i gh solid con tent [J].Progress i n Organ i c Coati ngs ,2000,40:21-29.
[5] Bouha m ed H,BoufiS,M agn i n A .D is pers i on of al um i na sus p ension
us i ng co m b li ke and d i b l ock copoly m ers p roduced by RAFT pol ym eriz ati on of A M PS and M PEG [J].Jou rnal of C oll o i d and In terface S ci en ce ,2007,312:279-291.
[6] Ausch ra C,E ckstei n E,M uh lebach A,et a l .Des i gn of ne w pig m ent
d i spersants by controlled radical pol y m eriz ati on [J].Progress i n O rgan ic Coati ngs ,2002,45:83-93.
[7] 郭宏涛,许钧强,何唯平.新型结构表面活性剂在涂料中的应
用[J].涂料工业,2008,38(6):59-61.
(上接第42页)
参考文献:
[1] 马立萌,徐宝财.新型绿色表面活性剂###烷基葡萄糖酰胺
[J ].精细化工,2005,22(S0):59-61.
[2] 唐林生,杨晶巍,陈恩平.葡萄糖(基)酰胺类新型表面活性剂
[J ].精细石油化工进展,2002,3(7):32-35.
[3] 赵寒冬,王建新.N 十二烷基葡糖酰甲胺香波体系的泡沫及增
稠性能[J].日用化学工业,2005,35(1):66-68.
[4] 王 峰,张高勇,李秋小.新一代绿色表面活性剂###烷基葡
萄糖酰胺[J].日用化学工业,2002,32(1):43-45.
[5] 冉君花,李和平.烷基葡萄糖酰胺的性能与生产工艺[J].精细
石油化工进展,2003,4(3):1-5.
[6] Ru iz C C,H ierrez uelo JM,Agu i ar J ,et a l .Physicoche m i cal st ud i es
on t he i nteracti on b et w een N decanoyl N m et hy l gl u ca m ide and
bov i ne seru m al bum i n[J ].B i o m acro m olecu les ,2007,8(8):2497-2503.
[7] Kao J un an .P rocess for p repari ng a m i des of N al kyl
pol yhydroxyal kyl a m i n es[P].US :5777165,1998-07-07.[8] Kao J unan ,S chei b el J J ,Shum at e R E,e t a l .Process f or preparing
N al ky lpo l yhydroxyalkyl a m i n es i n aqueou s /hydroxy sol ven t s[P].US :5625098,1997-04-29.
[9] 徐爱忠,王建新.N 十二烷基葡萄糖胺型表面活性剂的合成
[J].精细化工,2008,25(5):454-458.
[10] 牛利民,徐宝财,刘 滨.N 椰油酰基 N 甲基葡糖胺的制备
[J].中国洗涤用品工业,2000,(2):30-31.
[11] 张 浩,谢 晖,黄 莉,等.油酸改性甲基葡萄糖酰胺的合
成及其性能[J].南京工业大学学报,2008,30(4):84-87.
?
56?精细化工 FI N E CHE M I C ALS
第27卷
从果皮中提取果胶
从果皮中提取果胶 、实验目的 1、 学习从从果皮中提取果胶的基本原理和方法 ,了解果胶的一般性质。 2、 掌握提取有机物的原理和方法。 3、 进一步熟悉萃取、蒸馏、升华等基本操作。 、实验原理 果胶是一种高分子聚合物,存在于植物组织内,一般以原果胶、果胶酯酸和果胶酸 种形式存在于各种植物的果实、果皮以及根、茎、叶的组织之中。果胶为白色、浅黄色到黄 色的粉末,有非常好的特殊水果香味,无异味,无固定熔点和溶解度,不溶于乙醇、甲醇等 有机溶剂中。粉末果胶溶于 20倍水中形成粘稠状透明胶体,胶体的等电点 pH 值为3.5。果 胶的主要成分为多聚 D —半乳糖醛酸,各醛酸单位间经a — 1, 4糖甙键联结,具体结构式如 图1。 coon 小 |\oii H A )II 'ri El O'JII 图1果胶的结构式 在植物体中,果胶一般以不溶于水的原果胶 形式存在。 在果实成熟过程中,原果胶在果 胶酶的作用下逐渐分解为可溶性果胶, 最后分解 成不溶于水的果胶酸。 在生产果胶时,原料 经酸、碱或果胶酶处理,在一定条件下分解, 形成可溶性果胶,然后在果胶液中加入乙醇或 多价金属盐类,使果胶沉淀析出,经漂洗、干燥、精制而形成产品。 三、主要仪器和药品 仪器:恒温水浴锅、真空干燥箱、布氏漏斗、抽滤瓶、玻棒、纱布、表面皿、精密 烧杯、电子天平、小刀、小剪刀、真空泵、。 药品:干柑桔皮、稀盐酸、95%乙醇(分析纯)等。 四、实验内容 1、 柑桔皮的预处理 称取干柑桔皮20g ,将其浸泡在温水中(60?70C )约30min ,使其充分吸水软化, 并除掉 可溶性糖、有机酸、苦味和色素等;把柑桔皮沥干浸入沸水 5min 进行灭酶,防止果胶分解; 然后用小剪刀将柑皮剪成 2?3mm 的颗粒;再将剪碎后的柑桔皮置于流水中漂洗,进一步 除去色素、苦味和糖分等,漂洗至沥液近无色为止,最后甩干。 2、 酸提取 Illi Oil pH 试纸、 (}
柑橘皮果胶的提取实验
实验果胶的提取 一、目的要求 1.学习从柑橘皮中提取果胶的方法。 2.进一步了解果胶质的有关知识。 二、实验原理 果胶物质广泛存在于植物中,主要分布于细胞壁之间的中胶层,尤其以果蔬中含量为多。不同的果蔬含果胶物质的量不同,山楂约为6.6%,柑橘约为0.7~1.5%,南瓜含量较多,约为7%~17%。在果蔬中,尤其是在未成熟的水果和果皮中,果胶多数以原果胶存在,原果胶不溶于水,用酸水解,生成可溶性果胶,再进行脱色、沉淀、干燥即得商品果胶。从柑橘皮中提取的果胶是高酯化度的果胶,在食品工业中常用来制作果酱、果冻等食品。 三、实验器材 恒温水浴、布氏漏斗、抽滤瓶、玻棒、尼龙布、表面皿、精密pH试纸、烧杯、电子天平、小刀、真空泵、 柑橘皮(新鲜)。 四、实验试剂 1.95%乙醇、无水乙醇。 2.0.2 mol/L盐酸溶液 3.6 mol/L氨水 4.活性炭 五、操作步骤 1.称取新鲜柑橘皮20 g(干品为8 g),用清水洗净后,放入250 mL烧杯中,加120 mL水,加热至90 ℃保温5~10 min,使酶失活。用水冲洗后切成3~5 mm大小的颗粒,用50 ℃左右的热水漂洗,直至水为无色,果皮无异味为止。每次漂洗都要把果皮用尼龙布挤干,再进行下一次漂洗。 2.将处理过的果皮粒放入烧杯中,加入0.2 mol/L的盐酸以浸没果皮为度,调溶液的pH 2.0~2.5之间。加热至90 ℃,在恒温水浴中保温40 min,保温期间要不断地搅动,趁热用垫有尼龙布(100目)的布氏漏斗抽滤,收集滤液。 3.在滤液中加入0.5%~1%的活性炭,加热至80 ℃,脱色20 min,趁热抽滤(如橘皮漂洗干净,滤液清沏,则可不脱色)。 4.滤液冷却后,用6 mol/L氨水调至pH 3~4,在不断搅拌下缓缓地加入95%酒精溶液,加入乙醇的量为原滤液体积的1.5倍(使其中酒精的质量分数达50%~60%)。酒精加入过程中即可看到絮状果胶物质析出,静置20 min后,用尼龙布(100目)过滤制得湿果胶。 5.将湿果胶转移于100 mL烧杯中,加入30 mL无水乙醇洗涤湿果胶,再用尼龙布过滤、挤压。将脱水的果胶放入表面皿中摊开,在60~70 ℃烘干。将烘干的果胶磨碎过筛,制得干果胶。
茶叶中咖啡因的微波提取工艺
实验2 茶叶中咖啡因的微波提取工艺 一、实验目的 1.明确微波提取法提取原理; 2.学会用微波提取法提取茶叶中的咖啡因; 3.使用分光光度计,建立标准曲线,检测茶叶中咖啡因的含量。 二、实验原理 咖啡因是杂环化合物嘌呤的衍生物,它的化学名称为:1,3,7-三甲基-2,6-二氧嘌呤,其结构式如下: N N H N N N N N O O CH3 CH3 H3C 嘌呤咖啡因 含结晶水的咖啡因系无色针状结晶,味苦,能溶于水、乙醇、氯仿等。在100℃时即失去结晶水,并开始升华,120℃时升华相当显著,至178℃时升华很快。无水咖啡因的熔点为234.5℃。 从茶叶中提取咖啡因传统的方法有乙醇回流法和碳酸钠溶液煮沸法。但前者需在Soxhlet萃取器中回流约2.5h 以上, 周期较长、醇耗、能耗较大, 不利于工业化生产。后者虽只需煮沸20m in, 但煮沸后呈泥胶状, 过滤和萃取均很难, 致使收率很低。 微波是频率介于300 MHz和300 GHz之间的电磁波。微波提取的原理是微射线辐射于溶剂并透过细胞壁到达细胞内部,由于溶剂及细胞液吸收微波能,细胞内部温度升高,压力增大,当压力超过细胞壁的承受能力时,细胞壁破裂,位于细胞内部的有效成分从细胞中释放出来,传递转移到溶剂周围被溶剂溶解。微波具有穿透力强、选择性高、加热效率高等特点.微波作用于植物细胞壁,其热效应促使细胞壁破裂和细胞膜中的酶失去活性,细胞中多糖容易突破细胞壁和细胞膜而被提取出来,大大加快了反应提取速度、反应时间以分、秒计,有效地提高了多糖得率。微波提取法是强化固液提取过程颇具发展潜力的一项新型辅助提取技
术。 三、仪器与试剂 仪器:微波萃取仪;紫外-可见分光光度计;分析天平(1台);50 mL容量瓶(8个);100 mL 容量瓶(1个);1 mL 、2 mL 吸量管;50mL烧杯(10个); 100mL(3个); 布式漏斗;滤纸;抽滤瓶等。 试剂:无水乙醇;0.5 mg/mL咖啡因标准溶液等。 四、实验步骤: (一)、制作标准曲线 从无水乙醇为溶剂的咖啡因储备液( c = 500. 0μg/ mL) 中移取0. 50 ,1. 00 ,1. 50 ,2. 00 ,2. 50 ,3. 00 ,3. 50 mL于7 个50 mL 容量瓶中用50%的乙醇定容,得到浓度为5. 00 ,10. 00 ,15. 00 ,20. 00 ,25. 00 ,30. 00 ,35. 00μg/ mL 的系列标准溶液。在紫外分光光度计上测其最大吸收波长处的吸光度A ,得标准曲线。 (二)、咖啡因的提取 1.提取工艺流程 原料→粉碎→加入溶剂→微波处理→过滤→离心→粗提液→测定吸光度值2.提取工艺条件优化 (1).单因素实验 I.微波功率的筛选 微波功率的筛选称取5 g茶叶, 加入80 mL 50 %乙醇, 配制5 份相同混合液, 将混合液放置于微波提取仪中, 设定温度为90 ℃的条件, 改变功率(300 W、400 W、500 W)微波10 min, 测定不同微波功率下提取液的吸光度值A. II.微波时间的筛选 称取5 g 茶叶, 加入80mL50 %乙醇, 配制5 份相同混合液,将混合液放置于微波提取仪中, 在设定温度为90 ℃,微波功率为500 W的条件下,微波加热不同的时间(13 min、14 min、15 min) ,测定不同微波时间条件下提取液的吸光度A. III.微波温度的筛选 称取5 g茶叶,加入80 mL 50 %乙醇,配制6 份相同混合液,将混合液放
微波协同离子交换法提取果胶的研究
微波协同离子交换法提取果胶的研究 唐满生,戴永强 (湖南科技学院化学与生物工程系,湖南 永州 425100) 摘要:采用微波辐射协同离子交换法提取了桔皮中的果胶。通过单因素实验和正交实验探讨了微波密度、辐射时间和液料比对果胶得率及品质的影响,确定了实验最佳条件为:微波密度为650 μW/cm2,微波辐射提取时间8 min,液料比为20 mL/g,果胶得率为36.62%。产品的果胶百分含量为91.54%,胶凝度为126.05°,灰分含量为0.037%,优于我国食品质量标准。 关键词:果胶;微波辐射;离子交换 中图分类号:O636.1;文献标识码:A;文章篇号:1673-9078(2009)06-0678-03 Extraction of Pectin from Orange Peel by Ion-exchange under Microwave Irradiation TANG Man-sheng, DAI Y ong-qiang (Department of Chemistry and Bio-engineering, Hunan University of Science and technology, Y ongzhou 425100, China)Abstract: Pectin was extracted from orange peel by microwave radiation coupled with ion-exchange method. Effects of microwave radiation power, irritation time and liquid/material ratio on the extraction yield were discussed. By orthogonal experiments, the optimum extraction conditions were determined as follows: the microwave radiation power of 650 μW/cm2, liquid/material ratio of 20mL/g and extracting time of 8 minutes, under which the pectin yield was 33.69%. The pectin content in the products was 91.54%, the jelly grade was 126.05°, and the ash content was 0.037%. The quality of the product was superior to the quality requirements in the national food quality specifications. Key words: pectin; microwave radiation; ion-exchange 果胶作为一种亲水性植物胶,广泛存在于植物根、茎、叶、果的细胞壁中,一般分为水溶性和非水溶性(原果胶)两类。目前,果胶的生产原料主要是柑桔类果皮、橙皮、柠檬皮、苹果皮,作为果汁加工的副产品,来源稳定丰富。以各种果皮为原料提取果胶,既可变废为宝,取得较高的经济效益,又能有效地保护生态环境。 目前,国内从果皮中提取果胶多采用酸提取这一传统方法。近年来,用离子交换法和微波辐射法从果皮中提取果胶的方法已有报道[1-4]。本实验采用在酸法提取桔皮果胶的基础上,将微波法与离子交换法相结合,优化从桔皮中提取果胶的工艺条件,收效良好。 1 材料与方法 1.1 材料与试剂 新鲜桔皮。 无水乙醇、盐酸、氢氧化钠、氯化钙和蔗糖均为收稿日期:2008-12-01 作者简介:唐满生(1964-),男,湖南永州人,实验师,主要研究方向:食品科学分析纯;强酸性阳离子交换树脂购自天津大茂化学试剂厂。 1.2 仪器 pHS-3C型酸度计;LG微波炉;R201D-Ⅱ旋转蒸发仪;SHB-Ⅲ真空泵;电热鼓风干燥箱。 1.3 实验方法 1.3.1 果胶的提取 将桔皮放入蒸馏水中浸泡0.5 h,煮沸5 min灭酶,沥干后置烘箱于70 ℃烘干,粉碎。称取10.0 g桔皮粉末和0.5 g氢型732阳离子交换树脂,置500 mL烧杯中,将盐酸调节酸度至2.0,微波辐照浸提。过滤后滤液减压浓缩,注入到相同体积的、已预冷的95%乙醇溶液中,低温静置4~8 h,抽滤。滤饼用95%乙醇溶液洗涤,打散后铺成薄层,置烘箱中(45℃)烘干至恒重,称重。实验采用单因素实验和正交实验来确定微波密度、微波辐射时间、料液比果胶提取的最佳条件。 1.3.2 果胶含量与pH值的测定 含量测定采用重量法[5]进行测定。pH值的测定按文献[1]中的方法进行。 678
微波辅助萃取技术的应用和研究进展
微波辅助萃取技术的应用和研究进展 王新 郑先哲 (东北农业大学 工程学院,哈尔滨,150030) 摘要:本文描述了微波辅助萃取技术是一种很有潜力的萃取技术,全面综述了它在农业、食品工业、环境分析化学、传统中医药工业等方面的应用和研究进展。微波辅助萃取技术在传统萃取工艺基础上进行了强化传热、传质,试验体现了微波萃取技术具有装置简单、应用范围广、萃取效率高、重现性好、消耗溶剂和时间少、污染少等优点。目前,微波辅助萃取技术的工业化问题已倍受重视,这必将推动微波辅助萃取技术向更深、更广的领域发展。 关键词:微波辅助萃取;植物性物料;食品; 中图分类号:S26.201 0引言 微波辅助萃取技术是一种新兴技术。现今已有许多试验采用微波辅助萃取的方法,并且已形成了多种比较完善的微波辅助萃取系统。最新研究引进了将微波辅助萃取技术预处理样品和其它分析技术结合使用,发展前景很广[1,2,3]。在不同的试验中,各自体现了装置简单、应用范围广、萃取效率高、重复性好、消耗溶剂及时间少、环境污染少等优点[4]。 在实验室或工厂里,将微波技术改进后,用于从不同的植物原料中萃取许多挥发性组分。它的原理与索式提取、蒸汽蒸馏和浸提等传统方法是不同的。微波加热是样品直接吸收微波能[5]。微波能也是一种能量。在能量传输过程中,微波能直接影响极性分子原料。微波电磁场能让这些极性分子迅速极化。当使用频率为2450兆赫兹的微波能萃取时,溶质或溶剂中的极性分子将以每分钟24.5亿次的速度做极性反转运动,使分子间产生相互摩擦和碰撞。通过这种方式的运动,分子内的活性组分(极性部分)彼此间会加速碰撞并加速反应,同时产生了大量的热能,这些热能促使细胞破裂、同时细胞液溢出并且扩散到溶剂中[6]。因此,微波促1使细胞里的有效组分自由的流出,在低温条 收编日期:年月日 作者简介:王新(1979-),女(汉),辽宁省大连市,研究生,农产品加工及贮藏工程 通讯地址:150030,ml_earquake@https://www.wendangku.net/doc/7c3269799.html, 通讯作者:郑先哲(1968-),男(汉),吉林省德惠,教授,通讯地址:150030,zhengxz2006@https://www.wendangku.net/doc/7c3269799.html, 件下若进一步利用萃取媒介,将其捕获、溶解,再借助于过滤、分离技术,就可得到萃取物。 1微波萃取技术在萃取植物中天然活性组分方面的应用 自1986 年Ganzler等人首先报道了微波用于天然产物中化学成分的提取后,微波萃取被广泛用于生物碱类、黄酮类、蒽醌类、皂苷类等多种试验研究。如周志等[7]用微波从茶叶中提取茶多酚。郭振库等[8]应用自行设计的具较高压力控制精度的专用微波制样系统,对金银花中有效成分绿原酸和异绿原酸类化合物的提取条件进行了分析,并与超声波提取进行了比较,结果提取率提高了近2成。 邵海等[9]人用微波萃取核桃油工艺的研究等等。 2007年,Flamini Guido等[10]将新型的微波方法应用在从植物中萃取香精油试验研究。比起传统方法,微波方法萃取的香精油,含氧化混合物较高、单萜很少。由此可见,微波加热是更有效的,体现了省时、节能的优点。Lucchesi Marie等[11]研究了无溶剂的小豆蔻香精油的萃取。多参数的研究形成了一个中心合成设计,用来评估影响无溶剂萃取小豆蔻种子香精油的性能的三个变量的影响。由电荷耦合器件提供的统计结果表明试验选择的参数:萃取时间,微波辐射能和种子的水分含量都是相当关键的。 2微波萃取技术在食品工业上中的应用 最近,许多作者就微波萃取技术在物理、化学性质等方面的近期应用介绍了一些
从果皮中提取果胶
从果皮中提取果胶 一、实验目的 1、学习从从果皮中提取果胶的基本原理和方法, 了解果胶的一般性质。 2、掌握提取有机物的原理和方法。 3、进一步熟悉萃取、蒸馏、升华等基本操作。 二、实验原理 果胶是一种高分子聚合物,存在于植物组织内,一般以原果胶、果胶酯酸和果胶酸3种形式存在于各种植物的果实、果皮以及根、茎、叶的组织之中。果胶为白色、浅黄色到黄色的粉末,有非常好的特殊水果香味,无异味,无固定熔点和溶解度,不溶于乙醇、甲醇等有机溶剂中。粉末果胶溶于20倍水中形成粘稠状透明胶体,胶体的等电点pH值为3.5。果胶的主要成分为多聚D—半乳糖醛酸,各醛酸单位间经a—1,4糖甙键联结,具体结构式如图1。 图1 果胶的结构式 在植物体中,果胶一般以不溶于水的原果胶形式存在。在果实成熟过程中,原果胶在果胶酶的作用下逐渐分解为可溶性果胶,最后分解成不溶于水的果胶酸。在生产果胶时,原料经酸、碱或果胶酶处理,在一定条件下分解,形成可溶性果胶,然后在果胶液中加入乙醇或多价金属盐类,使果胶沉淀析出,经漂洗、干燥、精制而形成产品。 三、主要仪器和药品 仪器:恒温水浴锅、真空干燥箱、布氏漏斗、抽滤瓶、玻棒、纱布、表面皿、精密pH试纸、烧杯、电子天平、小刀、小剪刀、真空泵、。 药品:干柑桔皮、稀盐酸、95%乙醇(分析纯)等。 四、实验内容 1、柑桔皮的预处理 称取干柑桔皮20g,将其浸泡在温水中(60~70℃)约30min,使其充分吸水软化,并除掉可溶性糖、有机酸、苦味和色素等;把柑桔皮沥干浸入沸水5min进行灭酶,防止果胶分解;然后用小剪刀将柑皮剪成2~3mm的颗粒;再将剪碎后的柑桔皮置于流水中漂洗,进一步除去色素、苦味和糖分等,漂洗至沥液近无色为止,最后甩干。 2、酸提取
微波辅助提取
微波辅助提取-高效液相色谱法测定蔬果中的Vc含量 摘要:维生素C是一种水溶性维生素。在人体中为维持人体健康发挥着重要的作用。在本实验中,将市场上新鲜猕猴桃榨汁后,用微波辅助提取维生素C。配制出一系列标准浓度的维生素溶液,在265nm波长的光下用高效气相色谱测量其峰面积,并作出其峰面积-浓度曲线,得到其关系式。通过测出三组样品的峰面积,代入公式中计算维生素C的含量。实验测出猕猴桃中维生素C含量为56.95 mg·L-1,RSD为5.3%。 关键词:微波辅助提取液相色谱法维生素C 标准曲线 1 引言 维生素C是一种水溶性维生素,在所有维生素中,维生素C是最不稳定的,在贮藏、加工和烹调时,极易被氧化和分解。而维生素C是维持人体健康的最重要的维生素之一,人体不能自身合成,必须以食物形式获取。研究发现维生素C 的缺乏可导致坏血病和免疫力底下等多种疾病,其在人体中的含量高低常作为某些疾病诊断及营养分析的重要指标。因此抗坏血酸的定量分析在食品、医药领域相当重要[1]。 目前测定抗坏血酸含量的方法有很多,其中包括碘量法[2]、紫外分光光度法[3]、伏安法[4]、红外光谱法[5]、库伦滴定法[6]和液相色谱法等等。本实验采取微波辅助提取,快速、简便地萃取中蔬果中的维生素C,并采用高效液相色谱法进行分析,以维生素C标准系列溶液色谱峰面积相对其浓度做校准曲线,根据样品中维生素C的峰面积,由校准曲线计算其浓度。 2 实验部分 2.1 试剂 乙腈:色谱纯; 冰乙酸,维生素C,磷酸二氢钾:分析纯; Vc标准溶液:快速准确称取0.025 g Vc,用1 mol/L乙酸溶液溶解,定量转移至250 mL容量瓶中,用1 mol/L乙酸溶液定容,得到100 mg/L标准溶液备用,现用现配; 猕猴桃一个。 2.2 仪器 平头进样器;
实训8:柑橘皮果胶的提取及检测 (1)
综合实训8柑橘皮中果胶的提取及检测 摘要:为提高果胶质量,本实验拟采用酸性乙醇沉淀法协同酶法提取柑橘皮中的果胶,从而为工业生产提供理论依据。 关键词:柑橘皮果胶酸性乙醇沉淀酶法 1 前言 果胶本身为白色或淡黄色的粉末,稍有特异气味,在二十倍的水中几乎完全溶解,形成一种含负电荷的粘性液体。果胶的一个最重要性质是其胶凝化作用,在食品工业中被用作胶冻稳定剂和增稠剂;在医药中用来制造止血剂、血浆代用品等;在轻工业中还可以用来制造化妆品及代替琼脂做部分微生物的培养基,应用非常广泛。 柑橘为我国著名果品之一,柑橘皮中果胶含量约占20%~30%。从柑橘皮中提取的果胶是高酯化度的果胶,酯化度在70%以上,提取的果胶不仅安全优质而且是对柑橘皮的“废物利用”,不仅可解决废物处理问题,还可提高柑橘生产加工的经济效益,是柑橘综合利用的很好途径。 2 实验目的 掌握酸性乙醇沉淀法[1]协同酶法[2] [3]提取果胶的基本原理和方法 掌握咔唑比色法[4]测定果胶含量的基本方法和操作 3 实验原理 果胶是一种植物胶体,分布于果蔬类植物中,存在于植物的细胞壁和细胞内层,是细胞壁的一种组成成分。不同的果蔬中果胶的质量和含量不同,在未成熟的水果和果皮中,果胶多数以原果胶存在,原果胶不溶于水,用酸水解,生成可溶性果胶,再经乙醇沉淀、洗涤,即得果胶粗提液。 纤维素酶是酶的一种,具有高度专一性,能够在分解纤维素时发挥催化作用,在果胶提取的过程中加入纤维素酶可破坏细胞壁,从而增加果胶的提取率。(本次实验不用纤维素酶) 淀粉酶可以水解淀粉和糖原,从而提高果胶的纯度。综合利用两种酶辅助酶解提取果胶,可显著提高果胶质量。 果胶含量的测定方法主要有质量法、容量法、滴定法、高效液相色谱法、气相色谱法和比色法等。咔唑比色法快速简单易行,可对果胶粗品进行检测,从而对果胶含量进行半定量分析。其测定果胶含量的原理是果胶在硫酸的作用下水解成半乳糖醛酸,在硫酸溶液中与咔唑试剂进行缩合反应,生成紫红色化合物,在525nm处有最大吸收峰。测定样品中半乳糖醛酸的含量,即可确定果胶的含量。 4 实验设备 电热恒温水浴锅,紫外可见分光光度计,台式离心机,电子天平,分析天平,样品粉碎机,比色皿,称量纸,药匙,烧杯,玻璃棒,pH计,纱布,容量瓶,量筒,离心杯,试管,试管架,比色管(25mL),移液枪,枪头,100目筛,电磁炉。
盐析法从苹果皮中提取果胶的工艺研究
学士学位论文 盐析法从苹果皮中提取果胶的工艺研究
摘要 以新鲜苹果皮为原料研究果胶的提取工艺,采用传统的酸水解法进行提取,并应用盐析法沉淀分离果胶。实验结果表明最佳条件为在温度90℃,料液比为1:8,提取时间为1.5h,pH=2进行酸水解,在温度60℃,盐用量为5mL,时间为1h,pH=5条件下进行沉淀,果胶提取率最大为11.4%。 【关键词】苹果皮;果胶;提取;盐析
Abstract To study the extraction process of pectin with fresh apple peel as raw material,Samples were extracted with the traditional acid hydrolysis, and application of precipitation separation pectin salting-out method.This experiment measured properly for 90℃temperature, ratio of material and liquid was 1:8, extracting time for 1.5 h, pH value was 1.5, for the acid solution, and that measured properly for 60℃ temperature, the salt amount was 5 mL, Salting time is one hour,pH value was 5, for the precipitation, the largest for 11.3%. 【keywords】Apple peel;Pectin;Extract;Salting out
柑橘皮中果胶的提取
柑橘皮中果胶的提取 Document number【AA80KGB-AA98YT-AAT8CB-2A6UT-A18GG】
柑橘皮中果胶的提取 实验方案 一、目的要求: 1.学习从柑橘皮中提取果胶的方法。 2.进一步了解果胶质的有关知识。 二、实验原理 : 果胶物质广泛存在于植物中,主要分布于细胞壁之间的中胶层,尤其以果蔬中含量为多。不同的果蔬含果胶物质的量不同,山楂约为6.6%,柑橘约为0.7~1.5%,南瓜含量较多,约为 7%~17%。在果蔬中,尤其是在未成熟的水果和果皮中,果胶多数以原果胶存在,原果胶不溶于水,用酸水解,生成可溶性果胶,再进行脱色、沉淀、干燥即得商品果胶。从柑橘皮中提取的果胶是高酯化度的果胶,在食品工业中常用来制作果酱、果冻等食品。 三、实验药品: 仪器: 恒温水浴、布氏漏斗、抽滤瓶、玻棒、尼龙布、表面皿、精密 pH 试纸、烧杯、电子天 平、小刀、真空泵。 材料: 柑橘皮(新鲜)。 试剂: 1.95%乙醇、无水乙醇。 2.0.2 mol/L 盐酸溶液。 3.6 mol/L 氨水。 4.活性炭。 四、操作步骤 : 1.称取新鲜柑橘皮20 g(干品为8 g),用清水洗净后,放入250 mL 烧杯中,加120 mL 水,加热至90 ℃保温5~10 min,使酶失活。用水冲洗后切成3~5 mm 大小的颗粒,用50 ℃左右的热水漂洗,直至水为无色,果皮无异味为止。每次漂洗都要把果皮用尼龙布挤干,再进行下一次漂洗。 2.将处理过的果皮粒放入烧杯中,加入0.2 mol/L 的盐酸以浸没果皮为度,调溶液的 pH 2.0~ 2.5之间。加热至90 ℃,在恒温水浴中保温40 min,保温期间要不断地搅动,趁热用 垫有尼龙布(100目)的布氏漏斗抽滤,收集滤液。 3.在滤液中加入0.5%~1%的活性炭,加热至80 ℃,脱色20 min,趁热抽滤(如橘皮漂洗干净,滤液清沏,则可不脱色)。 4.滤液冷却后,用6 mol/L 氨水调至 pH 3~4,在不断搅拌下缓缓地加入95%酒精溶液,加入乙醇的量为原滤液体积的1.5倍(使其中酒精的质量分数达50%~60%)。酒精加入过程中即可看到絮状果胶物质析出,静置20 min 后,用尼龙布(100目)过滤制得湿果胶。 5.将湿果胶转移于100 mL 烧杯中,加入30 mL 无水乙醇洗涤湿果胶,再用尼龙布过滤、挤压。将脱水的果胶放入表面皿中摊开,在60~70 ℃烘干。将烘干的果胶磨碎过筛,制得干果胶。 五、注意事项: 1.脱色中如抽滤困难可加入2%~4%的硅藻土作助滤剂。 2.湿果胶用无水乙醇洗涤,可进行2次。 3.滤液可用分馏法回收酒精。 六、实验现象及结论记录表:
柑橘皮中提取果胶工艺条件研究(王文娇)
《果蔬加工工艺》课程论文 论文题目柑橘皮中果胶提取工艺研究 学生姓名王文娇学号 202015031 专业班级园林工程系2010级食品科学与工程 授课教师孙磊完成时间 2012-12-01 2012 年12月01日
柑橘皮中提取果胶工艺条件研究 食品科学与工程王文娇 201015031 摘要:本文以干燥的柑橘皮粉末为原料,采用传统的酸水解法和正交试验法进行果胶提取的优化试验。结果表明,影响果胶产率的强弱因素依次为C>A>D>B,提取果胶的最佳条件为:温度(A)85 ℃、料液比(B,g/g)1∶15、pH 值(C)1.0、提取时间(D)90 min,即最佳组合条件为A3B2C4D3,此时果胶的提取率达到最优化,果胶质量最好。 关键词:柑橘皮;果胶;工艺 The Processing Study of the Pectin Extracted from the Citrus Peel Abstract:This paper make the dry powder of Citrus skin as raw material, using the traditional method of acid solution and orthogonal experiments to study the optimal design of the experiment of extraction of pectin. The results show that the orthogonal extraction time, The impact of the strength of pectin yield factors were C>A>D>B, the best conditions for extraction of pectin is: temperature(C) 85 ℃, raw and liquid ratio(A) 1∶15, pH value (B)1.0, extraction time(D) 90 min, in other words, the best combination of condition is A3B2C4D3. Key words:Citrus peel;pectin;processing 柑橘皮含果胶在1.5 %~3 %以上,提取后可用于制作果酱、果冻、果汁的增稠剂,化妆品的乳化剂,制药工业的油膏基,还可以降血糖、降血脂、降胆固醇[1-2]。果胶(Pectin)是柑橘皮中一种重要的水溶性膳食纤维,属于异性分支(heterogeneous branched)多糖[3],存在于初级细胞壁和细胞间质内,其分子中除主链的α-D-(1-4)-半乳糖醛酸基外,还包括20 %的中性多糖侧链:D-半乳糖、L-阿拉伯糖和L-鼠李糖。本文对柑橘皮中提取果胶的影响条件及提取工艺进行初步优化研究,以期为进一步综合利用柑橘皮渣提供依据。 1 材料与器材 1.1 原料 柑橘:购于水果批发市场。 1.2 主要药品
果胶品牌
果胶品牌 果胶是一种新型、天然的多功能型食品添加剂,一般从柑橘皮、苹果皮、柠檬片等植物细胞中提取,通常为白色至黄褐色粉末,目前广泛应用在饮料,果酱,软糖,果冻等食品中,果胶可以作为增稠剂和稳定剂,以增强稠度、改善口感和风味,同时也可以代替黄原胶或明胶一起使用,提升产品的品质质量。 近年来,随着果胶的蛋白质稳定性、乳化特性越来越受到商家的青睐,以致于果胶的需求量也日益增长,那么哪些果胶品牌比较好呢?下面为大家介绍市场上比较流行的五大果胶品牌。 市场上比较流行的五大果胶品牌分别是:德国的嘉吉、意大利的施华、美的斯比凯可、荷兰的帝斯曼还有中国的安德里,主要以进口果胶品牌为主,一般进口的果胶的原料主要是从柑橘皮中提取,含量最丰富,口感清爽,而且纯度高;而国产的果胶一般是从果皮干或者苹果皮中提取,会出现皮味过重,口感不量,纯度底跟质量次等问题。正因为进口果胶不管是在质量上还是来源上都会比国产果胶好些,所以大部分做中高端产品的商家都会选用进口果胶,而对质量要求不高的普通商家来说,则选择国产的安德利也是不错的选择。 帝斯曼和嘉吉虽是进口果胶品牌,有着长年的积累,在食品行业中拥有着许多客户资源,但是两家企业的主营产品并不是果胶,其旗下拥有其他的食品添加剂产品,所以不管从技术专业度,科研投入,原料质量方面上都还是拥有着一定的差距。
施华和斯比凯可是在现市场上做的较好的2大果胶品牌,2者的果胶都是从橙皮中提取,果胶含量丰富,但这两个品牌最大的区别就是斯比凯可果胶是从干柑橘皮中提取的,容易出现皮味过重,甚至有腐烂的气味,口感不良的问题,主要是因为原料处理时控制不好所导致的,而且斯比凯可的果胶价格也是相对其他品牌来说较贵的,自然商家生产成本也比较贵。再者就是意大 利施华,意大利施华的果胶是从精选瓶中的新鲜橙皮中提取,果胶质量最好,性能最好,而且口感清爽,纯度高使用成本低,再加上价格便宜,所以性价比最高。 意大利施华成立于1854年,至今已有160多年的历史,其代理商遍布60多个国家和地区,专业从事果胶开发及生产,雄厚的技术实力,在当地拥有广阔的柑橘种植农场,在植物提取物领域享誉盛名。广州健科作为施华果胶在中国的代理,将会携手施华共同推广果胶产品,定期举办大型研讨会,共同讨论为生产企业提供产品的解决方案,因此施华是现市场五大果胶品牌中专业技术较强,性价比最高的品牌。
实验四 果胶的提取
实验四果胶的提取 一、引言 果胶广泛存在于水果和蔬菜中,如苹果中含量为0.7—1.5%(以湿品计),在蔬菜中以南瓜含量最多(达7%-17%)。果胶的基本结构是以α-1,4苷键连接的聚半乳糖醛酸,其中部分羧基被甲酯化,其余的羧基与钾、钠、铵离子结合成盐。 在果蔬中,尤其是未成熟的水果和皮中,果胶多数以原果胶存在,原果胶通过金属离子桥(比如Ca2+)与多聚半乳糖醛酸中的游离羧基相结合。原果胶不溶于水,故用酸水解,生成可溶性的果胶,再进行提取、脱色、沉淀、干燥,即为商品果胶。从柑橘皮中提取的果胶是高酯化度的果胶(酯化度在70%以上)。在食品工业中常利用果胶制作果酱、果冻和糖果,在汁液类食品中作增稠剂、乳化剂。 二、实验材料、试剂与仪器 材料:桔皮,苹果等; 试剂:0.25% HCL,95%乙醇(AR),精制乙醇,乙醚,0.05mol/L HCl,0.15%咔唑乙醇溶液,半乳糖醛酸标准液,浓硫酸(优级纯) 仪器:分光光度计,50mL比色管,分析天平,水浴锅,回流冷凝器,烘箱等 三、实验步骤 (一)果胶的提取 1、原料预处理:称取新鲜柑橘皮20g(或干样8g),用清水洗净后,放入250mL容量瓶中,加水120mL,加热至90℃保持5-10min,使酶失活。用水冲洗后切成3~5mm的颗粒,用50℃左右的热水漂洗,直至水为无色、果皮无异味为止(每次漂洗必须把果皮用尼龙布挤干,在进行下一次的漂洗)。 2、酸水解提取:将预处理过的果皮粒放入烧杯中,加约60mL 0.25% HCL 溶液,以浸没果皮为宜,调pH至2.0~2.5,加热至90℃煮45min,趁热用100目尼龙布或四层纱布过滤。 3、脱色:在滤液中加入0.5~1.0%的活性炭,于80℃加热20min,进行脱色和除异味,趁热抽滤(如抽滤困难可加入2%~4%的硅藻土作为助滤剂)。如果柑橘皮漂洗干净萃取液为清澈透明则不用脱色。 4、沉淀:待提取液冷却后,用稀氨水调pH至3~4。在不断搅拌下加入95%乙醇溶液,加入乙醇的量约为原体积的1.3倍,使酒精浓度达到50%~65%。 5、过滤、洗涤、烘干:用尼龙布过滤(滤液可用蒸馏法回收酒精),收集果胶,并用95%乙醇洗涤果胶2~3次,再于60~70℃干燥果胶,即为果胶产品。
向日葵杆中果胶的提取及测定
向日葵杆中果胶的提取及测定 果胶为不受添加量限制的安全食品添加剂,果胶是从植物组织中提取的一种天然高分子聚合物,是一种亲水性植物胶,属于多糖类的碳氢化合物,广泛存在于高等植物的根、茎、叶,果的细胞壁中。它是一种耐酸的胶凝剂和无毒无害的天然食品添加剂,广泛用于食品和非食品领域。由于果胶应用如此广泛,激发了人们研究的热忱,也取得了一些可喜的成绩。目前,提取果胶的原料主要采用干燥的柑橘类皮(含果胶约22.4%)、向日葵(含约17%~25%)、苹果皮(含15%)。这些原料最理想的当属向日葵。我国的向日葵资源丰富,取籽后剩下的葵盘和杆,常作为农作废弃物丢弃,既造成环境污染,又造成资源的浪费。而且向日葵中果胶含量较高,是很好的提取原料。 目前果胶的生产方法主要有酒精沉淀法和盐沉淀法。本实验采用铝盐沉淀法从向日葵杆中提取果胶。探讨了提取果胶的工艺条件,并对提取的果胶进行测定。 铝盐沉淀法提取果胶的基本原理是用酸水解成可溶性果胶酸,再加铝盐沉淀果胶,从而会有不溶于水
的果胶酸铝盐和少量的氢氧化铝以及其他杂质产生。经分离后,用盐酸溶解果胶酸铝和氢氧化铝,铝离子发生置换反应生成果胶,氢氧化铝沉淀除去,用乙醇使其沉淀,生成的果胶不溶于醇被沉淀下来,而氯化盐溶解于水溶液中,分离得果胶。 实验部分 一、材料和仪器 1.材料。 原料:向日葵杆芯的粉末(向日葵杆来自通辽郊区)。 试剂:半乳糖醛酸标准品,4%氢氧化钠(4克氢氧化钠溶于100毫升水中),无水乙醇分析纯试剂,水为两次蒸馏水,浓硫酸(98%),浓盐酸(37%),硫酸铝钾,咔唑,苯酚等均为分析纯。 2.仪器。 722s可见分光光度仪(上海精密科学仪器有限公司);电子天平(上海恒平科学仪器有限公司);SHA-BA型水浴恒温振荡器(江苏省金坛市荣华仪器制造有限公司);HH-S24型数显恒温水浴锅(金坛市大地自动化仪器厂);GZX-GF-101Ⅱ型恒温鼓风干燥箱(上海贺德实验设备有限公司);SHZ-DⅢ型循环水真空泵(巩义市予华仪器有限责任公司)。
实验室柑橘皮果胶提取
实验报告 指导老师:翁永根 应101-4 :张立群 201055501401 王聪 201055501402 崔秋丽201055501403
实验报告 一、实验目的: 1、了解柑橘果皮中的天然产物组分都有那些 2、了解果胶的性质和提取原理 3、掌握果胶的提取工艺 4、学习果胶的检验方法和果酱的制备方法 二、实验原理: 果皮中含有大量的功能性物质,如香精油、果胶、类胡萝卜素、橙皮苷、柠檬苦素等等。 果胶是一种组聚半乳糖醛酸,是由半乳糖醛酸组成的多糖混合物,含有许多甲基化的果胶酸。天然果胶是以原果胶、果胶、果胶酸的形态广泛分布于植物的果实、根、茎、叶中的多糖类高分子化合物,是细胞壁中的一种组成成分,伴随纤维素存在。果胶具有水溶性,工业上可分离其分子量约5万到30万。在适宜条件下其溶液能形成凝胶和部分发生甲基氧化,其主要成分是部分甲基化的a(1,4)—D—聚半乳糖醛酸。 在可食的植物中,有许多蔬菜、水果含有果胶。柑橘、柠檬、柚子等果皮中约含有30%的果胶,是果胶的最丰富来源。 果胶的提取主要是采用传统的无机酸提取法(酸萃取法)。
该法的原理是利用果胶在稀酸溶液中能水解的特性,将果皮中的原果胶质水解成溶性果胶,从而是果胶转到水相中,生成可溶于水的果胶。然后分离出果胶。提取液经过滤或离心后,得到的是粗果胶液,还需要进一步的纯化沉淀,本实验采用醇沉淀法。其基本原理是利用果胶不溶于醇类有机溶剂的特点,将大量的醇加入到果胶的水溶液中,形成醇—水混合溶剂将果胶沉淀出来,一般将果胶提取液浓缩,在添加60%的异丙基或乙醇,使果胶沉淀,然后离心得到果胶沉淀物,用更高浓度的异丙醇或乙醇洗涤沉淀数次再进行干燥、粉碎即可。 三、主要仪器试剂: 烧杯(150,250mL),电炉,纱布,电子天平,锥形瓶,胶头滴管,石棉网,PH试纸,玻璃棒,温度计,恒温水浴锅,蒸发皿,表面皿,洗瓶,布氏漏斗,真空泵, 柑橘皮,0.3%盐酸溶液,1%氨水,95%乙醇 四、实验步骤: 1、原材料的预处理 称取新鲜的柑橘皮40.19g用水漂洗干净。于250mL烧杯中加水约120mL,加热至90℃,将橘子皮放到烧杯中保持十分钟。取出后用水冲洗后切成尺寸大约1cm的小块,在250mL烧杯中用 50~60℃的热水漂洗,漂洗10次。 2、酸法萃取
高酯果胶特性
高酯果胶特性 果胶是在食品行业里常见的食品添加剂,主要功用是作为增稠剂,胶凝剂,稳定剂,乳化剂,起到增稠稳定,改进口感等效果。应用于果酱、烘焙馅料、固体饮料、肉制品、软糖等产品上,起到非常好的效果。 高酯果胶是果胶类型里面的其中一种,一般用作增稠剂;胶凝剂;稳定剂;乳化剂。主要是用于固形物含量较高的产品里形成凝胶,一般会使用在高糖果酱上。高酯果胶只能在可溶性固体含量高于65%和pH 在2.0 ~ 3.8之间形成凝胶。凝胶形成是在交联聚合物的交界区,其中主要是氢键和甲基之间的斥力使得糖和水可进入果胶网状物区域。高酯果胶制成的凝胶剂具有稳定的和短的结构,而且是清澈的,具有良好的风味,用于高糖果酱中特别明显。 高糖果酱的特性包括:脱水收缩少、表面光亮、容易涂抹、果肉分布均匀、可切割以及水果香气浓郁自然。然而高酯果胶就可以很好的帮助高糖果酱实现这些特性,改善口感风味,提高产品品质。
高酯果胶跟果胶一样,一般从柑橘皮、苹果皮等植物细胞中提取,其中柑橘皮中提取的果胶含量最为丰富,所以进口品牌的果胶大部分都是从柑橘皮中提取,可以拥有大规模的种植地域,产能稳定,对弄残、重金属的含量也能控制得很好。然而国内普遍使用的果胶都是从苹果皮中提取的,不仅产能不稳,而且质量控制和农残方面控制较差,导致国内很多果胶会出现控制不稳定的问题。 高酯果胶的选择取决于您想要的产品特性和生产技术,在选择果胶的时候,最好是使用从新鲜柑橘皮中提取的果胶,具有口感清新特点,不会出现皮味重,腐烂等气味。其中健科代理的意大利施华果胶就是从精选瓶中的新鲜橙皮中提取,果胶质量最好,性能最好,而且口感清爽,纯度高使用成本低,再加上价格便宜,所以性价比最高。
柑橘皮中橘皮油_果胶_橙皮苷的提取与利用
第24卷 第6期 湖 南 城 市 学 院 学 报 (自然科学) V ol.24 No.6 2003年11月 JOURNAL OF HUNAN CITY UNIVERSITY (Natural Science ) Nov. 2003 柑橘皮中橘皮油、果胶、橙皮苷的提取与利用 汤青云1,雷存喜1,谢志美2,胡舜钦2 (1.湖南城市学院 化学与环境工程系,湖南 益阳 413049;2.株洲师范高等专科学校 化学系,湖南 株洲412007) 摘 要:讨论了柑橘皮中橘皮油、果胶、橙皮苷的提取与综合利用. 关键词:柑橘皮;橘皮油;果胶;橙皮苷 中图分类号:S666;TQ028.9+6 文献标识码:A 文章编号:1672–1942(2003)06–0103–02 湖南盛产柑橘,每年产出的柑橘皮估计干重达数千吨.过去只有极少一部分柑橘皮作为中药陈皮被收购,绝大部分被白白浪费.据资料介绍,鲜柑橘皮中含油脂3%~5%,干皮中由于水分含量相对较少,含油量更高.橘皮油、色素可用水蒸气蒸馏法或溶剂萃取法提取,提油后的果皮渣还可提取果胶、色素和橙皮苷.橘皮油是很好的纯天然食品添加剂;果胶在食品、纺织、化妆品和医药上用作胶凝剂、乳化剂、增稠剂和稳定剂;橙皮苷在医药上也有作极为广泛的用途.若能充分地利用资源优势,合理开发,既可支援工、农业生产,又可增加社会财富,具有很好的经济效益、社会效益和环境效益. 1 实验部分 1.1 工艺流程 1.2 原料筛选与预处理 柑橘皮都含有油脂,在品种上不论是广柑皮、芦柑皮、椪柑皮、酸橙皮、皱皮柑皮或南橘皮、蜜橘皮,还是柚子皮、橙子皮;在颜色上不论是红色、花红,还是青色、黄色,只要没有腐烂和沤坏,都可提取油脂、果胶和橙皮苷.因此,收集或收购柑皮时,只须注意以下两点:鲜皮要求无白皮、杂质及腐烂;干皮要求无虫伤、白皮、杂质及沤黑. 收集到果皮后,先将柑、橘、柚、橙皮进行分 类,因各种果皮含油成份不同,须分开蒸馏.柚子 皮和橙子皮内层白皮含油量很低必须撕去,以免影响出油率,撕下的白皮可以并入提油后的果胶渣中提取果胶和橙皮苷.用水洗去果皮上沾附的泥沙等杂质,晾干果皮上附着的水分备用.若一次性收集的鲜皮原料很多估计不能在24 h 时内进行蒸馏时,应将果皮在阴凉通风处摊开晾干,纵有泥沙,暂时也不要洗湿,以免冲烧沤坏. 1.3 橘皮油的提取 1.3.1 蒸馏装置 鲜皮经压榨得到的果皮汁中可分离出橘皮油.压榨后的果皮渣中的橘皮油可用水蒸气蒸馏的方法提取,装置见图2.土法则可直接采用蒸馏法生产,即不要水蒸馏发生器,在原料斧的甑皮或隔板下装水,直接加热进行蒸馏,其它装置与 图2基本相似. 1.3.2 操作方法 将晾干表皮水分的果皮用压榨机压榨,榨出的果皮油静置数小时,使油水分离,油层经精制可得橘皮油,也可将压榨出来的果皮汁并入水蒸气蒸馏所得的馏液中一并处理.再将榨后的果皮碾碎或切成条状,使其中所含的果皮油易于挥发,便于蒸馏和果胶、橙皮苷的提取.干橘皮不须压榨,只须先用水浸泡数小时,其它操作方法相同. 打开原料釜上盖,在甑皮(带孔隔板)上铺一层棉布或旧棕片,把碾碎的果皮倾入原料釜中,扒平,使之紧密一致通气均匀,将上盖盖严,接通管道,勿使漏气.打开蒸汽阀门,通入水蒸气,对果皮加热,保持锅炉(或水蒸气发生器)火力,使蒸汽均匀产生.果皮中所含的油脂随水蒸气蒸出,油和水的混合蒸汽在冷凝器中冷凝成液体,流入作为接受器的油水分离器中.蒸馏时间取决于原料釜体 收稿日期:2003-03-31 作者简介:汤青云(1952-),男,湖南长沙人,高级实验师,主要从事有机合成及应用化学研究.
