联苯胺
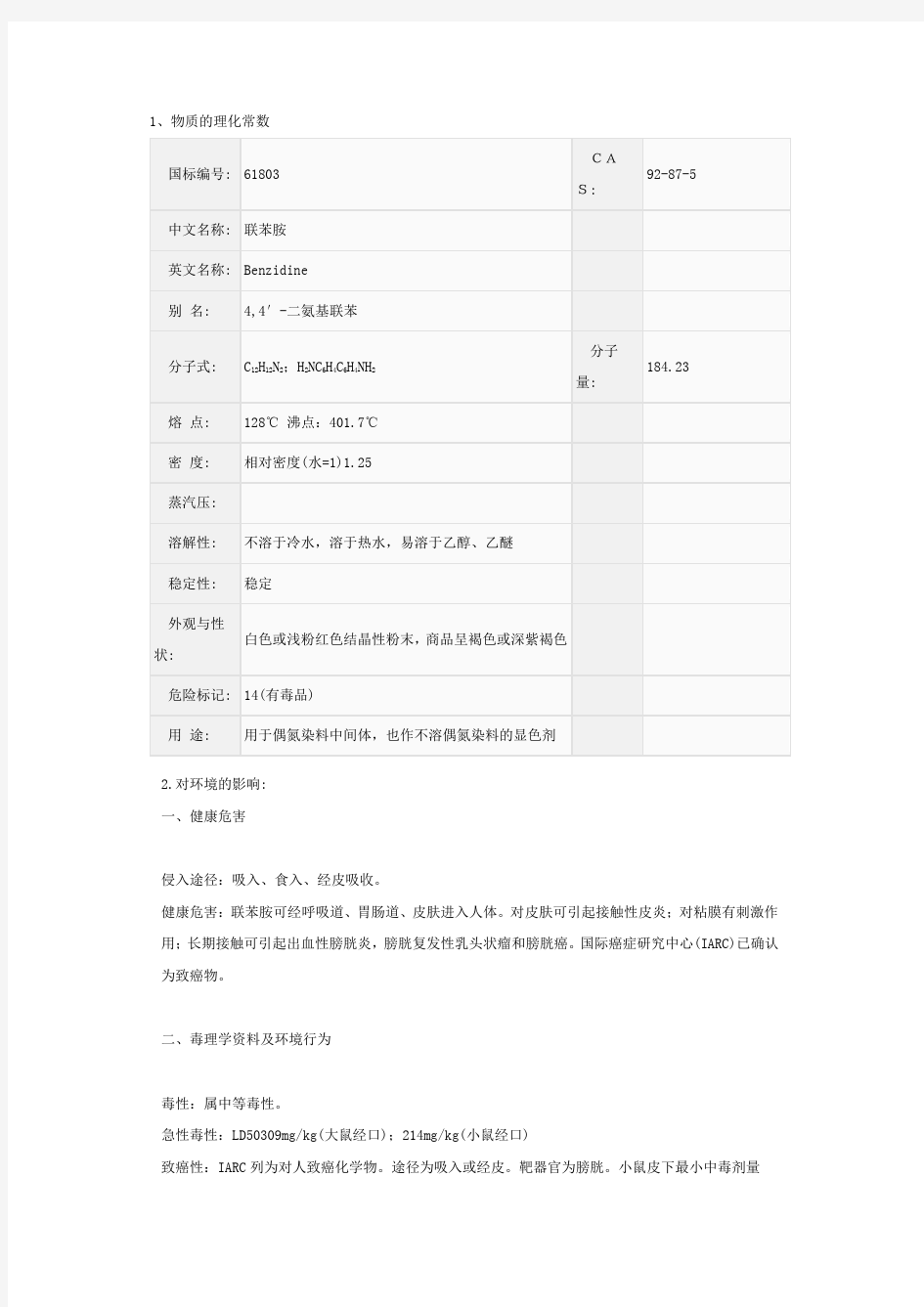

1、物质的理化常数
2.对环境的影响:
一、健康危害
侵入途径:吸入、食入、经皮吸收。
健康危害:联苯胺可经呼吸道、胃肠道、皮肤进入人体。对皮肤可引起接触性皮炎;对粘膜有刺激作用;长期接触可引起出血性膀胱炎,膀胱复发性乳头状瘤和膀胱癌。国际癌症研究中心(IARC)已确认为致癌物。
二、毒理学资料及环境行为
毒性:属中等毒性。
急性毒性:LD50309mg/kg(大鼠经口);214mg/kg(小鼠经口)
致癌性:IARC列为对人致癌化学物。途径为吸入或经皮。靶器官为膀胱。小鼠皮下最小中毒剂量
8mg/kg(35周,间断)致癌阳性;大鼠经口最小中毒剂量4500mg/kg(30日,间断)致癌阳性;人吸入最小中毒浓度18mg/m3×13年(间断)致癌阳性。
危险特性:遇明火、高热可燃。与强氧化剂可发生反应。受热分解放出有毒的氧化氮烟气。
燃烧(分解)产物:一氧化碳、二氧化碳、氧化氮。
3.现场应急监测方法:
快速比色法《化工企业空气中有害物质测定方法》,化学工业出版社
4.实验室监测方法:
高效液相色谱法(中国环境监测总站,水质)
色谱/质谱法《固体废弃物试验分析评价手册》中国环境监测总站等译
分光光度法《水和废水标准检验法》15版
5.环境标准:
中国(GHZB1-1999) 地面水环境质量标准(I、II、III类水域)0.0002mg/L
6.应急处理处置方法:
一、泄漏应急处理
隔离泄漏污染区,周围设警告标志,建议应急处理人员戴好防毒面具,穿化学防护服。不要直接接触泄漏物,避免扬尘,小心扫起,置于袋中转移至安全场所或按致癌物处理。如大量泄漏,收集回收或无害处理后废弃。
废弃物处置方法:用焚烧法。焚烧炉排出的氮氧化物通过洗涤器除去。
二、防护措施
呼吸系统防护:空气中浓度较高时,佩带防毒面具。紧急事态抢救或逃生时,应该佩带自给式呼吸器。眼睛防护:戴安全防护眼镜。
防护服:穿紧袖工作服,长统胶鞋。
手防护:戴橡皮手套。
其它:工作现场禁止吸烟、进食和饮水。及时换洗工作服。工作前后不饮洒,用温水洗澡。进行就业前和定期的体检。
三、急救措施
皮肤接触:立即脱去污染的衣着,用肥皂水及清水彻底冲洗。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水冲洗。
吸入:迅速脱离现场至空气新鲜处。呼吸困难时给输氧。呼吸停止时,立即进行人工呼吸。就医。食入:误服者给漱口,饮水,洗胃后口服活性炭,再给以导泻。就医。
灭火方法:雾状水、泡沫、二氧化碳、干粉、砂土。
细胞色素氧化酶染色液(联苯胺法)使用说明
细胞色素氧化酶染色液(联苯胺法)使用说明 货号:G2410 有效期:6个月。 产品组成: 产品名称规格保存 试剂(A):CO清除液2×50ml4℃避光 试剂(B):DAB 孵育液B1:DAB染色液45ml-20℃避光B2:DAB增强剂5ml RT B3:DAB反应液100μl RT 按B1:B2:B3=9000:1000:3混合,即为DAB孵育液,即配即用。 试剂(C):苏木素染色液50ml4℃避光 试剂(D):CO对照液1ml RT 产品说明: 细胞色素氧化酶(Cytochrome Oxidase,CO)被认为是线粒体膜固有的酶,在含有大量线粒体的细胞(如心肌、肾小管上皮以及胃壁细胞、肝细胞)内都具有高度活性。此酶活性往往作为细胞内氧化代谢的指标,亦作为线粒体的标志酶之一。 细胞色素氧化酶染色液(联苯胺法)染色原理是细胞色素氧化酶催化3,3-二氨基联苯胺(DAB)使其侧链的氨基氧化,进行反复的氧化性聚合和氧化性环化形成不溶性的棕色Phenazine 聚合物。此酶对固定剂敏感,故须用新鲜切片。 自备材料: 1、恒温培养箱
2、光学显微镜 操作步骤(仅供参考): 1、冰冻切片,厚6μm,不固定。 2、滴加CO清除液于切片上,铺满整个样品表面。 3、切片入DAB孵育液中,37℃避光孵育45~60min。 4、移去切片上的染色液,滴加CO清除液于切片上,铺满整个样品表面。 5、蒸馏水稍洗3~5s。 6、(可选)滴加苏木素染色液浅染细胞核3~5min。 7、流水冲洗10min。常规脱蜡透明,中性树胶封固。 染色结果: CO酶活性部位棕色 心肌、肾小管上皮内颗粒(线粒体)蓝色 阴性对照(可选):取新鲜配制好的DAB孵育液,按DAB孵育液:CO对照液=50:1的比例混合,即为CO对照工作液。相同切片入CO对照工作液,室温孵育30~60min,其余同上,呈阴性反应。 注意事项: 1、本染色液适用于冰冻切片,同时应减少切片在室温暴露的时间。 2、CO孵育液孵育时间因组织而异,心肌、肾孵育约20~30min,肝脏约50~60min,甲状腺滤泡上皮约2h。 3、为了您的安全和健康,请穿实验服并戴一次性手套操作。
TMB配方大全
1 。称取TMB 17.2mg(固体),加DMSO1ml 溶解,然后加醋酸钠缓冲液(0.1mol/l,pH5.5)66ml,此为底物A 底物B ,取双蒸水100ml,加30%H2O217微升 使用时A:B 液等体积混匀即可. 称取TMB 20mg(固体),先用无水乙醇10ml 溶解,充分振荡(试剂瓶要干净,干燥),加双蒸水定容到100 ml,此为底物A 底物B ,取1水柠檬酸 2.1g,无水Na2HPO4 2.82g,0.75%的过氧化氢尿素0.64ml,双蒸水定容至100ml(无须调PH值,应在4.5-5.0范围。 使用时A:B 各取5ml 混匀,可用于一块96孔板显色。 过氧化氢脲比H2O2稳定,不必如H2O2现用现配,都起供氢体的作用。 2 TMB(10mg/5ml无水l乙醇) 0.5ml 底物缓冲液10ml 0.75%过氧化氢32ul 底物缓冲液: 0.2M磷酸氢二钠25.7ml 0.1M柠檬酸24.3ml 加蒸馏水50ml TMB使用液: TMB (10mg/5ml,无水乙醇)0.5ml 底物缓冲液10ml 0.75% H2O2 32 Ul 3. TMB加入2.5ml无水酒精中,可加热至37℃~40℃直到TMB完全溶解。 将TMB配成1%浓度,4 ℃保存半年以内使用。 使用前,用pH5.0磷酸—柠檬酸底物液9.9ml加入0.1ml(1mgTMB)1%TMB液,再按每毫升TMB加入30% H2O21ul混匀后立即使用。 2NH2SO4终止后,450nm测定OD值。 4. HRP的底物: A液:0.02%H2O2 ;用0.1M柠檬酸-0.2M磷酸氢二钠,PH4.5~5.0稀释。 B液:TMB-HCl:0.4‰;用50mM柠檬酸钠,浓HCl调PH值为2.8的溶液溶解。 A液,B液各50ul使用。可使用起来显色比较缓慢,OD值较PIERCE的底物稍偏低一点。 5. 1、TMB粉末,溶于N,N-二甲基甲酰胺,配成10mg/mL。 2、底物缓冲液:0.2Mol/LNa2HPO4 25.7mL 0.1Mol/L柠檬酸24.3mL 水50mL 3、H2O2 用时10mg/mL TMB 165uL 底物缓冲液11mL
盐酸联苯胺法测定硫酸根
本文经大量试验,采用硫酸联苯胺法测定原盐中的SO42-。试样溶解后,在微酸性溶液中,加入盐酸联苯胺,与SO42-生成硫酸联苯胺: C12H8(NH2)2·2HCl + SO42-= C12H8(NH2)2·H2SO4↓ + 2Cl- 沉淀过滤并溶于热水中后,以酚酞为指示剂,用NaOH标准溶液进行滴定: C12H8(NH2)2·H2SO4+2OH- = C12H8(NH2)2 + SO42- +2H2O 1实验部分 1.1 主要试剂 1.1.1盐酸联苯胺溶液25g·L-1,25g盐酸联苯胺(AR)于瓷研钵中,加10mL 二次去离子水及10mL1:1HCl,小心研至糊状,移入盛有400mL纯水的烧杯中,搅拌溶解,用定性滤纸过滤,滤液用二次去离子水稀释至1000mL,贮于棕色试剂瓶中。 1.1.2 硫酸联苯胺溶液饱和溶液,量取10mL1:1 H2SO4溶液,加入盛有70mL 纯水的烧杯中,加1:1HCl1.0mL,25g·L-1的盐酸联苯胺溶液40mL,搅拌溶解至沉淀析出,静置5min后用定性滤纸过滤,用二次去离子水洗涤沉淀至无酸性反应。沉淀溶于水中至达到饱和,用NaOH溶液中和至呈中性。 1.1.3 其他溶液HCl溶液(1:1);H2SO4溶液(1:1);NaOH标准溶液, 0.10mol·L-1;酚酞指示剂,2g·L-1的乙醇溶液。 1.2 分析方法 1.2.1 NaOH标准溶液浓度的标定 准确称取在100~125℃烘干2h的邻苯二甲酸氢钾基准物质0.4~0.5g(准至0.0001 g)于250mL锥形瓶中,加20~30mL水,温热使之溶解,冷却后滴加2~3滴酚酞指示剂,用NaOH溶液滴定至溶液呈微红色,半分钟不褪色,即为终点(平行标定3~5份)。并按下式计算其NaOH标准溶液的浓度C : 式中:m ——称取邻苯二甲酸氢钾的质量,g ; M ——邻苯二甲酸氢钾的摩尔质量,g·mol-1 ; V ——滴定时消耗的NaOH标准溶液的体积,mL 1.2.2 试样分析 准确称取粗食盐10~12g(准至0.0001g)于400mL烧杯中,加入100mL二次去离子水溶解(如有泥、沙等杂质时,应予以过滤),加入HCl溶液10.0mL,加入20mL盐酸联苯胺溶液,搅拌后,静置10~15min,过滤,用硫酸联苯胺饱和溶液洗涤烧杯及沉淀至无酸性反应(精密pH试纸)。小心取出滤纸,展开后贴于原烧杯壁,用去离子水将沉淀冲入烧杯中,加入煮沸过的热水100~120mL,置于电炉上低温加热至沸,滴加2~3滴酚酞指示剂,在玻璃棒搅拌下,立即用标定好的NaOH标准溶液滴定至溶液呈微红色,用玻璃棒将滤纸搅碎,投入溶液中,继续用NaOH滴定至微红色,半分钟不褪色,即为终点。 1.2.3 硫酸根含量计算 可按下式计算原盐中SO42-离子的质量分数ω%: 式中:C、V—分别表示NaOH标准溶液的浓度(mol·L-1)和滴定时用去的体积,mL; M——SO42-的摩尔质量,为96g·mol-1 ; ms ——称取样品的质量,g 2 结果与讨论 2.1 测定结果的比较 本文以某盐厂的原盐为试样,分别用重量分析标准法和本法同时测定样品5
(PAS反应与联苯胺反应)
实验三PAS反应与联苯胺反应 一:实验目的: 掌握显示细胞中多糖和过氧化物酶反应的原理和方法。 二:实验原理: 1、高碘酸—希夫试剂反应简称PAS(Periodic Acid Schiff reaction)反应。组织内的多糖等都用PAS法来显示。其化学基础是利用过氧酸的氧化作用打开C—C键,将CH2OH—CH2OH变成CHO—CHO。同样,对CH2OH—CHO,CH2OH—COOH,CH2OH—CH2NH2等物质均有氧化作用而放出醛基,这种新生的醛基和无色品红作用形成紫红色化合物(见图1)。颜色的深浅与糖类的多少有关。 2、细胞内的过氧化物酶能把许多胺类化合物氧化为有色化合物(见图2),用联苯胺处理样本,细胞内的过氧化物酶能把联苯胺氧化为兰色的苯胺蓝,进而变为棕色产物,因而可以根据颜色反应来判断过氧化物酶的有无或多少。 三:实验材料与试剂 1.材料:土豆块茎、洋葱根尖或鳞茎表皮。 2.器具:显微镜、载波片、单面刀片、培养皿、镊子、染色钵、盖玻片、吸水纸。 3.试剂: (1)过碘酸酒精溶液: 过碘酸(高碘酸)0.4g 95%酒精35ml 0.2 mol/L醋酸钠5ml (即17.2g醋酸钠溶于1000ml 蒸馏水) 蒸馏水10ml 该液需保存于冰箱,包黑纸,如变黄则失效。 (2)Shiff试剂(详见指导书P75页) (3)0.1%钼酸铵溶液:称取0.1 g钼酸铵溶于100 ml 0.85%盐水 (4)联苯胺混合液(临用前配制) 联苯胺0.2g 95%乙醇100ml 3%H2022滴 (5)亚硫酸水溶液:取200ml自来水,加10ml10%的偏重亚硫酸钠水溶液和10ml1mol/L 的HCl,三者于使用前混匀。
ELISA稀释液配制
https://www.wendangku.net/doc/b62310880.html,/techniquezones/66 抗体稀释液和ELISA相关溶液的配制 1、抗体或免疫球蛋白稀释液0.01mol/L pH7.2PBS NaH2PO4·2H2O 0.39克 Na2HPO4 1.27克 NaCl 0.85克 NaN3 200mg H2O(蒸馏水)至1000ml 2、ELISA洗液及HRP标记抗体稀释液pH7.4,PBST NaCl 2.0克 KH2PO4 0.2克 Na2HPO4·12H2O 2.9克 KCl 0.2克 NaN3 0.2克 H2O 至1000ml 吐温(Tween)20 0.5ml 4°C保存备用 3、包被液(简称CB)pH9.6 Na2CO3 1.59克NaHCO3 2.93克 NaN3 0.2克 H2O 至1000ml 密封盖好,4°C存放备用 4、ELISA底物液(可溶性底物) 磷酸-柠檬酸缓冲液pH5.0 0.1mol/L柠檬酸(21.014克/100ml) 24.3ml 0.2mol/L Na2 HPO4(28.4克/1000ml) 25.7ml H2O 50ml 4°C存放备用 5、DAB底物液(不溶性底物,组化病理等)
0.05mol/L pH7.6 Tris-HCL Tris 6.05克 HCL(36%) 3.15克(约2.7ml浓HCL) H2O 至1000ml DAB为3′,3′二氧基联苯胺,不溶性底物,呈棕红色 6、DAB溶液配制:(组化及Western blot 显色) 称DAB30mg,用0.05mol/L pH7.6Trs-HCL缓冲液100ml溶解,如有沉淀,过滤后使用,一般新鲜配制使用。用前加入1%H2O2 1-1.5ml,H2O2浓度为0.01%,混均后使用。 7、3′,3′,5′,5′,-四甲基联苯胺(TMB)溶液配制: 用二甲基甲酰胺(dimethylformamide,DMF)或无水乙醇,将TMB配成1%浓度,4°C保存半年以内使用。使用前,用pH5.0磷酸-柠檬酸底物液9.9ml加入0.1ml(1mg/TMB)1%TMB液,再按每毫升TMB加入30%的H2O2 1ul,混匀后立即使用。2N H2SO4终止后,450nm测定OD值。 8、1%离子琼脂胶配制液 作免疫双相扩散,单相扩散及免疫电泳中使用。 0.05UpH8.6巴比妥钠-HCL缓冲液 巴比妥钠23.8克 1mol/L HCL 34.5ml H2O 2150ml
化妆品中4-氨基偶氮苯和联苯胺的检测方法
附件6: 化妆品中4-氨基偶氮苯和联苯胺的检测方法 1 范围 本标准规定了使用气相色谱–质谱法测定化妆品中4-氨基偶氮苯和联苯胺的含量。 本标准适用于粉、霜、露、膏、乳、油、液类化妆品中4-氨基偶氮苯和联苯胺的测定。 本标准的浓度适用范围为0.5 mg/Kg~10 mg/Kg,4-氨基偶氮苯及联苯胺的检出限(3σ)均为0.5 mg/Kg,定量下限(10σ)分别为2.0 mg/Kg、2.5 mg/Kg。 2 原理 试样在氨水-氯化铵缓冲溶液(pH = 9.5)中经叔丁基甲醚超声萃取后,使用硅胶-中性氧化铝混合填充的固相萃取小柱进行净化,叔丁基甲醚为淋洗液,浓缩后进样,经气相色谱分离、质谱检测器测定,使用保留时间、待测组分特征离子丰度比双重模式进行定性,外标法对各组分定量离子峰面积进行定量。 3 试剂及材料 除特别说明外,所有试剂均为分析纯;水为符合GB/T 6682规定的一级水。 3.1 标准物质:4-氨基偶氮苯,纯度≥99.0%。 3.2 标准物质:联苯胺,纯度≥98.5%。 3.3 正己烷:色谱纯。 3.4 甲醇:色谱纯。 3.5 叔丁基甲醚:色谱纯。 3.6 无水硫酸钠。 3.7 氯化铵。 3.8 氨水:25%。 3.9 氯化钠。 3.10 硅胶:100~200目,使用前于160 ℃下烘12 h。
3.11 中性氧化铝:100~200目,使用前于180 ℃下烘12 h。 3.12 氨水–氯化铵缓冲溶液:称取13.4 g 氯化铵、量取18.5 mL氨水于250 mL 烧杯中,加水溶解后转移至500 mL容量瓶,定容,配制成pH=9.5的缓冲溶液。 3.13 标准溶液 3.13.1 4-氨基偶氮苯标准储备溶液:准确称10.0 mg 4-氨基偶氮苯准品于10 mL 容量瓶中,加入少量甲醇溶解,并用甲醇定容至刻度,溶液浓度为1 mg/mL。将标准溶液转移到安瓿瓶中于4℃保存。 3.13.2 联苯胺标准储备溶液:准确称10.0 mg联苯胺准品于10 mL容量瓶中,加入少量甲醇溶解,并用甲醇定容至刻度,溶液浓度为1 mg/mL。将标准溶液转移到安瓿瓶中于4℃保存。 3.13.3 混合标准中间溶液:取一定量4-氨基偶氮苯和联苯胺的储备液,用甲醇稀释成混合标准中间溶液,溶液浓度为0.1 mg/mL。将混合标准中间溶液转移到安瓿瓶中于4℃保存。 3.13.4 混合标准工作液:用甲醇将一定量的混合标准中间溶液配制成相应浓度的混合标准工作液。将混合标准工作液转移至安瓿瓶中于4℃保存。 4 仪器和设备 4.1 气相色谱-质谱仪。 4.2 分析天平:感量0.0001 g。 4.3 超声波振荡器。 4.4 离心机。 4.5 氮气吹扫装置。 4.6 玻璃固相萃取柱:内径1 cm,长度10 cm。 4.7 圆底螺口玻璃离心管:50 mL。 4.8 滤膜:0.45 μm有机相滤膜。 4.9 分液漏斗振荡器。 4.10 K-D浓缩瓶:30 mL。 5 分析步骤 2
细胞色素氧化酶染色液(联苯胺法)
细胞色素氧化酶染色液(联苯胺法) 简介: 细胞色素氧化酶(Cytochrome Oxidase ,CO)被认为是线粒体膜固有的酶,在含有大量线粒体的细胞(如心肌、肾小管上皮以及胃壁细胞、肝细胞)内都具有高度活性。细胞色素氧化酶染色液(联苯胺法)染色原理是细胞色素氧化酶催化3,3-二氨基联苯胺(DAB)使其侧链的氨基氧化,进行反复的氧化性聚合和氧化性环化形成不溶性的棕色Phenazine 聚合物。此酶对固定剂敏感,故须用新鲜切片。 组成: 操作步骤(仅供参考): 2、 冰冻切片,厚6μm ,不固定。 3、 滴加CO 清除液于切片上,铺满整个样品表面。 4、 切片入DAB 孵育液中37℃避光孵育。 5、 移去切片上的染色液,滴加CO 清除液于切片上,铺满整个样品表面。 6、 蒸馏水稍洗。 7、 (可选)滴加Lea 苏木素染色液浅染细胞核。 8、 流水冲洗。常规脱蜡透明,中性树胶封固。 染色结果: CO 酶活性部位 棕色 心肌、肾小管上皮内颗粒(线粒体) 蓝色 编号 名称 DE0031 4×50ml Storage 试剂(A): CO 清除液 2×50ml 4℃ 避光 试剂(B): DAB 孵育液 B1: DAB 染色液 45ml -20℃ 避光 B2: DAB 增强剂 5ml RT B3: DAB 反应液 100μl RT 按B1:B2:B3=9000:1000:3混合,即为DAB 孵育液,即配即用。 试剂(C): Lea 苏木素染色液 50ml 4℃ 避光 试剂(D): CO 对照液 1ml RT 使用说明书 1份
注意事项: 1、本染色液适用于冰冻切片,同时应减少切片在室温暴露的时间。 2、CO孵育液孵育时间因组织而异,心肌、肾孵育约20~30min,肝脏约50~60min, 甲状腺滤泡上皮约2h。 3、为了您的安全和健康,请穿实验服并戴一次性手套操作。
高效液相色谱法测定废水中苯胺类化合物
高效液相色谱法测定废水中苯胺类化合物的实验模拟 作者:李佛军,班级:2班,学号:211103350 摘要:苯胺类化合物作为工业原料被广泛用于多种行业,它的大量使用对环境和人类的饮用水安全造成了很大的危害。本文以高效液相色谱法(HPLC)检测水中5种苯胺类化合物的方法,该方法等5种苯胺类的检出限为0.10~0.52 μg/L,回收率为70.2%~95.6%,相对标准偏差(RSD)为3.68%~8.79%,线性范围为1.0~10.0 mg/L。 关键词:苯胺类化合物;水;环境;高效液相色谱法。 Measuring the aniline compound in water experiment simulation with high performance liquid chromatography Fo jun LI Abstract:As industrial raw material,aniline compound is widely used in many industries,and it's heavy use causes great harm to environment and the safety of human's drinking water。This paper establishes the method,of measuring 5 kinds of aniline compound in water with HPLC。In this method,for the 5 kinds of aniline categories,detection limit is 0.10~0.52,recovery rate is 70.2%-95.6%,relative standard deviation (RSD) is3.68%-8.79%,linear range is 1.0 - 10.0 mg/L。 Keywords:aniline compound;water;environment;high performance liquid chromatography。 一、前言 1.1 技术发展 苯胺类化合物是致癌物质,它对环境造成的污染随着它的广泛应用而日趋严重,因此对这类化合物的监测已越来越受到重视。美国、日本等国把苯胺类化合物列入主要监测项目或优先监测的污染物黑名单[1]。在我国,苯胺类化合物也被列为环境重点污染物并制定了最高容许排放浓度。在已颁布的污水综合排放标准(GB 8978-88)中规定了苯胺类化合物的排放标准,并制订了分析苯胺类化合物的标准方法——萘乙二胺偶氮光度法[2],但不足的是该方法只能分析总的苯胺类化合物,不能对单个的苯胺类化合物进行定性和定量分析。高效液相色谱法能弥补这个不足。目前,用高效液相色谱法测定废水中苯胺类化合物已有报道,但未见同时测定苯胺、对硝基苯胺、间硝基苯胺、联苯胺、邻硝基苯胺、2,4-二硝基苯胺、Ν,Ν-二甲基苯胺等7种物质的报道[3]。我们用更简单、快速、准确的方法来测定这7种物质。
HZ HJ SZ 水质 硒的测定 ' 二氨基联苯胺分光光度法
HZHJSZ00123 水质硒的测定 分光光度法 HZ-HJ-SZ-0123 水质3, 3’-二氨基联苯胺分光光度法 1 范围 本方法测硒的最低检出浓度为2.5ìg/L 本方法已用于各种天然水硫酸制造 水中常见离子一般不干扰本法测定硒铜 对本法有干扰EDTA消除3 因此水样用混合酸液消解时一定要加热至大量硝酸被赶掉 2 原理 3, 3’-二氨基联苯胺(3,3’-Diaminobenzidine)在酸性条件下与四价硒反应生成黄色化合物 进行比色定量将四价以下的无机和有机硒氧化至四价硒然后测定总硒含量 准确称取纯度加入2mL高氯酸稍冷后加入少量水和8.4mL盐酸 然后转移至1000mL容量瓶此溶液每毫升含硒100.0ìg ????±ê×??ü±?èüòoó?0.1mol/L盐酸溶液稀释成每毫升含硒1.0ìg 3.3 氢氧化钠溶液 3.4 1+1硝酸-高氯酸 3.5 1+4盐酸溶液 3.6 甲酚红溶液将20mg甲酚红(C22H18O5S)溶于少量水中加1滴氨水 加水稀释至100mL ??10g Na2?óèèèü?a HCl)及10mL甲酚红溶液(3.6)贮于冰箱内 3.8 3-二氨基联苯胺盐酸盐溶液因此溶液易变质 3.9 甲苯 5 试样制备 取200mL或适量水样(含硒量为1~10ìg)置250mL具塞锥形瓶中 3.3加热浓缩至约10mL(注意取下放冷高氯酸5mL è???继续加热至再冒浓白烟时放冷备测 于上述瓶中加入混合试液20mLó?10%(m/V)氢氧化钠溶液调pH至2~3±?òaê±Dèó?pH0.5~5.0精密pH试纸检查3 摇匀
6.1.2 萃取 必要时需用pH5.4~7.0的精密pH试纸检查振摇2min ′y·?2?oó???×±?2?·?è?10mL具塞刻度管中待测 用30mm比色皿以甲苯作参比并作空白校正 分别加入0 1.00 3.007.00及10.00mL 硒标准使用溶液以下按照上述第5条和6.1进行操作 7 结果计算 c硒(Se m由校准曲线查得的硒量(ìg) 8 精密度和准确度 单一实验室用本法测定545ìg/L硒的标准溶液的相对标准偏差分别为31 5.5%?????????°á?óí3§o???á??a?′?ì3??á21.3ìg/L 对自来水矿泉水 加入2~5ìg硒 注意事项 其pH值在6~7之间可不必调节 因水样pH太低蒸发时可能会使低价硒损失浓缩后过碱 影响样品消解效果 高氯酸消解不完全时杂质荧光高所以消解快到终点时不要过多摇动瓶应立即取下 前者是由桃红色变为黄色 pH 3~6为黄色3二氨基联苯铵在pH2~3条件下反应 用甲苯萃取时不可过高因此采用由黄色变成浅橙黄色(黄色刚刚消失)为宜 放出水相后振摇分层后 9 参考文献 ±à?ˉ?á±àμúèy°?pp. 202~204 ±±??
PH1138 过氧化物酶染色液联苯胺法实验方法
PH1138|过氧化物酶染色液(联苯胺法) Peroxidase Staining Solution Catalog No:PH1138Size:?4×10mL|?4×20mL Store at RT 过氧化物酶(Peroxidase,简称POX或MPO)是由微生物或植物所产生的一类能催化很多反应的以过氧化氢为电子受体催化底物氧化的酶氧化还原酶,主要存在于细胞的过氧化物酶体中,以铁卟啉为辅基,可催化过氧化氢氧化酚类和胺类化合物,具有消除过氧化氢和酚类、胺类毒性的双重作用。 过氧化物酶染色液(联苯胺法)是ICSH推荐采用的POX染色液,其原理是细胞内的过氧化物酶能将无色的3,3-二氨基联苯胺(DAB)的氢原子传递给过氧化氢,使前者催化成有色染料沉积在细胞质中的POX所在部位。该染液可用于血液、骨髓或细胞涂片过氧化物酶染色,POX活性部位呈棕黄色。 试剂组分 Components4×10ml4×20ml Storage 试剂(A):BFA固定液10ml20ml4℃避光 B1:DAB染色液10ml20ml4℃避光 试剂(B):POX孵育液 B2:DAB氧化剂2×100μl4×100μl RT 临用前,按B1:B2=1000:1比例混合,即为POX孵育液,即配即用 试剂(C):WG染色液10ml20ml RT避光 试剂(D):WG Buffer10ml20ml RT Manual1份 有效期12个月 1、血液、骨髓或细胞涂片滴加预冷的BFA固定液,4℃固定30~60s,稍水洗。 2、滴加配制好的POX孵育液,室温(20~25℃)避光孵育10~15min,水洗2min。 3、滴加WG染色液,孵育30~60s。 4、直接滴加等量WG buffer,染色10~15min。 5、水洗、晾干、镜检。 染色结果 POX活性部位棕黄色 细胞核蓝色 粒细胞系除早期原粒细胞阴性外,分化好的原粒细胞以下阶段细胞随细胞成熟而阳性反应增强,衰老中性粒细胞反应程度减弱单核细胞系弱阳性,淋巴细胞系为阴性。浆细胞及巨核细胞均为阴性。嗜酸性粒细胞和Auer小体呈强阳性反应。
二甲氧基联苯胺监测分析方法
3,3?-甲氧基联苯胺 1简介 英文名称:3,3'-Dimethoxybenzidine CAS登记号:119-90-4 2监测分析方法 3,3?-甲氧基联苯胺常见于纺织品中,本方法为对纺织品中的3,3?-甲氧基联苯胺进行测定的方法。 2.1 试剂及分析方法 2.1.1 标准样品溶液的制备 称取3,3?-甲氧基联苯胺标准样品,用甲醇配制成浓度为1000mg/L的标准储备液,并用甲醇稀释成各种浓度的标准溶液。 2.1.2 样品前处理、萃取及浓缩 取有代表性试样,剪成约5 mm ×5 mm的小片,混合。从混合样中称取1.0g,精确至0.01g,置于反应器中,加入17 mL预热到(70±2)℃的柠檬酸盐缓冲溶液,将反应器密闭,用力振摇,使所有试样浸于液体中,置于已恒温至(70±2)℃的水浴中保温30 min,使所有的试样充分润湿。然后,打开反应器,加入3. 0 mL连二亚硫酸钠溶液,并立即密闭振摇,将反应器再于(70士2)℃水浴中保温30 min,取出后2 min内冷却到室温。 用玻璃棒挤压反应器中试样,将反应液全部倒人提取柱内,任其吸附15 min,用4× 20 mL 乙醚分四次洗提反应器中的试样,每次需混合乙醚和试样,然后将乙醚洗液灌人提取柱中,控制流速,收集乙醚提取液于圆底烧瓶中。 将上述收集的盛有乙醚提取液的圆底烧瓶置于真空旋转蒸发器上,于35℃左右的温度低真空下浓缩至近1 mL,再用缓氮气流驱除乙醚溶液,使其浓缩至近干(其中各种溶液的制备标准参见GB/T17952-2011)。 2.2 分析方法 2.2.1 HPLC/DAD分析方法 a)色谱柱:ODS C18 (250 mm × 4. 6 mm ×5 μm),或相当者; b)流量:0. 8 mL/min-1. 0 mL/min; c)柱温:40℃;
101.硒的测定(3,3'-二氨基联苯胺光度法)
硒的测定(3,3’-二氨基联苯胺光度法) 一、填空题 1.测定硒的水样采集后,最好尽快分析,否则必须贮于经1+1盐酸或1+1硝酸浸泡4h以上,然后用大量清洁水、纯水冲洗干净的玻璃瓶或塑料瓶中。 2.强氧化剂能将3,3’-二氨基联苯胺试剂氧化产生棕红色,因此水样用混合酸液消解时一定要加热至大量硝酸被赶走,少量的强氧化剂可用盐酸羟胺消除。 3. 3,3’-二氨基联苯胺光度法适用于各种天然水、饮用水及炼油、硫酸制造、特种玻璃等工业废水中总硒的测定,方法最低检出限为2.5μg/L,测定上限为50μg/L。 4.3,3’-二氨基联苯胺光度法测定硒时,用30mm比色皿,于450nm波长处,以甲苯作参比,测量吸光度,并做空白校正。 5.显色时,在预处理后的样品瓶中加入混合试液20ml,溶液呈桃红色,用10%(m/V)氢氧化钠溶液调pH值至2—3,溶液呈浅橙黄色。加入3,3’-二氨基联苯胺溶液3.5ml,摇匀,在暗处放置30min。 二、选择题 1.水样浓缩之前应先测一下pH值,若其pH值在6—7之间可不必调节。 2. 3,3’-二氨基联苯胺光度法测定硒灵敏度低,适合于测定含硒量在5μg/L以上的水样。 三、判断题 1.微量硒是生物必需的营养元素,但过量的硒却又能引起中毒。(√) 2. 3,3’-二氨基联苯胺溶液配制后可长期保存使用。(×) 3.用甲苯萃取时,溶液pH值应控制在6—7,不可过高,否则会使测定结果偏低。(×) 四、问答题 1. 3,3’-二氨基联苯胺光度法测定硒的原理是什么? 答:3,3’-二氨基联苯胺在酸性条件下与四价硒反应生成黄色化合物,在pH7左右时能被甲苯萃取,进行比色定量。水样需要经混合酸液消解后,将四价以下的无机和有机硒氧化至四价硒,再盐酸反应将六价硒还原至四价硒,然后测定总硒含量。 2.萃取时若产生乳化现象应怎样处理? 答:萃取时若产生乳化现象,放出水相后,加入少许无水硫酸钠,振摇分层后,从分液漏斗上口倾出甲苯层。 3.怎样去除较大量的铁、铜、钼及钒等重金属离子的干扰? 答:若存在较大量的铁、铜、钼及钒等重金属离子时,可用Na2-EDTA消除。 1
固相萃取-高效液相色谱法同时测定水中苯胺和联苯胺
固相萃取-高效液相色谱法同时测定饮用水中苯胺和联苯胺 摘要:用WatersOasisMCX固相萃取小柱富集水中的苯胺和联苯胺,以2%氨水-甲醇混合溶液为洗脱液,采用高效液相色谱法DAD检测器在285nm波长下测定。苯胺和联苯胺分别在0mg/L~100mg/L和0mg/L~10.0mg/L范围内线性良好,检出限分别为0.3μg/L和0.1μg/L,饮用水加标平行测定6次的RSD分别为0.9%和0.3%,回收率分别为98.3%~99.1%和97.6%~102%。 关键词:苯胺;联苯胺;固相萃取;高效液相色谱法;饮用水 苯胺、联苯胺都是染料工业的中间体。苯胺可通过呼吸道、消化道被人体摄入,也可通过皮肤吸收进入人体,对人类的毒害主要是使氧和血红蛋白变为高铁血红蛋白,影响组织细胞供氧造成窒息。4,4-二氨基联苯俗称联苯胺,分子式为(C6H4NH2)2,系联苯的衍生物之一。联苯胺及其盐都是有毒物质,可以通过皮肤进入人体,引起接触性皮炎,刺激黏膜,损坏肝和肾脏,且会造成膀胱癌和胰腺癌,为第一类致癌物。测定水中苯胺和联苯胺需对样品预处理,常用的富集方法有液液萃取、固相萃取和固相微萃取等。近年来固相萃取技术取得了快速发展,可实现水中痕量苯胺和联苯胺的高倍富集与分离。分离分析技术主要有紫外扫描分光光度法[1]、液质联用色谱法[1-4]、气相色谱 法(GC)[5-7]、高效液相色谱法(HPLC)[8-10]。紫 外扫描分光光度法干扰较大,检出限较高;液质联用色谱法对仪器和检测人员的要求都比较高;GC法分析前需对联苯胺衍生,且衍生物受热易分解,会导致准确度和重现性差;HPLC法操作简便,稳定性好[1-4,8-10]。今采用固相萃取富集与分离, HPLC法同时测定饮用水中的苯胺和联苯胺,结果令人满意。
过氧化物酶染色液(联苯胺法)
南京森贝伽生物科技有限公司 网址:https://www.wendangku.net/doc/b62310880.html,/ 第1页 仅供科研 版本号:171024 过氧化物酶染色液(联苯胺法) 【产品组成】 【保存条件】 4℃,避光 ,6个月 【产品概述】 过氧化物酶(Peroxidase ,简称POX 或MPO)是由微生物或植物所产生的一类能催化很多反应的以过氧化氢为电子受体催化底物氧化的酶氧化还原酶,主要存在于细胞的过氧化物酶体中,以铁卟啉为辅基,可催化过氧化氢氧化酚类和胺类化合物,具有消除过氧化氢和酚类、胺类毒性的双重作用。 过氧化物酶染色液(联苯胺法)是ICSH 推荐采用的POX 染色液,其原理是细胞内的过氧化物酶能将无色的3,3-二氨基联苯胺(DAB)的氢原子传递给过氧化氢,使前者催化成有色染料沉积在细胞质中的POX 所在部位。该染液可用于血液、骨髓或细胞涂片过氧化物酶染色,POX 活性部位呈棕黄色。 【使用方法】 1、血液、骨髓或细胞涂片滴加预冷的BFA 固定液,4℃固定30~60s ,稍水洗。 2、滴加配制好的POX 孵育液,室温(20~25℃)避光孵育10~15min ,水洗2min 。 3、滴加WG 染色液,孵育30~60s 。 4、直接滴加等量WGbuffer ,染色10~15min 。 5、水洗、晾干、镜检。 【染色结果】 粒细胞系除早期原粒细胞阴性外,分化好的原粒细胞以下阶段细胞随细胞成熟而阳性反应增强,衰老中性粒细胞反应程度减弱单核细胞系弱阳性,淋巴细胞系为阴性。浆细胞及巨核细胞均为阴性。嗜酸性粒细胞和Auer 小体呈强阳性反应。 阳性反应强度的判断:
【临床意义】 1、急性粒细胞白血病晚期的原粒细胞呈阳性,颗粒较少且大。 2、急性单核白血病细胞呈阴性或弱阳性,颗粒小且稀疏。 3、单核急性白血病呈阴性或弱阳性。 4、急性早幼粒白血病呈强阳性,某些早幼粒细胞呈阳性,恶性组织细胞呈阴性。 5、急性淋巴细胞白血病呈阴性。 【注意事项】 1、血液或骨髓涂片应新鲜,薄厚适宜,及时固定,否则会影响酶的活性。 2、POX孵育液易失效或降低阳性强度,即配即用,不宜久置。 3、样本在未染色前切勿接触氧化剂类物质,以免细胞内的过氧化物酶被抑制。 4、每次染色时,应采取健康人末梢血或骨髓涂片作为阴性对照。 5、为了您的安全和健康,请穿实验服并戴一次性手套操作。 第2页 南京森贝伽生物科技有限公司网址:https://www.wendangku.net/doc/b62310880.html,/
缓冲液的配制
Elisa 相关试剂的配制 1、抗体或免疫球蛋白稀释液0.01mol/L pH7.2PBS NaH2PO4·2H2O——0.39克;Na2HPO4——1.27克;NaCl——0.85克;NaN3——200 mg;H2O(蒸馏水)至1000ml 2、ELISA洗液及HRP标记抗体稀释液PH7.4,PBST NaCl——2.0克;KH2PO4——0.2克;Na2HPO4·12H2O——2.9克;KCl——0.2克;NaN3——0.2克;H2O至1000ml 吐温(Tween)20 0.5ml; 4°C保存备用 3、包被液(简称CB)pH9.6 Na2CO3——1.59克;NaHCO3——2.93克;NaN3——0.2克;H2O至1000ml 密封盖好,4°C存放备用 4、ELISA底物液(可溶性底物) 磷酸-柠檬酸缓冲液pH5.0 0.1mol/L柠檬酸(21.014克/100ML)——24.3ml;0.2mol/L Na2 HPO4(28.4克/L)——25.7ml;H2O ——50ml; 4°C存放备用 5、DAB底物液(不溶性底物,组化病理等)0.05mol/L pH7.6 tris-HCL Tris——6.05克;HCL(36%)——3.15克(约2.7ml浓HCL);H2O 至1000ml DAB为3′,3′二氧基联苯胺,不溶性底物,呈棕红色 ELISA试剂配制及实验流程 是酶联接免疫吸附剂测定(( Enzyme-Linked Immunosorbnent Assay )的简称。以双抗体夹心法举例说明。 试剂配制: (1) 包被缓冲液(PH9.6 +0.2 0.05M碳酸盐缓冲液): Na2CO3——1.59g ;NaHCO3 ——2.93g ;加蒸馏水至1000ml。(用时稀释成1x,加0.1%BSA) (2)洗涤缓冲液(PH7.4 0.15M PBST):0.05%Tween-20——0.5ml;加在PBS缓冲液1000ml 中。PBS缓冲液: KH2PO4——0.2g ;Na2PO4·12H2O——2.9g ;NaCl——8g ;KCl——0.2g;加蒸馏水至1000ml。 (3)封闭缓冲液:牛血清白蛋白(BSA)2%——2g ;(或5%脱脂奶粉)加洗涤缓冲液100ml。(4)稀释液:牛血清白蛋白 0.1 % ——0.1g ;加PBS 缓冲液100ml。 (5)底物缓冲液(PH5.0):0.2M Na2HPO4(无水28.4g/L,带12结晶水71.7g/L) 取25.7ml 0.1M 柠檬酸(无水19.2g/L,带1结晶水21.01g/L)取24.3ml;加蒸馏水至100ml。 (或Na2HPO4·12H2O——1.84g ;柠檬酸·H2O ——0.51g 加蒸馏水至100ml) (6)TMB(四甲基联苯胺)显色液(显蓝色):TMB(2mg/ml水)——0.05ml;底物缓冲液——0.95ml; 30% H2O2 ——0.001ml ;总体积1ml。 (7) 或配OPD(邻苯二胺)显色液(显黄棕色)(现配避光):OPD(干粉)——0.004g ;底物缓冲液——10ml ;30% H2O2 ——0.015ml ;总体积——10ml。 (8)终止液(2M H2SO4):在178.3ml水中,逐滴加入浓硫酸(18M,约98%)21.7ml,边加边摇。操作步骤: 1. 包被:用包被液将抗体(一抗)稀释至蛋白质含量为1~10μg/ml。在每板的反应孔中加0.1ml,4℃过夜(或37℃温育2~3小时)。次日,弃去孔内溶 液,用洗涤液冲洗3次,中间振荡。(简称洗涤,下同)。 2. 封闭:加0.3ml封闭液于上述已包被之反应孔中,置37℃温育2小时。然后洗涤3次
联苯胺
1、物质的理化常数 2.对环境的影响: 一、健康危害 侵入途径:吸入、食入、经皮吸收。 健康危害:联苯胺可经呼吸道、胃肠道、皮肤进入人体。对皮肤可引起接触性皮炎;对粘膜有刺激作用;长期接触可引起出血性膀胱炎,膀胱复发性乳头状瘤和膀胱癌。国际癌症研究中心(IARC)已确认为致癌物。 二、毒理学资料及环境行为 毒性:属中等毒性。 急性毒性:LD50309mg/kg(大鼠经口);214mg/kg(小鼠经口) 致癌性:IARC列为对人致癌化学物。途径为吸入或经皮。靶器官为膀胱。小鼠皮下最小中毒剂量
8mg/kg(35周,间断)致癌阳性;大鼠经口最小中毒剂量4500mg/kg(30日,间断)致癌阳性;人吸入最小中毒浓度18mg/m3×13年(间断)致癌阳性。 危险特性:遇明火、高热可燃。与强氧化剂可发生反应。受热分解放出有毒的氧化氮烟气。 燃烧(分解)产物:一氧化碳、二氧化碳、氧化氮。 3.现场应急监测方法: 快速比色法《化工企业空气中有害物质测定方法》,化学工业出版社 4.实验室监测方法: 高效液相色谱法(中国环境监测总站,水质) 色谱/质谱法《固体废弃物试验分析评价手册》中国环境监测总站等译 分光光度法《水和废水标准检验法》15版 5.环境标准: 中国(GHZB1-1999) 地面水环境质量标准(I、II、III类水域)0.0002mg/L 6.应急处理处置方法: 一、泄漏应急处理 隔离泄漏污染区,周围设警告标志,建议应急处理人员戴好防毒面具,穿化学防护服。不要直接接触泄漏物,避免扬尘,小心扫起,置于袋中转移至安全场所或按致癌物处理。如大量泄漏,收集回收或无害处理后废弃。 废弃物处置方法:用焚烧法。焚烧炉排出的氮氧化物通过洗涤器除去。 二、防护措施 呼吸系统防护:空气中浓度较高时,佩带防毒面具。紧急事态抢救或逃生时,应该佩带自给式呼吸器。眼睛防护:戴安全防护眼镜。 防护服:穿紧袖工作服,长统胶鞋。 手防护:戴橡皮手套。 其它:工作现场禁止吸烟、进食和饮水。及时换洗工作服。工作前后不饮洒,用温水洗澡。进行就业前和定期的体检。
四甲基联苯胺
3 , 3 ′, 5 , 5 ′-四甲基联苯胺| 54827-17-7|显现法及应用注意事项 摘要:血手印是有色的手印,经常出现于杀人、抢劫、强奸等重特大暴力性案件中,通常情况下清晰的血手印是无须再行显现处理的,但有些潜血手印则需要进行处理,增强反差和显现。实际工作中我们常用的是四甲基联苯胺。 关键词:3,3′,5,5′-四甲基联苯胺(TMB),3 , 3 ′, 5 , 5 ′- 四甲基联苯胺显现法,应用注意事项 前言 3,3′,5,5′-四甲基联苯胺,白色或浅黄色结晶,熔点168.0-171.0℃,CAS:54827-17-7,[1]是一种新型安全的色原试剂,与传统的色原试剂如联苯胺、邻联甲苯胺及邻苯二胺等相比较,具有检测灵敏度高、稳定性好等优点,而且使用安全,无致癌、致突变作用。目前3,3′,5,5′-四甲基联苯胺已在逐步取代强致癌物联苯胺和其他致癌性的联苯胺衍生物,应用于临床化验、法医检验、刑事侦破及环境监测领域。尤其在临床生化检验方面,3,3′,5,5′-四甲基联苯胺作为过氧化酶的新底物,在酶免疫分析法(EIA)和酶联免疫吸附检验法(ELISA)中获得了广泛的应用。 1 3 , 3 ′, 5 , 5 ′- 四甲基联苯胺显现法[2] 刑事案件现场上经常遇到因盗窃、强奸、抢劫、绑架等原因发生的行凶杀人案, 在这些手段残忍、性质恶劣、影响极坏的杀人命案中, 在被害人的常用品、衣物、周围环境以及作案工具上经常会遗留下犯罪嫌疑人的血手印或潜血手印,这就给我们在现场勘查中提取血手印提供了可能。近年来, 各地在重、特大案件现场进行潜血手印的显现处理时, 都普遍采用了低毒安全的四甲基联苯胺显现法。 通常我们大都采用无水乙醇作为溶剂配制四甲基联苯胺显现液, 通常的配方为: 甲液: 四甲基联苯胺1- 1.2g, 无水乙醇100ml; 乙液: 3%过氧化氢(H2O2)。配制浓度: 甲: 乙= 5: 1, 即甲液100ml, 乙液20ml。对渗透性客体显现前, 如各种纺织品、本色木、浅色纸张等物体上的潜血手印, 传统的操作是在疑有潜血手印的部位用无水乙醇多次固定, 然后用四甲基联苯胺显现液进行显现, 但是在实际操作中经常发现显现出的手印只有轮廓, 纹线模糊不清等现象, 显现效果不够理想。笔者经反复试验摸索, 发现用无水甲醇替代无水乙醇对潜血手印进行固定, 改进潜血手印的固定剂, 显现效果较好。这种方法经多次验证, 与传统固定剂无水乙醇相比, 用无水甲醇固定显现出的手印有纹线清晰、不易扩散等优点。 ( 一) 无水甲醇是一种蛋白质变性剂, 且易挥发, 可使潜血手印中蛋白质快速凝固变性, 减少药液与潜血手印作用时间, 避免长时间浸泡使潜血手印扩散而造成显出的手印模糊不清, 同时提高手印显现速度, 并易于操作, 适合在实际工作中应用。 ( 二) 过氧化氢极易挥发, 所以新购的过氧化氢配制药液时的浓度可小些, 放置很久的过氧化氢配制药液时的浓度可大些。同时, 其浓度的大小要按检材上的潜血部位血清的多少与承痕体的性质而定。一般来说, 渗透性的客体使用过氧化氢溶液的浓度要小些, 非渗透性客体使用的过氧化氢溶液浓度要大些。 ( 三) 在显现出手印的部位, 往往潜血血痕较多, 影响显出手印的反差。直接拍照有时得不到满意效果, 可采用透明胶带纸直接沾取, 贴于光滑的白纸上, 使手印反差增大。 ( 四) 对于尸体皮肤显出的潜血手印, 用直接照相方法固定提取。潜血手印底色有影响时,往往是反差小, 效果差, 而且, 拍照常常受到现场环境的影响, 极不方便。用透明胶纸沾取后,贴于光滑白纸上, 可以减轻手印底色影响, 增大反差。但用透明胶纸提取时, 必须要等显现出的手印处的皮肤干燥后, 方可使用, 且在沾取时,要防止皮肤伸缩变形, 影响特征。 2 应用四甲基联苯胺应注意的两个问题[3] (一)要注意区别血手印是人血还是动物血形成 四甲基联苯胺的反应原理是利用血液中含有的过氧化氢酶和血卟啉,而动物血和人血一样,都
联苯胺的测定 气相色谱质谱法 作业指导书
水质联苯胺的测定气相色谱质谱法 作业指导书 XX省环境监测中心 2011.5
1 方法依据和适用范围 本作业指导书编制依据:USEPA8270D-2007和气相色谱质谱法《水和废水监测分析方法》第四版。 本方法适用于分析地表水、地下水、生活污水和工业废水中联苯胺的气相色谱-质谱法。 本方法的检出限为0.1ug/L。 2 方法原理 水样采用液液萃取的方法,在碱中性和酸性的条件下,用二氯甲烷分别对水样进行萃取,来分析地表水、地下水、废水等样品中的联苯胺,萃取液经无水硫酸钠脱水及浓缩器浓缩后,用气相色谱质谱法(GC/MS)分析。色谱峰按保留时间和目标化合物的特征离子定性,内标法定量,联苯胺的特征离子见表3。 3干扰和消除 3.1当分析高浓度和连续分析低浓度的样品时可能由于过载而引起污染。进样前需用溶剂清洗注射器,在分析了一个高浓度的样品后,后续分析样品应考虑高浓度样品可能存在的干扰,对后续样品中出现的相似的分析组分应重新分析,以确保不是污染引入的。 3.2联苯胺在溶剂浓缩时可能会发生氧化反应而损失,其色谱特性也较差。 4 试剂准备 除非另有说明,分析时均使用符合国家标准的分析纯试剂和蒸馏水。 4.1 二氯甲烷:农残级。 4.2 无水硫酸钠:无水硫酸钠需在500℃高温4小时,除去干扰后,保存在干燥器内。 4.3硫酸(1+3)。 4.4 氢氧化钠。 4.5 联苯胺标准液:ρ=2000μg/mL。 可以用联苯胺的纯物质用溶剂溶解配制,也可以用混合的标样稀释后使用。现采用进口标样(M-625C-1-40X)为联苯胺标准储备液。
4.6 内标化合物:ρ=2000μg/mL。 市售有证标准品,一般以二氯甲烷为溶剂,共6个:1,4-二氯苯-d 4、萘-d 8 、 苊-d 10、菲-d 10 、屈-d 12 、苝-d 12 。每个用于分析的1mL萃取物中应加入5μL内标 溶液,使萃取物中内标的浓度为10μg/mL。 4.7 代用品:ρ=2000μg/mL。 市售有证标准品,一般以二氯甲烷为溶剂,共8个:2-氟酚、酚-d 5 、2-氯 酚-d 4、1,2-二氯酚-d 4 、硝基苯-d 5 、、2-氟联二苯、三联苯- d 14 、2,4,6-三溴 酚。根据标准品计算加入量,使样品中代用品的浓度为20μg/mL。 4.8 标准调机化合物DFTPP(十氟三苯基磷酸酯) 4.9载气:氦气,高纯(99.999%),用净化管净化。 5仪器和设备 5.1气相色谱仪:连接带EI源的四极杆质谱仪。 5.2自动进样塔:配10μL微量注射器。 5.3色谱柱:固定相为5%苯基-95%甲基聚硅氧烷30m0.25mm的熔融石英毛细 柱液膜厚度0.25μm或同等效果的其他型号色谱柱均可。 5.4吹氮浓缩仪:配有1.00mL刻度的浓缩管。 5.5分液漏斗:2000mL,具聚四氟乙烯旋塞。 5.6 250mL具塞锥形瓶 6. 样品 6.1 样品的采集与保存 样品必须采集在具聚四氟乙烯内衬盖的棕色玻璃容器中,采样后应尽快完成萃取,否则应在4℃冰箱中保存,保存时间不超过7天。萃取后的浓缩液应在40d 内分析完毕。 6.2 试样的制备 6.2.1 水样预处理依据 USEPA3510和《水和废水监测分析方法》第四版,液液萃取方法。 取1000ml均匀水样于2000ml分液漏斗,将水样的pH值调到 9-10,加入30mL 二氯甲烷到水样中,振摇萃取10min,在萃取时注意放气。然后静置分层,从分液漏斗中放出有机相,收集用在锥形瓶中,重复以上萃取步骤两次,将萃取液合
- 联苯胺重排的反应机理_许家喜2013
- (PAS反应与联苯胺反应)
- 固相萃取-高效液相色谱法同时测定水中苯胺和联苯胺
- 细胞色素氧化酶染色液(联苯胺法)
- PH1138 过氧化物酶染色液联苯胺法实验方法
- 实验三、细胞内过氧化物酶的显示——联苯胺反应
- 细胞色素氧化酶染色液(联苯胺法)使用说明
- 过氧化物酶染色液(联苯胺法)
- 过氧化物酶染色液(联苯胺法)使用说明
- 盐酸联苯胺法测定硫酸根
- 联苯胺92-87-5
- 粪便隐血试验单克隆抗体法与联苯胺法的比较
- 联苯胺的测定 气相色谱质谱法 作业指导书
- 细胞色素氧化酶染色液(联苯胺法)
- 联苯胺
- 过氧化物酶染色液(联苯胺法)
- 液液萃取-高效液相色谱法测定水中的苯胺和联苯胺
