化学方程式计算导学案

班级学习小组姓名阳光总在风雨后,请相信有彩虹
4、变式练习
实验室需要64g氧气需要秤取多少克高锰酸钾进行反应?
5、强化练习
工业上电解氧化铝制取金属铝的化学方程式是
通电
2Al2O3 ===== 4Al + 3O2↑
“完全电解10t氧化铝可以得到多少吨单质铝?”(你还能用什么方法进行解答)
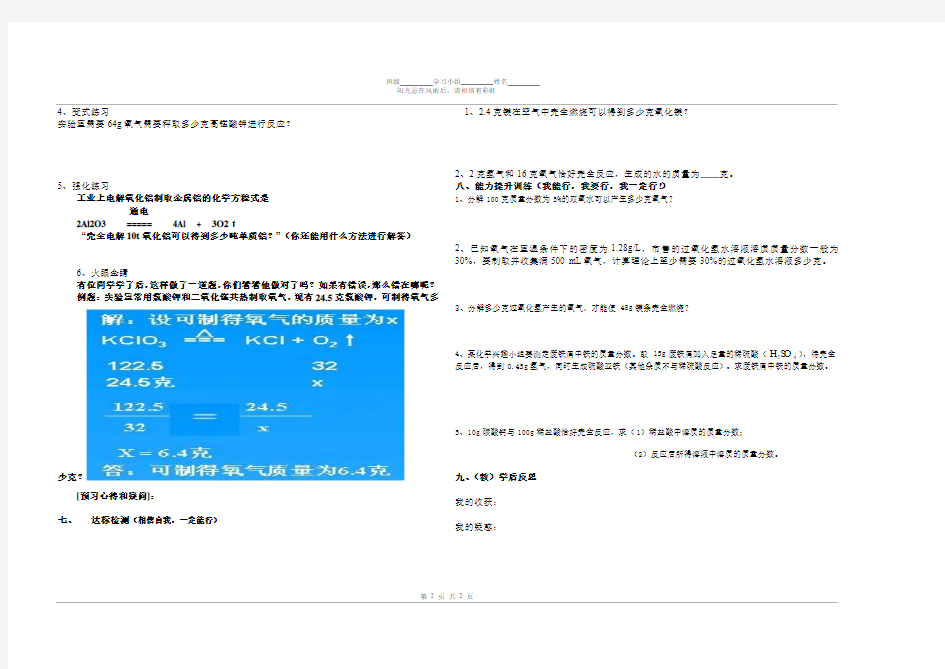
6、火眼金睛
有位同学学了后,这样做了一道题,你们看看他做对了吗?如果有错误,那么错在哪呢?
例题:实验室常用氯酸钾和二氧化锰共热制取氧气,现有24.5克氯酸钾,可制得氧气多
少克?
[预习心得和疑问]:
七、达标检测(相信自我,一定能行)
1、2.4克镁在空气中完全燃烧可以得到多少克氧化镁?
2、2克氢气和16克氧气恰好完全反应,生成的水的质量为克。
八、能力提升训练(我能行,我要行,我一定行!)
1、分解100克质量分数为5%的双氧水可以产生多少克氧气?
2、已知氧气在室温条件下的密度为1.28g/L,市售的过氧化氢水溶液溶质质量分数一般为30%,要制取并收集满500 mL氧气,计算理论上至少需要30%的过氧化氢水溶液多少克。
3、分解多少克过氧化氢产生的氧气,才能使48g镁条完全燃烧?
4、某化学兴趣小组要测定废铁屑中铁的质量分数。取15g废铁屑加入足量的稀硫酸(
4
2
SO
H),待完全反应后,得到0.45g氢气,同时生成硫酸亚铁(其他杂质不与稀硫酸反应)。求废铁屑中铁的质量分数。
5、10g碳酸钙与100g稀盐酸恰好完全反应,求(1)稀盐酸中溶质的质量分数;
(2)反应后所得溶液中溶质的质量分数。
九、(教)学后反思
我的收获:
我的疑惑:
初三化学专题复习导学案化学方程式
第五单元化学方程式复习导学案 可能用到的相对原子质量:Fe-56 O-16 S-32 Ca-40 C-12 K-39 Mn-55 Cl-35.5 【复习目标】: 1.认识质量守恒定律,能说明常见化学反应中的质量关系;能从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。 2.理解化学方程式的涵义,了解书写化学方程式要遵守的原则。能正确书写化学方程式。 3、掌握有关反应物、生成物质量的计算;掌握化学计算的解题格式,锻炼化学计算题的解题能力;通过有关化学反应的计算,能从定量的角度理解化学反应。 【知识梳理】: 一、质量守恒定律 1、质量守恒定律的内容:。理解时应该注意以下几点:(1)质量守恒定律适用于变化; (2)一切化学反应都遵循。 2、质量守恒定律的微观解释:化学反应的过程,就是的过程。在化学反应中,反应前后原子的没有改变,没有增减,也没有改变。 二、化学方程式: 1.化学方程式表示的意义:①质的意义 ②量的意义:通过相对分子质量的计算,可知 2.书写化学方程式遵守的原则: ;。3.正确书写化学方程式的步骤。 一“写”:根据事实,左边写反应物,右边写生成物,反应物或生成物不止一种时用“+”连接,反应物和生成物之间用“—”连接。 二“配”:在化学式前配上适当的化学计量数(并使之成最简整数比),使反应物和生成物中各元素的种类和原子个数都相等(遵守质量守恒定律),切不可改动化学式中的数字 ............! 一般用最小公倍数法或观察法。 三“改”:将短线改成等号。 四“注”:即注明反应发生的条件。 五“标”:气体用“↑”,液体中生成固体用“↓”,但当 ............. ..反应物和生成物中均有气体或 固体时,不须标出! ......... 2.利用化学方程式的简单计算 (1)计算的依据: (2)计算的步骤:①“设”②“写” ③“找”找出之间的质量关系④“列” ⑤“求”⑥“答”。 典型例题分析及点拨: 【例题1】根据所给信息书写化学方程式: (1)黑火药是我国古代四大发明之一,它是由硝石(KNO3)、木炭、硫粉组成, 点燃后生成硫化钾、二氧化碳和一种气体单质,并产生猛烈地爆炸威力。反应的化学方程式:点拨:根据题中提供的信息,分析出反应物、生成物、反应的条件,然后在等号的上面标出反应条件。根据质量守恒定律可知,黑火药爆炸后的已知产物中少了氮元素,故而产生
化学平衡计算专题导学案
太师庄中学高二化学选修4 化学反应原理导学案编制:王瑞燕审核:许文新张楠时间:4.2 第二章化学反应速率和化学平衡 化学平衡计算专题导学案 班级:小组:姓名:组内评价:教师评价: 【学习目标】1.理解转化率、百分含量、化学平衡常数的含义。 2.通过练习使学生掌握化学平衡的基本计算方法—三段式法。 3.培养学生逻辑思维能力和科学态度,培养学生归纳总结的能力。 【重点】化学平衡计算的基本方法。【难点】化学平衡综合计算。 复习回顾 1.阿伏加德罗定律: 同温同压下,相同体积的任何气体含有相同的。 2.化学平衡状态:指在一定条件下的里,,反应混合物中各 组分的浓度的状态。 3.化学平衡常数:在一定温度下,当一个可逆反应达到时, 与是一个常数,这个常数叫做该反应的化学平衡常数 4. 反应物:平衡浓度= 。生成物:平衡浓度= 合作探究 【例题】某温度下,在装有催化剂的容积为2 L的反应容器中,充入SO2和O2各4 mol ,发生如下反应:2SO2(g)+O2(g)2SO3(g),反应5 min后达到平衡,测得反应容器内混合气体的压强为原来的80 % ,回答下列问题: (1)用O2的浓度变化表示该反应的化学反应速率。 (2)求混合气体中,SO3的物质的量分数。 (3)求SO2的转化率。 (4)求该反应的平衡常数。 【归纳总结】(1)化学平衡计算的基本方法是 . (2)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时:p 1/p 2 = 恒温、恒压时:V 1 /V 2 = (3)恒温、恒容时,密度之比与物质的量之比的关系:ρ 1/ρ 2 = (4)化学反应速率表达式:。(其中△C是)(5)A的百分含量= A的转化率= 以上两个公式的单位可用、,也可用,但必须单位统一。(6)恒容时,化学反应速率之比= =。【基础练习】1. PCl5的热分解反应为:PCl 5 (g)PCl3(g)+Cl2(g) (1) 写出反应的平衡常数表达式: (2) 已知某温度下,在容积为10.0 L的密闭容器中充入2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.15 mol/L。计算该温度下的平衡常数。 【基础练习】2.合成氨反应N 2 (g)+3H 2 (g)=2NH 3 (g)在某温度下达到平衡时,各物质的浓度是 c(N 2 )=3mol/L, c(H 2 )=9mol/L, c(NH 3 )=4mol/L,求: ①该温度时的平衡常数; ②若NH 3 的起始浓度为0,求N 2 、H 2 的起始浓度。 拓展提升 1.将1molA(气)和3molB(气)混合后充入2L的密闭容器中,发生如下反应:2A(气)+B( 气) 2C(气),10min后反应达到平衡,同温同压下测得反应前后气体的密度之比为9∶10。 求(1)A物质的平均反应速率。 (2)A物质的转化率。 (3)C物质的百分含量 (4)反应后气体的压强与反应前压强之比。 【课堂反思】关于三段式法需要注意哪些问题? 【作业】1 图像专题导学案;2 将归纳总结部分的内容整理到笔记本上 1
化学平衡常数学案(含答案)
化学平衡常数学案 设计老师: 班级: 姓名: . 一、化学平衡常数 1、定义: 在一定温度下,当一个可逆反应达到平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数。这个常数就是该反应的化学平衡常数(简称平衡常数),用“K ”表示。 2、表达式: 对于一般的可逆反应:mA(g)+nB pC(g)+qd(g),当在一定温度下达到平衡时,K=________ 3、特点:K 只受_______和_______影响,与反应物或生成物的无关。 4、意义: (1).平衡常数的大小反映了化学反应进行的程度 ①K 值越大,说明平衡体系中生成物所占比例_________。它的正向反应进行的程度________,即该反 应进行得越_____,反应物的转化率_______。 ②K 值越小,说明平衡体系中生成物所占比例_________,它的正向反应进行的程度_______,即该反应进行的程度越_____,反应物的转化率___________。 ③.一般当K >______时,该反应进行得基本完全。 (2).判断正在进行的可逆反应是处于平衡状态及反应向何方向进行: 对于可逆反应:mA(g)+ nB(g)pC(g)+ qD(g),在一定的温度下的任意时刻,反应物的浓度和 生成物的浓度有如下关系: Q c 是该反应的浓度商。 Q c <K ,未达到平衡,反应向 进行, Q c =K ,反应处于平衡状态 Q c >K ,未达到平衡,反应向 进行 【温馨提示】: 化学平衡常数(K )与浓度商(Q c )的表达式相同,但在表达式中各物质的浓度不同,K 值中各物 质的浓度必须是平衡状态下的浓度,而Q c 值中是在任一时刻的浓度。 (3).利用K可判断反应的热效应 若升高温度,K值增大,则正反应为 反应(填“吸热”或“放热”)。 若升高温度,K值减小,则正反应为 反应(填“吸热”或“放热”)。 【问题思考】: 不同温度时,反应:H 2(g)+I 2(g) 2HI(g),的浓度平衡常数与温度的关系如下: 温度 623 698 763 化学平衡常66.9 54.4 45.9 ) ()()()(B c A c D c C c Q n m q p C
人教版九年级化学上册导学案 5.2 如何正确书写化学方程式
课题5.2 如何正确书写化学方程式 一、学习目标: 1.领会化学方程式、反应物与生成物的含义。 2.明确化学方程式中各种符号及化学意义。 3.学会正确书写化学方程式和配平简单化学方程式。(重难点) 【课前预习】 1.什么是质量守恒定律? 2.用原子、分子的观点解释质量守恒的原因。 3.用化学式完成下表中的化学反应(注明反应条件): 【情境导入】 二、自主探究: 【阅读】自学课本P99-100,完成以下问题: 1.书写化学方程式的原则:⑴必须以为基础;⑵遵 守。 2.书写化学方程式的步骤(以磷在空气中燃烧生成五氧化二磷为例): ⑴; ⑵; ⑶。 3.注意: ⑴化学方程式配平的标志:。 ⑵化学反应在一定条件下才能发生,因此,需要在化学方程式中注明, 如把点燃、加热(常用“△”来表示),催化剂等写在。 ⑶如果生成物中有气体,在气体物质的化学式右边要注号;溶液中的反应如果 生成物中有固体,在固体物质化学式右边要注号。 ■如果,气体生成物就不需注“↑”号,同样,溶液中的反应如 果,固体生成物也不需注“↓”。 1.最小公倍数法:寻找化学反应方程式左右两边各出现一次的原子,且原子个数相差最 多的元素为配平起点。 Fe2O3+C----Fe+CO2选择O原子为配平起点,由于3与2Fe2O3系 数为2,而CO2的系数为3,然后调节C与Fe2O3的系数分别为3和4,2Fe2O3+3C 4Fe+3CO2。
2.奇数配偶法:寻找反应式左右两边出现次数较多的原子,且原子的个数为一奇一偶的 元素为配平的起点。将奇数的原子用2、4、4、8….等偶数配成偶数,调节其他元素的原子 的个数。 Fe2O3+C----Fe+CO2选择O原子,因O Fe2O3用偶数2 配平,再依次推导出C、Fe2O3、CO2的系数,分别为3、4、3,即得2Fe2O3+3C 4Fe+3CO2。 3.观察法:当反应方程式两边有的物质组成较为复杂时,考虑用观察法。即观察分析反 应式左右两边相关物质的组成,从中找出其变化规律来确定各自化学式前的系数;在推导其 他原子的个数。 Fe2O3+C----Fe+CO2反应中:C-----CO2,C夺取了Fe2O3里两个O Fe2O3里的3个O原子可以供给3/2个C-----3/2个CO2,然后调节为整数系数为:2O3+3C 4Fe+3CO。 【课堂小结】通过本节课的学习,你收获了什么? 【我的收获】 【小结】 1、书写化学方程式的步骤: ⑴写:根据事实,左边写反应物,右边写生成物,反应物或生成物不止一种时用“+” 连接,反应物和生成物之间用“—”连接。 ⑵配:在化学式前配上适当的化学计量数(并使之成最简整数比),使反应物和生成物 中各元素的种类和原子个数都相等(遵守质量守恒定律),切不可改动化学式中的数字 ............!一 般用最小公倍数法或观察法。 ⑶标:即标明反应条件和生成物状态。气体用“↑”,液体中生成固体用“↓”,但当反 ... 应物和生成物中均有气体或固体时,不须注明!.....................将“—”改成“==”。 2、配平化学方程式的常用方法:①最小公倍数法;②奇数配偶法;③观察法。 三、自我测评 【课堂练习】 1.将“嫦娥一号” 送上太空的火箭推力巨大,因为它所使用的燃料是液氢、助燃剂是液氧, 则液氢燃烧的化学方程式为;液氢作燃料除了单位质量燃烧的热 能最大以外,还有一个与环保有关的优点是。 2.写出下列反应的化学方程式: (1)碳在氧气中燃烧; (2)硫在氧气中燃烧; (3)红磷在氧气中燃烧; (4)铁丝在氧气中燃烧; (5)氢气在氧气中燃烧; (6)镁条在空气中燃烧; (7)电解水; (8)过氧化氢溶液中加入二氧化锰; (9)氯酸钾和二氧化锰共热; (10)加热高锰酸钾固体; (11)铁和硫酸铜溶液反应; (12)碳酸钠和稀盐酸反应。
化学平衡常数和平衡转化率导学案
化学平衡常数与平衡转化率 设计者: 审核:高二化学组 【学习目标】 1、描述化学平衡建立的过程,学会判断化学平衡状态。 2、知道化学平衡常数的涵义,会求算某些化学反应的化学平衡常数。 3、了解浓度商的概念,并能利用浓度商与化学平衡常数的相对大小关系判断化学反应的方向 4、掌握平衡转化率的相关计算,了解平衡转化率与化学平衡常数的异同。 【课前预习区】 1、化学平衡状态的概念 化学平衡状态是指在一定条件下的 反应里, 相等,反应物不再 ,生成物不再 ,反应混合物中各组成成分的百分含量保持不变的状态。 [B] 表示反应体系中物质B 在化学平衡状态时的浓度 4、浓度商Q 的概念: 5、对于可逆反应:aA(g)+bB(g) cC(g)+ dD(g), 反应物A 的平衡转化率可以表示为: 反应物B 的平衡转化率可以表示为: 【课堂导学】 1、化学平衡状态的特点: 逆 动 等 定 变 问题组一 (1)什么叫做可逆反应? (2)你还知道生活中哪些反应是可逆的? (3)随着反应的进行,反应物和生成物的浓度如何变化?正、逆反应速率如何变化? (4)当反应进行到足够长时间后,反应物和生成物的浓度是否继续发生变化?正、逆反应速率是否为零? (5) 当反应进行足够长时间后,是否意味着反应就停止了? 【例题1】容积不变的密闭容器中,有反应 N 2(g)+3H 2(g) 2NH 3(g)下列能说明该反 应已达平衡状态的是: (1)N 2 、H 2 、NH 3的物质的量之比是1∶3∶2 (2)V (N 2):V (H 2) :V (NH 3)=1∶3∶2 (3)NH 3的生成速率和消耗速率相等 (4)H 2的生成速率和NH 3的消耗速率之比是3∶2 (5)各成分的质量不随时间变化 (6)单位时间内有1 molN 2 生成,同时有2molNH 3生成 (7)1 mol 氮氮键断开的同时有3 mol 氢氢键断开 (8)气体的总质量不随时间变化 (9)气体总物质的量不随时间变化 (10)体系的总压强不随时间变化 二、化学平衡常数(K )
【初三】初三化学专题复习导学案化学方程式
【关键字】初三 第五单元化学方程式复习导学案 可能用到的相对原子质量:Fe-56 O-16 S-32 Ca-40 C-12 K-39 Mn-55 Cl-35.5 【复习目标】: 1.认识质量守恒定律,能说明常见化学反应中的质量关系;能从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。 2.理解化学方程式的涵义,了解书写化学方程式要遵守的原则。能正确书写化学方程式。 3、掌握有关反应物、生成物质量的计算;掌握化学计算的解题格式,锻炼化学计算题的解题能力;通过有关化学反应的计算,能从定量的角度理解化学反应。 【知识梳理】: 一、质量守恒定律 1、质量守恒定律的内容:。理解时应该注意以下几点:(1)质量守恒定律适用于变化; (2)一切化学反应都遵循。 2、质量守恒定律的微观解释:化学反应的过程,就是的过程。在化学反应中,反应前后原子的没有改变,没有增减,也没有改变。 二、化学方程式: 1.化学方程式表示的意义:①质的意义 ②量的意义:通过相对分子质量的计算,可知 2.书写化学方程式遵守的原则: ;。3.正确书写化学方程式的步骤。 一“写”:根据事实,左边写反应物,右边写生成物,反应物或生成物不止一种时用“+”连接,反应物和生成物之间用“—”连接。 二“配”:在化学式前配上适当的化学计量数(并使之成最简整数比),使反应物和生成物中各元素的种类和原子个数都相等(遵守质量守恒定律),切不可改动化学式中的数字!一般用最小公倍数法或观察法。 三“改”:将短线改成等号。 四“注”:即注明反应发生的条件。 五“标”:气体用“↑”,液体中生成固体用“↓”,但当反应物和生成物中均有气体或固体时,不须标出! 2.利用化学方程式的简单计算 (1)计算的依据: (2)计算的步骤:①“设” ②“写” ③“找”找出之间的质量关系④“列” ⑤“求” ⑥“答” 。 典型例题分析及点拨: 【例题1】根据所给信息书写化学方程式: (1)黑火药是我国古代四大发明之一,它是由硝石(KNO3)、木炭、硫粉组成, 扑灭后生成硫化钾、二氧化碳和一种气体单质,并产生猛烈地爆炸威力。反应的化学方程式:点拨:根据题中提供的信息,分析出反应物、生成物、反应的条件,然后在等号的上面
【 精品导学案】高中化学 2.3.2化学反应的限度学案 新人教版必修二
第2课时化学反应的限度 1.了解化学反应的可逆性,知道化学反应是有一定限度的。 2.了解化学平衡状态的判定方法。 3.了解控制反应条件对生产、生活及科学研究的意义。 本课时宜从日常生活和实验中的化学现象引出有关的概念和原理,经过对化学反应的可逆性→可逆反应→化学平衡状态的分析推进,让学生认识化学反应是有限度的。 1.可逆反应 (1)在同一条件下,①正向反应(反应物→生成物)和②逆向反应(生成物→反应物)能同时进行的化学反应称为可逆反应。 (2)可逆反应的特点有“四同”:同一反应;(反应处于)同一条件;(正、逆反应)同时进行;(反应物和生成物)同时存在。 (3)可逆反应用化学方程式表示时,不用“”,而用“③”。 2.化学反应的限度 (1)化学平衡状态的建立 在密闭容器中加入1 mol H2和1 mol I2发生反应: H2(g)+I2(g)2HI(g) 对于以上反应: ①当反应刚开始时,反应物的浓度④最大。 ②当反应刚开始时,正反应速率⑤最大。 ③随着反应的进行,反应物浓度逐渐减小,生成物浓度逐渐增大。 ④随着反应的进行,v(正)逐渐减小,v(逆)逐渐增大,达到平衡时,v(正)=v(逆)。 ⑤反应进行到⑥v(正)=v(逆)时,宏观上处于“静止”状态。 ⑥此时,反应物和生成物浓度不再改变。 ⑦这个状态称为⑦化学平衡状态。 ⑧此时反应未停止,仍在进行,只是任何一种物质反应掉的速率和生成的速率相等。 (2)化学平衡状态的特点 化学平衡状态是可逆反应达到的一种特殊状态,是在给定条件下所能达到的最大限度,当可逆反应达到平衡状态时,v(正)=v(逆)≠0。 3.化学反应条件的控制 (1)在生产、生活中,化学反应条件的控制主要是促进有利反应和控制有害反应两个方面: ①促进有利反应,提高原料利用率,加快有利反应的速率; ②控制有害反应,减少甚至消除有害物质的产生,减慢有害反应的速率。 (2)为加快煤燃烧的反应速率,对煤炭颗粒的要求是⑧越小越好,对空气的要求是保持适当过量,并保证煤炭与空气中的氧气⑨充分接触。
化合价导学案
化合价导学案
九年级《化学》上册——《化学式与化合价》导学 案 2009年11月24日17:00:31 来源:博白县东平镇合江初级中学【字体:大中小】 课题4 化学式与化合价 【学习目标】 1、知识与技能 (1)了解化学式的涵义,并能用化学式表示某些常见物质的组成。 (2)熟记某些常见元素及原子团的化合价。 (3)能用化合价推求化学式。 (4)了解相对分子质量的涵义,并能利用相对原子质量、相对分子质量进行物质组成的简单计算。 (5)能看懂某些商品标签或说明书上标示的物质成分及其含量。 2、过程与方法 (1)通过对图、表的观察,让学生学会对所学知识进行整理归纳并初步运用,培养学生分析、归纳整理、寻找规律的学习能力。 (2)通过编顺口溜和小组比赛形式,激发学生学习的兴趣,培养学生科学的记忆方法。 3、情感态度与价值观 (1)通过交流讨论、活动探究,培养学生善于合作、勤于思考、勇于实践的精神。 (2)通过推求化学式的学习,使学生懂得只有确实存在的物质,才能根据化合价写出它的化学式,培养学生实事求是的思想品质。 (3)通过引导学生查看药品、食品等商品的标签或说明书,使学生感受到生活中处处充满化学,从而激发学生热爱学习、热爱生活的感情。 【学习建议】 1、本课题分2课时完成。第一课时学习课题的第一部分:化学式和第二部分:化合价;第二课时学习课题的第三部分:有关相对分子质量的计算。
2、本课题的学习要与生活实际密切联系,以实事求是和循序渐进的态度,认真分析图4-11和表4-6,充分展开你的想象,寻找最适合自己的记忆方法,大胆与同组的同学进行交流和PK。 第一课时化学式与化合价 第一部分化学式 【自主学习】 一、学习导航 当你看到下面的图片时(大球表示氧原子,小球表示氢原子),你会想到它表示什么意思? 二、阅读课文81-82页,并完成下列填空 1、用元素符号和数字的组合表示物质组成的式子,叫做_____。 2、写出下列物质的化学式 (1)氧气___,(2)水___,(3)二氧化碳___,(4)氮气__,(5)氢气__,(6)四氧化三铁___,(7)硫___,(8)氯化钠_____。 上述物质中属于单质的是_____,属于化合物的是_______。 3、化学式H2O的意义有:(1)表示________,(2)表示___________________,(3)表示___________________,(4)表示___________________。 4、由两种元素组成的化合物的名称,一般读作某化某。例如NaCl读作______,P2O5读作______,SO2读作______。 【合作学习与探究】 1、每种物质的组成是固定不变的,所以每种物质的化学式只有___个。 2、物质的组成是通过实验测定的,因此化学式的书写必须依据_______。 3、化学式的书写分单质化学式书写和化合物化学式书写 (1)单质化学式书写 ①由原子直接构成的物质,用_____表示。例如:硫___,磷___,
化学平衡状态 导学案
选修四第二章第三节化学平衡状态 本章导学: 1.掌握化学反应速率的计算和比较,掌握外界因素对化学反应速率的影响; 2.掌握化学平衡状态的特征、标志和外界因素对化学平衡状态的影响; 3.掌握化学平衡常数的应用和判断化学平衡移动的方向; 4.掌握有关化学平衡的计算题和图像题的做法和技巧。 第三节第一课时化学平衡状态 学习目标: 1.掌握化学平衡状态的特点 2.掌握化学平衡状态的判断方法 想一想: 1.影响化学反应速率的外界条件有: 等,此外还有光、固体表面积等其他因素。 2.列举三个学过的可逆反应: 特点: 特点: 特点: 3. 溶解平衡:当固体物质溶解进行到一定程度,固体溶质的速率与溶液中溶质的 速率相等,此时溶液处于饱和状态,溶液的浓度和固体溶质的质量都。 填一填: 一.可逆反应与不可逆反应 1.概念:在下,既能向方向进行又能向方向进行的化学反应。 2.表示方法:约定采用“”表示,把从左向右的反应称作,从右向左的反 应称作。例如:。 3.特征:; ; 。 4. 不可逆反应:有些化学反应的正反应进行程度特别大,逆反应进行程度太小因而可以忽略,把这 类反应叫做不可逆反应,用“”符号表示,例如: 。 二.化学平衡状态 1. 化学平衡状态的建立:在一定的条件下,把一个可逆反应的反应物加入固定体积的密闭容器中, 反应过程如下: 反应过程可表示如下:
2.化学平衡状态 (1). 概念:一定条件下,可逆反应中,正反应速率与逆反应速率相等,反应混合物中各种物质的保持不变的状态。 (2). 特征: 注意事项 (1)化学平衡状态是一定条件下的可逆反应进行到最大限度的结果。 (2)对于一个既定的可逆反应,如果其他条件一定,不论采取何种途径(反应是从反应物开始或 从生成物开始),最后都能建立化学平衡状态。 (3)化学平衡状态不会因时间变化而变化。 (4)可逆反应达到化学平衡状态的根本原因是v(正)=v(逆),正是由于各物质的消耗速率与生成 速率相等,才会有反应混合物中各组分的浓度保持不变。 (3).判断化学平衡状态的标志 对于可逆反应m A(g)+n B(g) p C(g)+q D(g)。 1.根本标志:v(正)=v(逆)≠0 常见形式主要有: (1)同一种物质的生成速率等于消耗速率。 如:v(A)生成=v(A)消耗。 (2)在化学方程式同一边的不同物质生成速率与消耗速率之比等于化学计量数之比。 如v(A)生成∶v(B)消耗=m∶n。 (3)化学方程式两边的不同物质生成(或消耗)速率之比等于化学计量数之比。 如:v(A)生成∶v(D)生成=m∶q。 2.特征标志 (1)各组分的浓度不随时间的改变而改变。 (2)各组分的质量分数、物质的量分数、体积分数不随时间的改变而改变。 (3)某种反应物的转化率不随时间的变化而变化。 (4)当m+n≠p+q时,体系的压强或平均相对分子质量不随时间的改变而改变。 试一试 [例1] (2012·郑州高二检测)下列对于反应C(g)+H2O(g) CO(g)+H2(g)的描述正确的是( )
最新2021高中化学第一轮复习导学案 (20)
第12课时练习 化学反应中的能量变化 胡文2021年 1.石油、煤、天然气等在地球上的蕴藏量是有限的,为缓解能源危机:①可以利用电解水的方法得到氢 气做能源;②可用酒精做能源;③砍伐树木做能源;④应开发太阳能、核能等新能源。上述说法正确的是 A. 只有① B. ①和④ C. ②和④ D. ④ 2.下列关于燃料充分燃烧的说法,不正确的是 A .空气量越多越好 B .应通入适量空气 C .固体燃料燃烧前要粉碎 D .液体燃料燃烧时可以以雾状喷出 3.甲烷和氢气燃烧的热化学方程式分别如下:CH 4(g )+2O 2(g )=CO 2(g )+2H 2O (l )△H 1,2H 2(g ) +O 2(g )==2H 2O (g )△H 2, 2H 2(g )+O 2(g )=2H 2O (l )△H 3常温下取体积为4:1的甲烷和氢气混合 气体11.2L (标况),完全燃烧后恢复常温,放出热量为 A.0.4△H 1+0.05△H 3 B.0.4△H 1+0.05△H 2 C.0.4△H 1+0.1△H 3 D.0.4△H 1+0.2△H 3 4.下列说法正确的是 A .在101kPa 时,1mol 物质完全燃烧时所放出的热量,叫做该物质的燃烧热 B .酸和碱发生中和反应生成1mol 水,这时的反应热叫中和热 C .燃烧热或中和热是反应热的种类之一 D .在稀溶液中,1molCH 3COOH 和1mol NaOH 完全中和时放出的热量为57.3kJ 5.已知反应X+Y=M+N 为放热反应,对该反应的说法正确的是 A.X 的能量一定高于M B.Y 的能量一定高于N C.X 和Y 的总能量一定高于M 和N 的总能量 D.因为该反应为放热反应,故不必加热就可发生 6.(09上海19)已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(l Q 、2Q 均为正值): 221222H (g)+Cl (g)2HCl(g)+Q H (g)+Br (g)2HBr(g)+Q →→有关上述反应的叙述正确的是 A .12Q >Q B .生成物总能量均高于反应物总能量 C .生成1molHCl 气体时放出l Q 热量 D .1mol HBr(g)具有的能量大于1mol HBr(1)具有的能量 7.(09天津卷6)已知: 2CO(g)+O 2(g)=2CO 2(g)ΔH=-566 kJ/mol Na 2O 2(s)+CO 2(g)=Na 2CO 3(s)+1/2O 2(g)ΔH=-226 kJ/mol 根据以上热化学方程式判断,下列说法正确的是 A.CO 的燃烧热为283 kJ B.右图可表示由CO 生成CO 2的反应过程和能量关系 C.2Na 2O 2(s)+2CO 2(s)=2Na 2CO 3(s)+O 2(g) ΔH >-452 kJ/mol D.CO(g)与Na 2O 2(s)反应放出509 kJ 热量时,电子转移数为6.02×10 23 8.(09四川卷9)25 ℃,101 k Pa 时,强酸与强碱的稀溶液发生中和反应的中 和热为57.3 kJ/mol ,辛烷的燃烧热为5518 kJ/mol 。下列热化学方程式书写正确的是 A.2H +(aq) +24SO -(aq)+2Ba +(aq)+2OH -(aq)=BaSO 4(s)+2H 2O(1);?H=-57.3 kJ/mol B.KOH(aq)+1/2H 2SO 4(aq)= 1/2K 2SO 4(aq)+H 2O(l);?H=-57.3kJ/mol C.C 8H 18(I)+ 25/2O 2 (g)=8CO 2 (g)+ 9H 2O (g );?H=-5518 kJ/mol D.2C 8H 18(g)+25O 2 (g)=16CO 2 (g)+18H 2O(1);?H=-5518 kJ/mol 9.(09全国卷Ⅱ11) 已知:2H 2(g )+ O 2(g)=2H 2O(l) ΔH= -571.6KJ· mol -1 CH 4(g )+ 2O 2(g)=CO 2(g)+2H 2O(l) ΔH= -890KJ· mol -1 现有H 2与CH 4的混合气体112L (标准状况),使其完全燃烧生成CO 2和H 2O(l),若实验测得反应放热3695KJ , 则原混合气体中H 2与CH 4的物质的量之比是 A .1∶1 B.1∶3 C .1∶4 D.2∶3 10. (09重庆卷12)下列热化学方程式正确的是(H ?的绝对值均正确) A .C 2H 5OH (l )+3O 2(g )==2CO 2(g )+3H 2O (g );△H=—1367.0 kJ/mol (燃烧热) B . NaOH (aq )+HCl (aq )==NaCl (aq )+H 2O (l );△H=+57.3kJ/mol(中和热) C .S (s )+O 2(g )===SO 2(g );△H=—269.8kJ/mol (反应热)
化学平衡常数学案
化学平衡常数 适用学科化学适用年级高二适用区域天津课时时长(分钟)60 知识点化学平衡常数的定义 影响平衡常数的因素 学习目标1、化学平衡常数的概念 2、化学平衡常数表达式 3、影响化学平衡常数的因素 学习重点1、化学平衡常数的概念 2、化学平衡常数的表达式 学习难点1、化学平衡常数表达式 学习过程 一、复习预习 平衡常数表达式及其意义 对于化学反应mA+nB pC+qD 在一定温度下达到化学平衡时,其平衡常数表达式为: 二、知识讲解
考点1、平衡常数的书写 在应用平衡常数表达式时,稀溶液中的水分子浓度可不写。因为稀溶液的密度接近于1 g/mL。水的物质的量浓度为55.6 mol/L。在化学变化过程中,水量的改变对水的浓度变化影响极小,所以水的浓度是一个常数,此常数可归并到平衡常数中去。例如: 平衡常数表达式为: 对于非水溶液中的反应,溶剂的浓度同样是常数。 考点2、含有固体物质的平衡常数书写 当反应中有固体物质参加时,分子间的碰撞只能在固体表面进行,固体的物质的量浓度对反应速率和平衡没有影响,因此,固体的“浓度”作为常数,在平衡常数表达式中,就不写固体的浓度。例如,赤热的四氧化三铁与氢气的反应: 平衡常数K=c(CO2) 考点3、系数为分数的平衡常数书写 化学平衡常数表达式与化学方程式的书写方式有关。同一个化学反应,由于书写的方式不同,各反应物、生成物的化学计量数不同,平衡常数就不同。但是这些平衡常数可以相互换算。例如:氨的合成反应,如写成
三、例题精析 【例题1】 【题干】下列说法正确的是() A.凡是放热反应都是自发的,因为吸热反应都是非自发的 B.自发反应的熵一定增大,非自发反应的熵一定减小 C.常温下,反应C(s)+CO2(g)2CO(g)不能自发进行,则该反应的ΔH>0 D.反应2Mg(s)+CO2(g)===C(s)+2MgO(s)能自发进行,则该反应的ΔH>0 【答案】C 【解析】反应的自发性是由熵变和焓变共同决定的。若ΔH<0,ΔS>0,则一定自发,若ΔH>0,ΔS<0,则一定不能自发,若ΔH<0,ΔS<0或ΔH>0,ΔS>0,反应能否自发,和温度有关,A、B错误;C项中反应的ΔS>0,若ΔH<0,则一定自发,现常温下不自发,说明ΔH>0,正确;D项中反应的ΔS<0,能自发,说明ΔH<0,错误。 【例题2】 【题干】反应Fe(s)+CO2(g)=FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是() A.升高温度该反应的正反应速率增大,逆反应速率减小
化学式学案
课题4 化学式与化合价 第1课时化学式 1.了解化学式的含义。了解化学式前、中有关数字的不同意义。 2.学会根据规定书写和读出一些简单的化学式。 ●温故互查默写30个常见元素符号及名称 化学式 ●自主预习 阅读课文83页,并完成下列填空 1. 的组合表示物质组成的式子,叫做化学式。 2.任何纯净物都有的组成,每种纯净物只有个化学式,混合物化学式。 3.写出下列物质的化学式。 (1)氧气,(2)水,(3)二氧化碳2,(4)氮气,(5)氢气,(6)四氧化三铁,(7)硫,(8)氯化钠。 上述物质中属于单质的是,属于化合物的 4.化学式H2O的意义有:(1)表示水这种物质,(2)表示1个水分子,(3)表示水由氢元素和氧元素组成,(4)表示1个水分子由2个氢原子和1个氧原子组成。 ●小组讨论 1.化学式能表示哪些意义?其中有哪些意义属于宏观意义?有哪些属于微观意义?请举一例说明。 2.化学式前面和化学式中元素符号右下角的数字各表示什么意义? (1)化学式前面的数字表示有几个这样的分子或原子。 (2)化学式中元素符号右下角的数字表示一个分子中有几个这样的原子。 ●教师点拨 化学式右下角的数字表示一个分子中有几个这样的原子;化学式前面的数字表示几个这样的分子或原子,只表示微观意义。金属、稀有气体和固态非金属的化学式表示3种意义:一种元素;一个原子;这种物质。 ●跟踪练习 1.2H2O中,前面的“2”表示,元素符号H右下角的“2”表示 2.下列化学符号表示两个氢分子的是C,表示两个氢原子的是()。 A.2H B.H2 C.2H2 D.2H2O 3.下列符号只具有微观意义的是() A.2H B.H2 C.H E.H2O F.2H2O 4.既能表示某元素,又能表示该元素的一个原子,还能表示一种物质的是() A.H B.2O2 C.N2 D.Hg E.2He 5.O2除可以表示氧气还可以表示:①氧元素;②一个氧分子;③两个氧元素;④氧气由氧元素组成;⑤每一个氧分子由两个氧原子构成;⑥两个氧原子。正确的是( ) A.①②③ B.②④⑤ C.②④⑥ D.①④⑥
化学平衡判据导学案
化学平衡状态的判定 班级 姓名 小组 【学习目标】 1. 回顾化学平衡特征,正确利用v 正=v 逆及各组分含量是否变化来判断反应是否达到平衡 2. 结合M 、ρ的计算公式,正确判断反应在进行过程中M 、ρ、n 总、P 如何变化。 3. 结合反应的Δn 及是否有固体参与,正确分析M 、ρ、n 总、P 不变能否说明反应达平衡态。 4. 结合变量不变的思想,正确判断所给条件反应是否达平衡状态。 【重点难点】 重点:不同反应M 、ρ、n 总、P 不变时判断反应是否达平衡状态;“变量不变”思想应用。 难点:不同反应M 、ρ、n 总、P 不变时判断反应是否达平衡状态。 【导学流程】 一.知识链接 V m =ρ 总总n m =M PV=nRT(注:当V 、T 不变时,n 不变则P 不变) 二.基础感知 1.在2L 容器中进行反应:H 2(g )+I 2(g ) 2HI (g ),下列能说明反应达平衡的为 。 ①H 2转化率不变 ②H 2与I 2的转化率相同 ③H 2体积分数不再变化 ④若反应在绝热条件下进行,温度不再发生改变 ⑤体系的颜色不再改变 ⑥2v(H 2)=v (HI ) ⑦生成1molH 2的同时消耗2molHI 2.(1) 在体积不变的容器内充入1 mol N 2和3mol H 2发生下列反应:N 2+3H 22NH 3 ①在反应过程中,气体的总质量、体积是否变化? ②在表格中填写(变/不变) n 总 P ρ M 反应进行中未达到平衡时 平衡时 表格中四个量哪个不变时可以判断反应达到平衡状态?(下面两个表格也是相同的问题) (2) 对于恒容条件下发生反应H 2(g )+I 2 (g)2HI (g ) ①在反应过程中,气体的总质量、体积是否变化? ②在表格中填写(变/不变) n 总 P ρ M 反应进行中未达到平衡时 平衡时 (3)在恒容条件下发生反应A(s)+B(g) C(g) ①在反应过程中,气体的总质量、体积是否变化? ②在表格中填写(变/不变) n 总 P ρ M 反应进行中未达到平衡时 平衡时 3.①恒压条件下进行N 2+3H 22NH 3,压强不变的条件下,能否说明反应达平衡? ②C(s)+H 2O(g) CO(g)+H 2(g),此反应H 2的体积百分数不变能否说明反应达平衡? ③在体积不变的容器中充1mol NH 4Br 发生反应:NH 4Br(s)NH 3(g)+HBr(g),NH 3的体积百分数不变能否说明反应达平衡?
5.2化学方程式导学案.doc
课题:5.2 书写化学方程式 【学习目标】: 1.了解化学方程式的定义和意义 【学习重点】:正确书写化学方程式【难点】化学方程式的配平。 【经典回顾】:1.用质量守恒定律说明下列叙述是否正确? (1)化学反应前后,各物质的质量保持不变。 (2)13g碳和32g氧气充分反应后,只能生成44g二氧化碳,这一过程符合质 量 守恒定律。 (3)发生化学变化时,原子的种类和个数都保持不变。 (4)参加反应的各物质的总体积,等于各生成物的总体积。 【导学过程】阅读课本96页完成下列内容。 【导学1】化学方程式的定义和意义 1?什么是化学方程式? _______________________________________________ 2?化学方程式表示什么?它与文字表达式有什么不同? 化学方程式:从定性的角度表明了______________________________________ 从定量角度表明了_________________________________________ 3?P+O2TP2O5这个式子是化学方程式吗?它符合质量守恒定律吗? 【预习自测1】 1.用 _______ 来表示化学反应的式子叫_____ ,又叫________ O 2.化学方程式2Mg+O2===2MgO的读法是: %1_________ 和________ 在 ____ 条件下反应生成_________ o %1每____ 份质量的镁和_____ 份质量的氧气恰好完全反应生成_____ 份质量
的氧化镁。 %1Mg、O2、MgO微粒个数比_________ 。
水和 份质量的氧气 5 ?计算化学方程式中各物质的质量比:(只列式子不计算) 点燃 4P+502====2P 205中 P 、02、P2O5的质量比为: ____________ 2H 2+02====2H 20中比、02、也0的质量比为: ______________ 2KCIO 3^=2KCI +3O 2 t 中 KC103> KC1> O2的质量比 _______________________________________________________ 2KMn0 === K MnO +MnO +0 f 中 KMnO . K MnO . Mn0. O2 的质 (1) (3) (4) 点燃 3. 在 3Fe+202 Fe3()4 反应中: ⑴反应物是 __________ 和 _____________ O (2) _____________________ 每—份质量的铁和 _________________ 份质量的氧气恰好完全反应生成 ____ 份质量的 四氧化三铁。 (3) __________________________________ Fe> 02. Fe 304微粒个数比 , Mn02 一 亠, 4、在 2H2O2 ===2H 20t + Ozf 反应中, (1) 反应物是 _________ 和 _____________ o (2) 每—份质量的过氧化氢在二氧化猛做催化剂的条件下生成 份质量的 (3) H 202>也0、O2微粒个数比
化学平衡计算--“三段式”法导学案
化学平衡计算--“三段式法”导学案【题型认识】 例题1:在某温度下,容积为20L的容器中充入2molSO 2和1molO 2 发生反应: 2SO 2 (g)+O 2 (g) 2SO 3 (g), 10min达到平衡时,容器内气体压强为开始时的70%。试求: ①10min内v(O 2) ②SO 2 的转化率③平衡时的SO 3 浓度 ④SO 3 的体积分数⑤混合气体的平均相对分子量⑥平衡时混合气体的密度 ⑦该温度下的平衡常数K 例题2:在密闭容器中,将1.0 mol CO与1.0 mol H2O混合加热到800℃,发生下列反应: CO(g)+H2O(g)CO2(g)+H2(g) 一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是() A.800℃下,该反应的化学平衡常数为0.25 B.427℃时该反应的平衡常数为9.4,则该反应的△H>0 C.该条件下,平衡体系中CO2的体积分数为20% D.800℃下,若继续向该平衡体系通入1.0 mol的H2O(g),则平衡时CO转化率为66.7 % 【解题思路】 化学平衡的计算一般涉及到各组分的物质的量、浓度、速率、转化率、百分含量、气体混合物的密度、平均摩尔质量、压强等,通常的思路是写出化学方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的关系,列出比例式或等式或依据平衡常数求解。 1.计算模式: mA(g) + nB(g) pC(g) + qD(g) 起始量 变化量 平衡量 “三段式法”是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol、mol/L,也可用L。反应可从左向右开始,也可以从右向左开始,也可以多种物质同时充入。可逆反应达到平衡状态时各物质浓度间的关系。反应物:平衡浓度=起始浓度-转化浓度;生成物:平衡浓度=起始浓度+转化浓度,其中各物质的转化浓度之比等于它们在化学方程式中各物质的化学计量数之比。
化学平衡学案
专题八 化学平衡 【考纲展示】 1.了解化学反应速率的概念、反应速率的定量表示方法。理解外界条件(温度、浓度、压强、催化剂等)对反应速率的影响。 2.了解催化剂在生产、生活和科学研究领域中的重大作用。 3.了解化学平衡建立的过程。了解外界条件(温度、浓度、压强、催化剂等)对反应平衡的影响,认识其一般规律。 4.理解化学平衡常数的含义,能利用化学平衡常数进行简单计算。 5.了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。 6.以上各部分知识的综合应用。 【知识网络】 知识网络 化学反应速率与化学平衡 表示方法:v= c/t 单位:或mol/L·min 公式法简单计算 化学计量数之比法影响因素 内因:反应物的结构、性质 外因 浓度:c 增大,v 增大压强:P 增大, v 增大温度:T 升高,v 增大 催化剂:使用催化剂一般加快反应速率 化学平衡 概念:可逆反应,条件一定,v 正 =v 逆特征:逆、等、动、定、变原因:外界条件变化,正、逆反应速率不同程度改变结果:再次v 正=v 逆 ,各组分百分含量又不变方向 v 正>v 逆,平衡正向移动v 正
- 《化学反应热的计算》 导学案
- 4.4 化学方程式 课时一导学案
- 热化学方程式的书写以及意义导学案
- 【初三】初三化学专题复习导学案化学方程式
- 书写化学方程式第1课时导学案
- 含杂质的化学方程式计算导学案
- 1.3化学反应热的计算 导学案
- 《利用化学方程式的简单计算》导学案2
- 24热化学方程式及反应热的计算(无答案)-河北省涞水波峰中学高三化学二轮复习导学案
- 导学案:5-6化学式和化学方程式的书写
- 高中化学 精准导学案 热化学方程式
- 初三化学专题复习导学案化学方程式
- 利用化学方程式的简单计算导学案
- 热化学方程式导学案
- 热化学方程式导学案
- 初三上册化学 化学方程式导学案
- 5.2化学方程式导学案.doc
- 第五单元化学方程式导学案
- 利用化学方程式的简单计算优秀导学案
- 2020高中化学 第一章 化学反应与能量 第三节 化学反应热的计算导学案 新人教版选修4
